Clear Sky Science · zh
SPINK2 沉默通过下调 MECOM 抑制急性髓系白血病的增殖并恢复髓系分化
这对血癌意味着什么
急性髓系白血病(AML)是一种进展迅速的血液恶性肿瘤,未成熟的白细胞占据骨髓,挤压正常造血。许多患者,尤其是那些白血病细胞具有多处染色体异常(所谓复杂核型)的人,对现有药物反应不佳。本研究发现了一种名为 SPINK2 的分子,它是白血病细胞维持增殖并逃避成熟为正常血细胞的关键帮手。由于可以在实验条件下关闭 SPINK2,这为减缓疾病并促使癌细胞回归更健康命运提供了新的潜在途径。
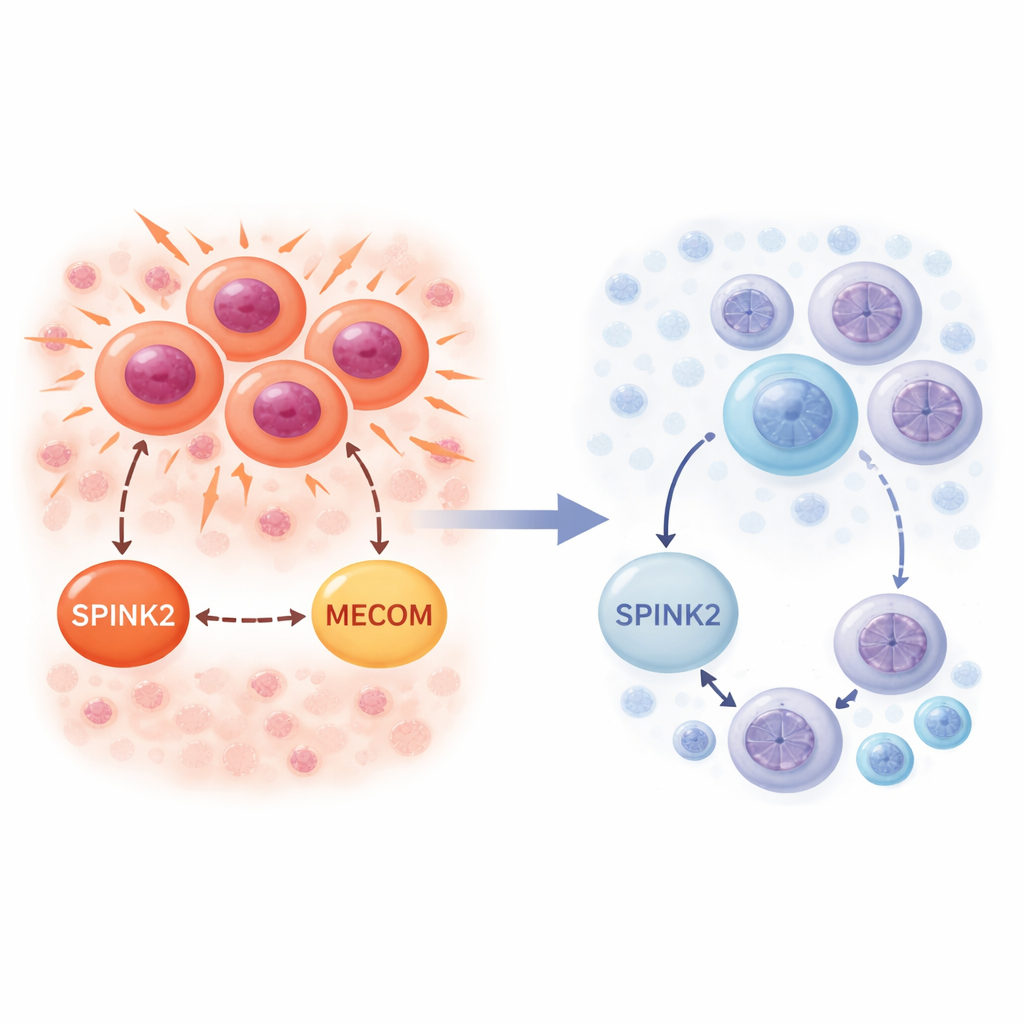
早期造血干细胞中的一个开关
研究者首先探查了 SPINK2 在健康骨髓中的正常分布。利用单细胞 RNA 测序数据——逐细胞测量基因活性——他们发现 SPINK2 主要在标记为 CD34 的最原始造血干/祖细胞中被打开。这些细胞处于静止或缓慢循环状态,位于造血谱系的顶端。随着细胞沿髓系或淋巴系成熟,SPINK2 活性迅速下降,并在成熟血细胞中几乎不可检测。这个模式表明 SPINK2 属于定义早期干样细胞状态的程序之一,通常在细胞一旦决定承担特定功能时被关闭。
同一开关在白血病中助长肿瘤生长
团队接着在 AML 患者的白血病骨髓中考察了 SPINK2。同样利用单细胞数据,他们发现 SPINK2 在那些最类似干细胞的白血病细胞以及高速循环的 AML 浆母细胞中都很活跃。与健康组织不同的是,这里 SPINK2 与细胞周期基因的强烈信号并行,尤其是驱动 DNA 复制的 S 期基因。在来自大型癌症基因组项目的群体样本中,较高的 SPINK2 水平与更差的生存期相关,并且在复杂核型 AML 患者中显著升高。这些观察结果表明,白血病细胞劫持了一个干细胞基因,通过 SPINK2 支持持续分裂同时维持原始表型。
关闭 SPINK2 放慢癌变并促其成熟
为了验证 SPINK2 是标记而非真正驱动因子,科学家们将一个代表复杂核型疾病的 AML 细胞系 FUJIOKA 工程化,携带一个能被多西环素诱导的短发夹 RNA,以选择性沉默 SPINK2。当关闭 SPINK2 时,白血病细胞分裂速度明显放慢。详细的细胞周期分析显示,许多细胞被滞留在 G0/G1 期,无法进入 S 期和 G2/M 期,且未观察到明显的细胞死亡增加。与此同时,细胞表面开始出现更高水平的典型成熟髓系细胞标志,表明常见的发育阻滞有所缓解。换言之,失去 SPINK2 即削弱了增殖推动力,又解除分化的刹车。
与另一白血病驱动因子的分子联系
对 FUJIOKA 细胞在 SPINK2 沉默前后的 RNA 测序揭示了广泛的基因活性变化。数百个控制细胞周期、染色体分离和有丝分裂检查点的基因被下调,而与蛋白合成和免疫反应相关的一组基因被上调。其中一个显著靶点是 MECOM,一种已知促进白血病的转录因子,它帮助干样细胞自我更新并抑制髓系成熟。SPINK2 被沉默后,MECOM 表达显著下降。对一项大型儿童 AML 数据集的分析证实,对于复杂核型患者,SPINK2 与 MECOM 水平往往同步升降。这指向了一个 SPINK2–MECOM 轴,可能在高危 AML 中协调过度自我更新与增殖。
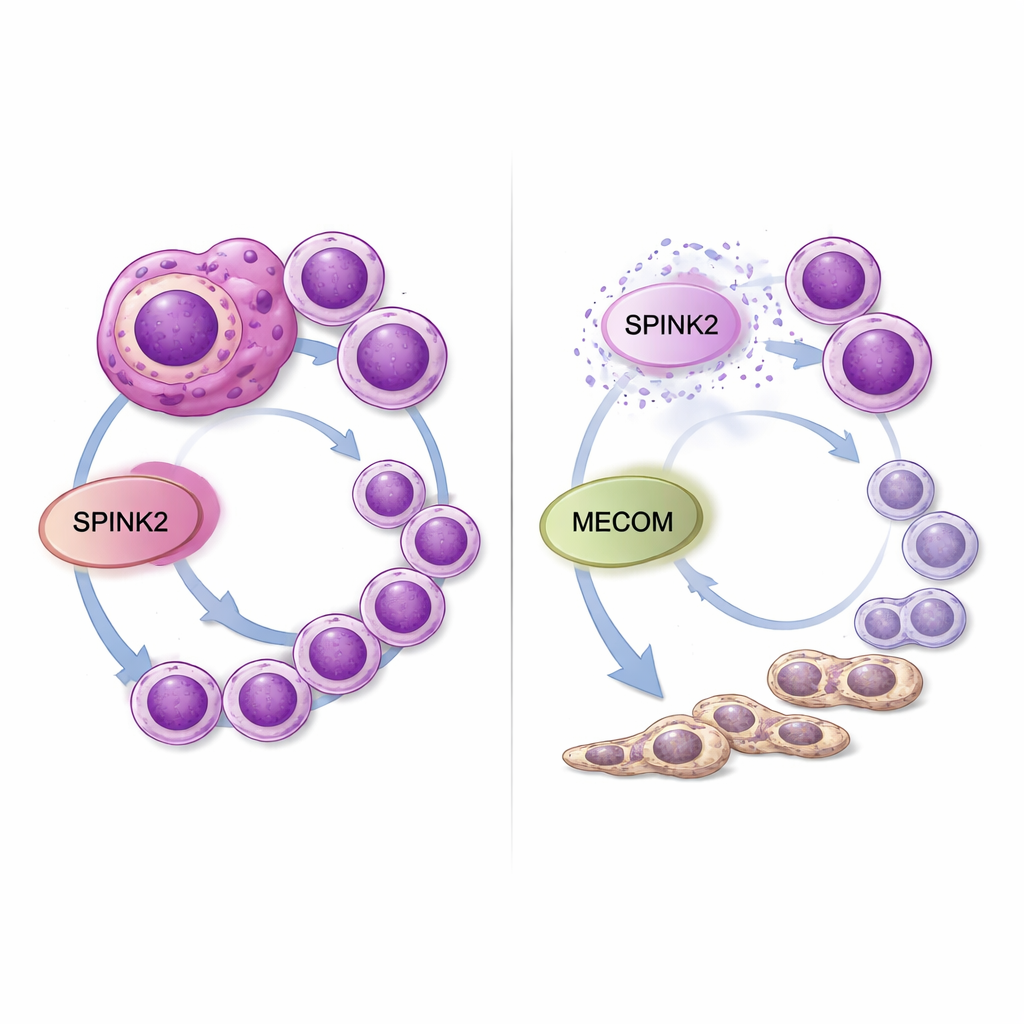
这对未来治疗的意义
对普通读者而言,这些发现表明 SPINK2 在白血病细胞中像一个被调得过高的隐性旋钮:它让细胞保持年轻的干样状态并促使它们不受控制地增殖。在实验室中下调 SPINK2 既减缓了癌细胞,又促使它们向更正常的髓系细胞分化,同时降低了另一个危险基因 MECOM 的活性。由于 SPINK2 通常仅限于早期造血干细胞,并在大多数成年组织中处于沉默状态,针对该分子或其与 MECOM 的相互作用的药物可能选择性地削弱侵袭性 AML——尤其是复杂核型病例——而不会严重损害正常造血。仍需在动物模型和药物开发方面进行进一步工作,但这项研究将 SPINK2 标记为一种在亟需更好治疗方案的白血病类型中的有前景的新脆弱点。
引用: Ventura, A.B., Loconte, T., Ahmed, A. et al. SPINK2 silencing suppresses leukemic proliferation and restores myeloid commitment via MECOM downregulation in acute myeloid leukaemia. Cell Death Discov. 12, 135 (2026). https://doi.org/10.1038/s41420-026-02988-1
关键词: 急性髓系白血病, SPINK2, 白血病干细胞, MECOM, 髓系分化