Clear Sky Science · sv
SPINK2-tystnad dämpar leukemisk proliferation och återställer myeloid åtagande via nedreglering av MECOM vid akut myeloisk leukemi
Varför detta är viktigt för blodcancer
Akut myeloisk leukemi (AML) är en snabbväxande blodcancer där omogna vita blodkroppar tar över benmärgen och tränger undan normal blodbildning. Många patienter, särskilt de vars leukemiceller bär många kromosomala avvikelser (så kallade komplexa karyotyper), svarar dåligt på dagens läkemedel. Denna studie identifierar molekylen SPINK2 som en nyckelassistent som tillåter leukemiceller att fortsätta dela sig samtidigt som de vägrar mogna till normala, färdiga blodkroppar. Eftersom SPINK2 kan stängas av experimentellt kan den erbjuda ett nytt sätt att bromsa sjukdomen och styra cancerceller tillbaka mot ett friskare öde.
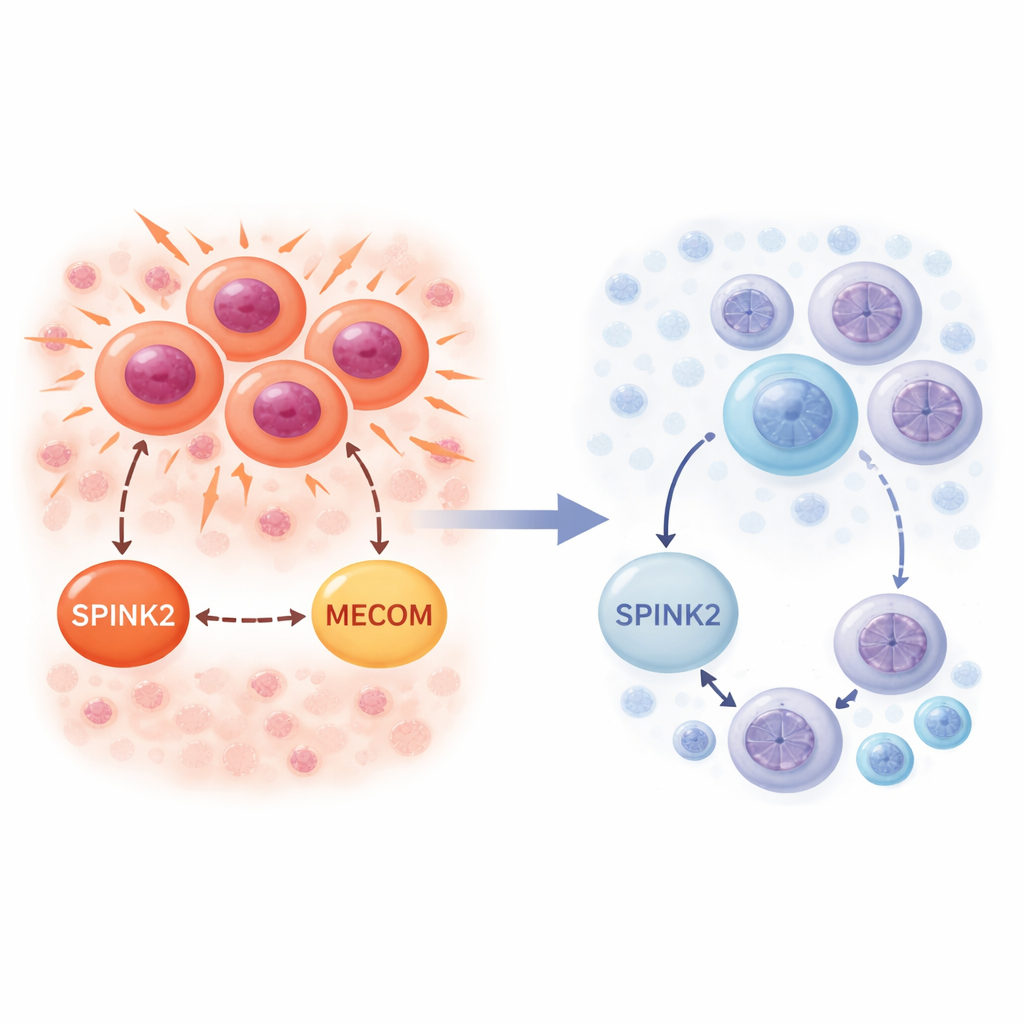
En strömbrytare som hittas i tidiga blodstamceller
Forskarna undersökte först var SPINK2 normalt uttrycks i frisk benmärg. Med hjälp av enkelcells-RNA-sekvenseringsdata, som mäter genaktivitet cell för cell, fann de att SPINK2 främst är påslaget i de mest primitiva blodstam‑ och progenitorcellerna märkta med CD34. Dessa är vilande, långsamt cyklerande celler som sitter högst upp i blodcellernas släktträd. När celler mognar längs antingen myeloida eller lymfoida banor sjunker SPINK2-aktiviteten kraftigt och är i princip frånvarande i fullt utvecklade blodceller. Detta mönster tyder på att SPINK2 är en del av programmet som definierar mycket tidiga stamliknande celler och normalt stängs av när celler bestämmer sig för en specifik uppgift.
När samma strömbrytare driver leukemitillväxt
Teamet studerade sedan SPINK2 i leukemisk benmärg från patienter med AML. Återigen med enkelcellsdata fann de att SPINK2 var aktiv i leukemiceller som mest liknade stamceller, samt i snabbt delande AML-blaster. Till skillnad från det friska sammanhanget gick här SPINK2 hand i hand med starka signaler från cellcykelgener, särskilt de som driver DNA-kopierande S‑fasen. I stora patientkohorter från större cancer‑genomikprojekt kopplades högre SPINK2-nivåer till sämre överlevnad och var särskilt förhöjda hos personer med komplex karyotyp-AML. Tillsammans tyder dessa observationer på att leukemicellerna har kapat en stamcellsgen och använder SPINK2 för att understödja obeveklig delning samtidigt som de bevarar en primitiv identitet.
Att stänga av SPINK2 bromsar cancern och skjuter den mot mognad
För att testa om SPINK2 bara är en markör eller en verklig drivkraft konstruerade forskarna en AML-cellinje kallad FUJIOKA—som representerar komplex karyotyp-sjukdom—så att den bar en doxycyklin‑inducerbar kort hårnål‑RNA som selektivt tystar SPINK2. När SPINK2 stängdes av delade leukemicellerna mycket långsammare. Detaljerad analys av cellcykeln visade att många celler fastnade i G0/G1‑fasen och inte gick vidare genom S och G2/M, utan någon påtaglig ökning av celldöd. Samtidigt började cellerna visa högre nivåer av ytmolekyler typiska för mogna myeloida celler, vilket indikerar att den vanliga utvecklingsblockaden lättade. Med andra ord tog SPINK2-bortfall både bort tillväxtstödet och släppte bromsen på differentiering.
En molekylär koppling till en annan leukemidrivare
RNA‑sekvensering av FUJIOKA‑celler före och efter SPINK2‑tystnad avslöjade omfattande förändringar i genaktivitet. Hundratals gener som kontrollerar cellcykeln, kromosomsegregering och mitotiska checkpointar nedreglerades, medan genuppsättningar kopplade till proteinsyntes och immunsvar uppreglerades. En framträdande var MECOM, en välkänd transkriptionsfaktor som främjar leukemi, hjälper stamliknande celler att självförnya sig och förhindrar myeloid mognad. MECOM‑uttrycket sjönk kraftigt när SPINK2 tystades. Analyser av en stor pediatrisk AML-dataset bekräftade att SPINK2‑ och MECOM‑nivåer tenderar att stiga och falla tillsammans, särskilt hos patienter med komplexa karyotyper. Detta pekar på en SPINK2–MECOM‑axel som kan samordna överdriven självförnyelse och delning i hög‑risk AML.
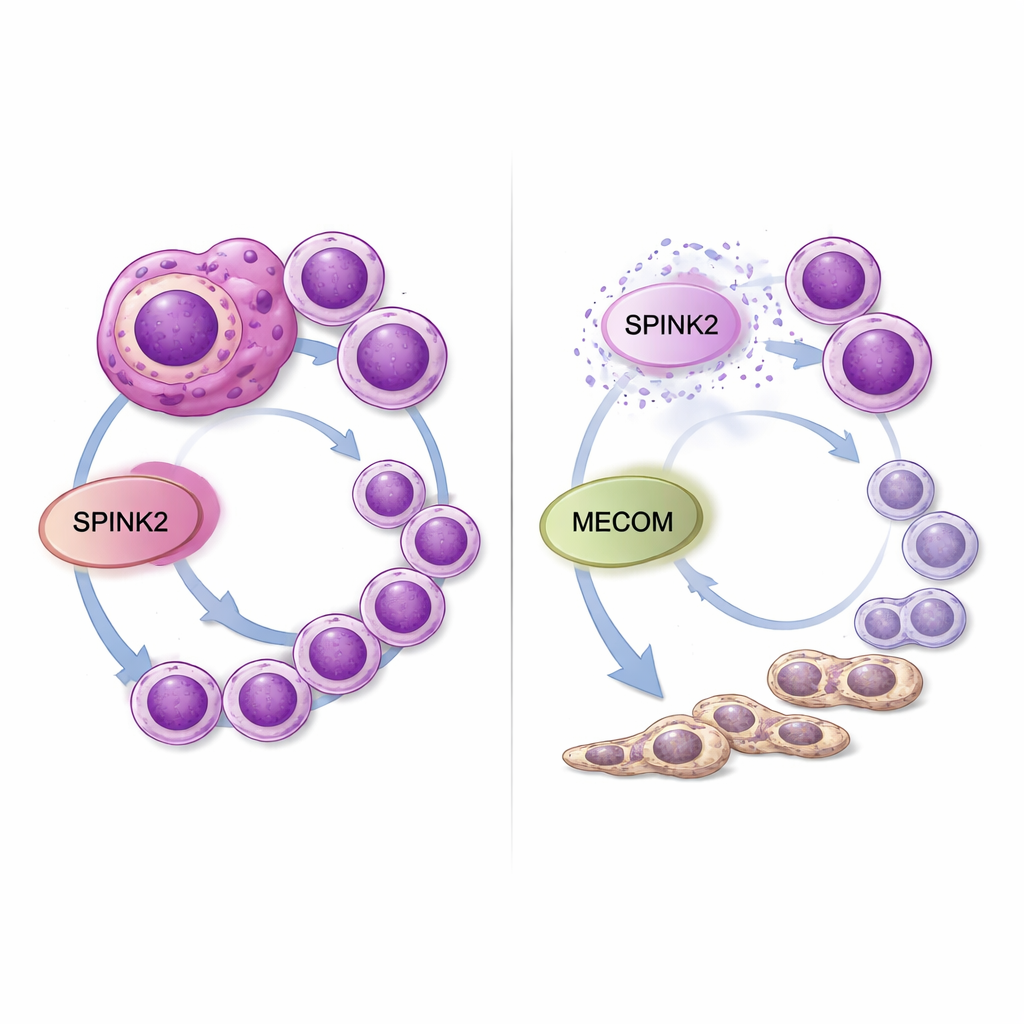
Vad detta betyder för framtida behandlingar
För en lekmannabetraktare tyder dessa fynd på att SPINK2 fungerar som en dold ratt i leukemiceller som vridits upp för högt: den håller cellerna i ett ungdomligt, stamliknande tillstånd och uppmuntrar dem att föröka sig okontrollerat. Att vrida ner SPINK2 i labbet både bromsar cancercellerna och uppmuntrar dem att mogna till mer normala myeloida celler, samtidigt som aktiviteten i en annan farlig gen, MECOM, minskar. Eftersom SPINK2 normalt är begränsad till tidiga blodstamceller och i stort sett tyst i de flesta vuxna vävnader, kan läkemedel som riktar in sig på denna molekyl eller dess samspel med MECOM selektivt försvaga aggressiv AML—särskilt fall med komplex karyotyp—utan att allvarligt skada normal blodbildning. Ytterligare arbete i djurmodeller och läkemedelsutveckling krävs, men denna studie utpekar SPINK2 som en lovande ny svag punkt i en form av leukemi som akut behöver bättre behandlingsalternativ.
Citering: Ventura, A.B., Loconte, T., Ahmed, A. et al. SPINK2 silencing suppresses leukemic proliferation and restores myeloid commitment via MECOM downregulation in acute myeloid leukaemia. Cell Death Discov. 12, 135 (2026). https://doi.org/10.1038/s41420-026-02988-1
Nyckelord: akut myeloisk leukemi, SPINK2, leukemistamceller, MECOM, myeloid differentiering