Clear Sky Science · ru
Подавление SPINK2 тормозит пролиферацию лейкемии и восстанавливает миелоидную дифференцировку через понижение MECOM при остром миелобластном лейкозе
Почему это важно для рака крови
Острый миелоидный лейкоз (ОМЛ) — быстро прогрессирующее заболевание крови, при котором незрелые лейкоциты захватывают костный мозг, вытесняя нормальное кроветворение. Многие пациенты, особенно те, чьи лейкозные клетки несут многочисленные хромосомные нарушения (так называемые комплексные кариотипы), плохо реагируют на существующие препараты. В этом исследовании выявлена молекула SPINK2 как ключевой помощник, позволяющий лейкозным клеткам продолжать деление и одновременно препятствующий их созреванию в нормальные зрелые клетки крови. Поскольку SPINK2 можно экспериментально выключать, она может представлять новый путь для замедления болезни и направления раковых клеток в более здоровое состояние.
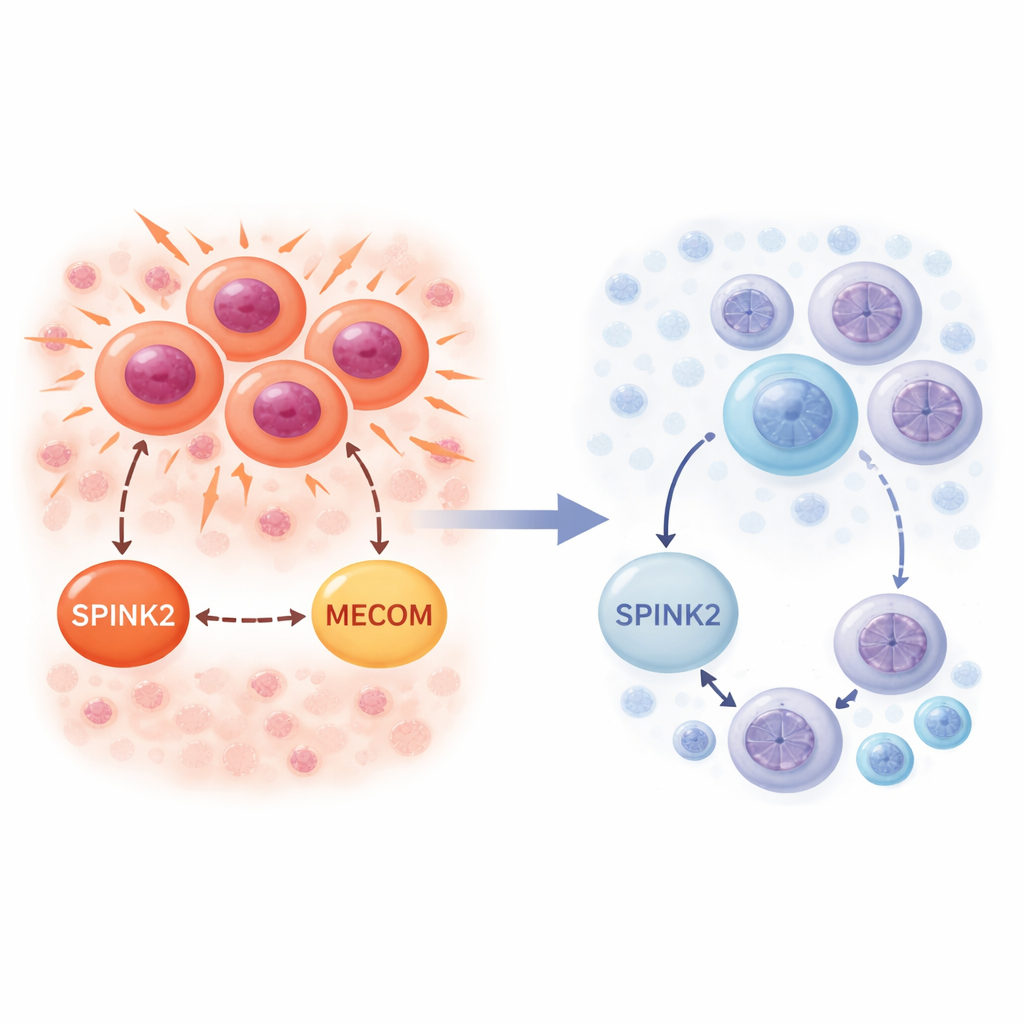
Выключатель, обнаруженный в ранних кроветворных клетках
Исследователи сначала выяснили, где SPINK2 обычно экспрессируется в здоровом костном мозге. Используя данные одноклеточного РНК‑секвенирования, которые измеряют активность генов по отдельности в каждой клетке, они обнаружили, что SPINK2 преимущественно включен в самых примитивных стволовых и прогениторных клетках крови, отмеченных CD34. Это покоящиеся, медленно циркулирующие клетки, находящиеся на вершине иерархии кроветворения. По мере созревания клеток по миелоидному или лимфоидному направлению активность SPINK2 резко снижается и практически отсутствует в полностью дифференцированных кровяных клетках. Такая картина указывает на то, что SPINK2 входит в программу, определяющую ранние стволоподобные клетки, и обычно выключается, когда клетки принимают конкретную специализированную роль.
Когда тот же выключатель питает рост лейкемии
Далее команда проанализировала SPINK2 в лейкемическом костном мозге пациентов с ОМЛ. Снова используя одноклеточные данные, они обнаружили активность SPINK2 в лейкемических клетках, наиболее похожих на стволовые, а также в быстро делящихся бластах ОМЛ. В отличие от здорового состояния, здесь SPINK2 шло в ногу с сильными сигналами от генов клеточного цикла, особенно тех, что управляют фазой S — репликацией ДНК. В кумулятивных наборах данных пациентов из крупных проектов геномики рака более высокие уровни SPINK2 ассоциировались с худшей выживаемостью и были особенно повышены у людей с ОМЛ и комплексным кариотипом. В совокупности эти наблюдения указывают на то, что лейкемические клетки присвоили ген, характерный для стволовых клеток, используя SPINK2 для поддержания неуклонного деления и одновременно сохранения примитивной идентичности.
Выключение SPINK2 замедляет рак и побуждает его созревать
Чтобы проверить, является ли SPINK2 просто маркером или настоящим драйвером, учёные создали линию клеток ОМЛ FUJIOKA — модель комплексного кариотипа — с доксициклин‑индуцируемой короткой шпилевой РНК, выборочно подавляющей SPINK2. При выключении SPINK2 лейкемические клетки делились значительно медленнее. Детальный анализ клеточного цикла показал, что многие клетки застревали в фазе G0/G1 и не проходили через S и G2/M, без заметного увеличения гибели клеток. Одновременно клетки стали проявлять более высокие уровни поверхностных маркеров, типичных для зрелых миелоидных клеток, что указывает на ослабление обычной блокировки развития. Иными словами, потеря SPINK2 одновременно убирала стимул к росту и снимала тормоз дифференцировки.
Молекулярная связь с другим драйвером лейкемии
РНК‑секвенирование клеток FUJIOKA до и после подавления SPINK2 показало широкие изменения в активности генов. Сотни генов, контролирующих клеточный цикл, сегрегацию хромосом и митотические контрольные точки, были снижены, в то время как наборы, связанные с синтезом белка и иммунными ответами, были повышены. Одним из заметных оказался MECOM — известный транскрипционный фактор, способствующий лейкемии, который поддерживает самовоспроизведение стволоподобных клеток и препятствует миелоидному созреванию. Экспрессия MECOM резко падала при подавлении SPINK2. Анализы большого педиатрического набора данных по ОМЛ подтвердили, что уровни SPINK2 и MECOM склонны колебаться синхронно, особенно у пациентов с комплексным кариотипом. Это указывает на ось SPINK2–MECOM, которая может координировать избыточное самовоспроизведение и деление в ОМЛ высокого риска.
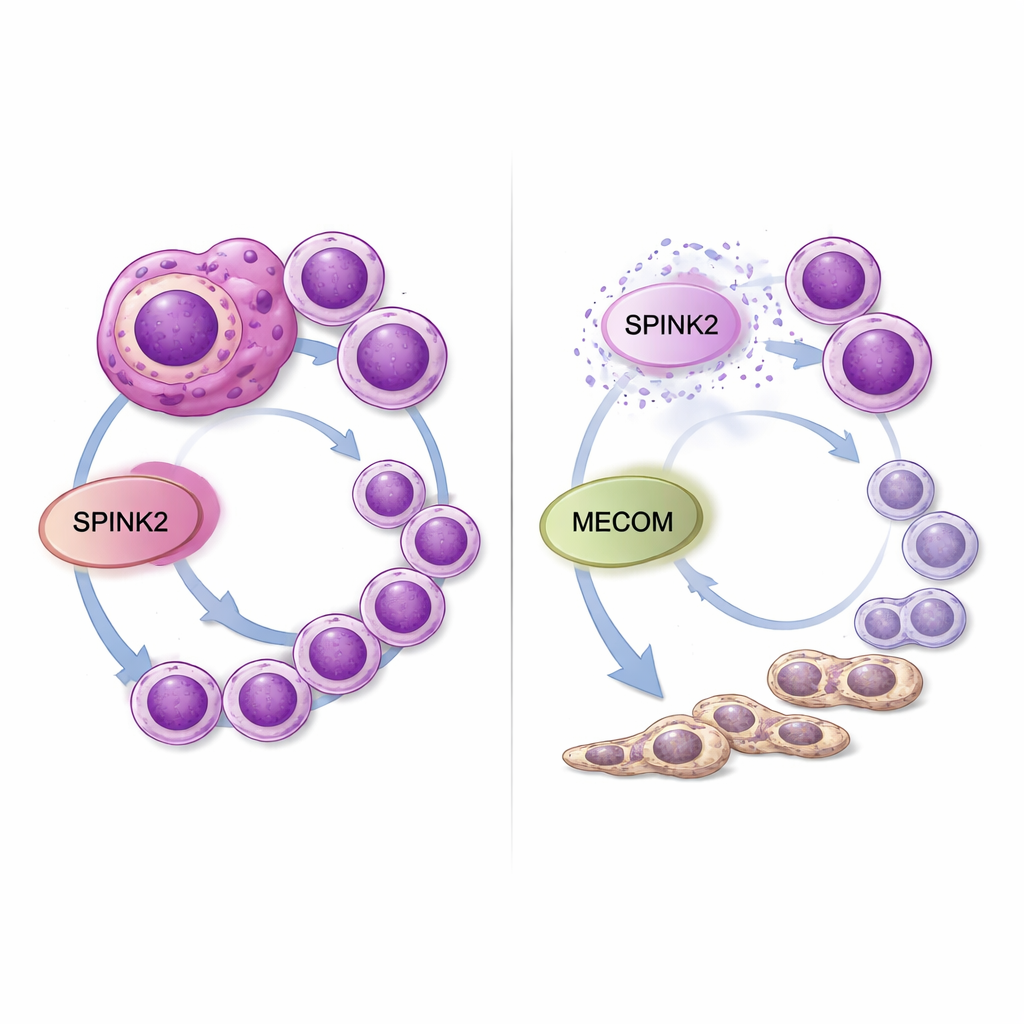
Что это значит для будущих терапий
Для непрофессионала эти результаты предлагают представление о том, что SPINK2 действует подобно скрытой ручке в лейкемических клетках, повернутой слишком сильно: она удерживает клетки в юном, стволоподобном состоянии и стимулирует их неконтролируемое размножение. Понижение активности SPINK2 в лаборатории и замедляет рост раковых клеток, и побуждает их дифференцироваться в более нормальные миелоидные клетки, а также снижает активность ещё одного опасного гена — MECOM. Поскольку SPINK2 в норме ограничена ранними кроветворными стволовыми клетками и в основном неактивна в большинстве взрослых тканей, препараты, нацеленные на эту молекулу или на её взаимодействие с MECOM, могут селективно ослаблять агрессивный ОМЛ — особенно случаи с комплексным кариотипом — без сильного ущерба для нормального кроветворения. Потребуются дополнительные исследования на животных моделях и усилия по разработке препаратов, но это исследование выделяет SPINK2 как перспективную уязвимость в форме лейкемии, которая остро нуждается в лучших вариантах лечения.
Цитирование: Ventura, A.B., Loconte, T., Ahmed, A. et al. SPINK2 silencing suppresses leukemic proliferation and restores myeloid commitment via MECOM downregulation in acute myeloid leukaemia. Cell Death Discov. 12, 135 (2026). https://doi.org/10.1038/s41420-026-02988-1
Ключевые слова: острый миелоидный лейкоз, SPINK2, стеблевые клетки лейкемии, MECOM, миелоидная дифференцировка