Clear Sky Science · pt
Silenciamento de SPINK2 suprime a proliferação leucêmica e restaura o comprometimento mieloide via desregulação de MECOM na leucemia mieloide aguda
Por que isso importa para o câncer do sangue
A leucemia mieloide aguda (LMA) é um câncer sanguíneo de evolução rápida no qual glóbulos brancos imaturos dominam a medula óssea, sufocando a produção normal de sangue. Muitos pacientes, especialmente aqueles cujas células leucêmicas apresentam numerosas anomalias cromossômicas (os chamados cariótipos complexos), respondem mal às terapias atuais. Este estudo revela uma molécula chamada SPINK2 como um auxiliar chave que permite às células leucêmicas continuar se dividindo enquanto se recusam a amadurecer em células sanguíneas normais e maduras. Como o SPINK2 pode ser desligado experimentalmente, ele pode oferecer uma nova maneira de desacelerar a doença e empurrar as células cancerosas de volta para um destino mais saudável.
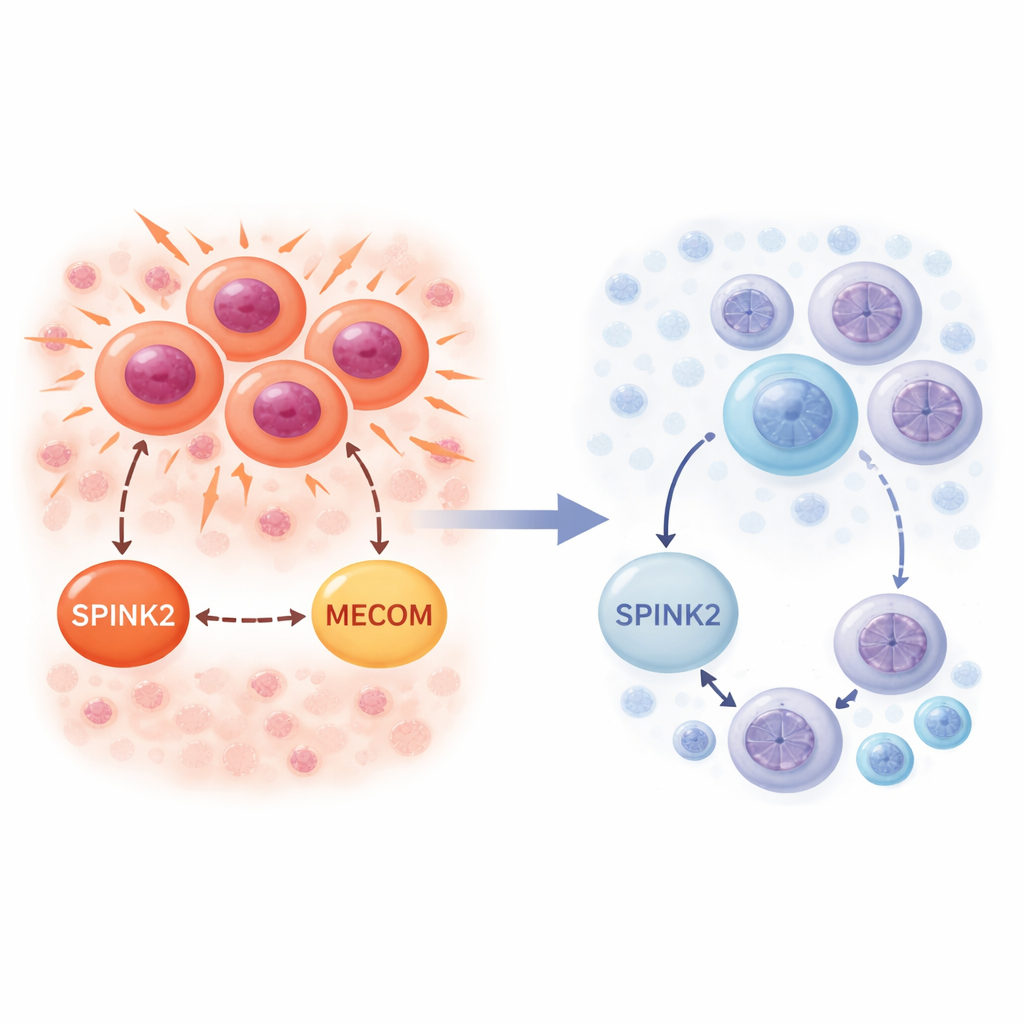
Um interruptor encontrado em células-tronco sanguíneas precoces
Os pesquisadores primeiro investigaram onde o SPINK2 aparece normalmente na medula óssea saudável. Usando dados de RNA de célula única, que medem a atividade gênica célula a célula, descobriram que o SPINK2 é principalmente ativado nas células-tronco e progenitoras sanguíneas mais primitivas marcadas por CD34. São células quiescentes, de ciclo lento, que ficam no topo da árvore genealógica das células sanguíneas. À medida que as células amadurecem ao longo das vias mieloide ou linfoide, a atividade de SPINK2 cai acentuadamente e é essencialmente ausente em células sanguíneas totalmente desenvolvidas. Esse padrão sugere que o SPINK2 faz parte do programa que define células muito precoces com características de tronco e normalmente é desligado assim que as células se comprometem com uma função específica.
Quando o mesmo interruptor alimenta o crescimento da leucemia
A equipe então examinou o SPINK2 na medula óssea leucêmica de pacientes com LMA. Novamente, usando dados de célula única, encontraram SPINK2 ativo em células leucêmicas que mais se assemelham a células-tronco, bem como em blastos de LMA que se dividem rapidamente. Em contraste com o cenário saudável, aqui o SPINK2 veio acompanhado de sinais fortes de genes do ciclo celular, especialmente os que impulsionam a fase S de cópia do DNA. Em coortes em larga escala de pacientes de grandes projetos de genômica do câncer, níveis mais altos de SPINK2 associaram-se a pior sobrevida e estavam particularmente elevados em pessoas com LMA de cariótipo complexo. Em conjunto, essas observações indicam que as células leucêmicas sequestraram um gene de célula-tronco, usando SPINK2 para sustentar uma divisão implacável enquanto preservam uma identidade primitiva.
Desligar o SPINK2 desacelera o câncer e o empurra a maturar
Para testar se o SPINK2 é apenas um marcador ou um verdadeiro motor da doença, os cientistas modificaram uma linhagem celular de LMA chamada FUJIOKA—representando doença de cariótipo complexo—para carregar um RNA de cabelo curto induzível por doxiciclina que silencia seletivamente o SPINK2. Quando o SPINK2 foi desligado, as células leucêmicas se dividiram muito mais devagar. Análises detalhadas do ciclo celular mostraram que muitas células ficaram presas na fase G0/G1 e não progrediram pelas fases S e G2/M, sem aumento notável da morte celular. Ao mesmo tempo, as células passaram a exibir níveis mais altos de marcadores de superfície típicos de células mieloides maduras, indicando que o bloqueio de desenvolvimento habitual estava se aliviando. Em outras palavras, a perda de SPINK2 tanto removeu o impulso de crescimento quanto liberou o freio da diferenciação.
Uma ligação molecular a outro impulsionador da leucemia
O sequenciamento de RNA das células FUJIOKA antes e depois do silenciamento de SPINK2 revelou mudanças amplas na atividade gênica. Centenas de genes que controlam o ciclo celular, a segregação cromossômica e os pontos de checagem mitóticos foram reduzidos, enquanto conjuntos ligados à síntese de proteínas e respostas imunes aumentaram. Um destaque foi MECOM, um fator de transcrição conhecido por promover a leucemia, que ajuda células com características de tronco a se auto-renovarem e impede a maturação mieloide. A expressão de MECOM caiu acentuadamente quando SPINK2 foi silenciado. Análises de um grande conjunto de dados pediátricos de LMA confirmaram que os níveis de SPINK2 e MECOM tendem a subir e cair em conjunto especificamente em pacientes com cariótipo complexo. Isso aponta para um eixo SPINK2–MECOM que pode coordenar a auto-renovação e a divisão excessivas na LMA de alto risco.
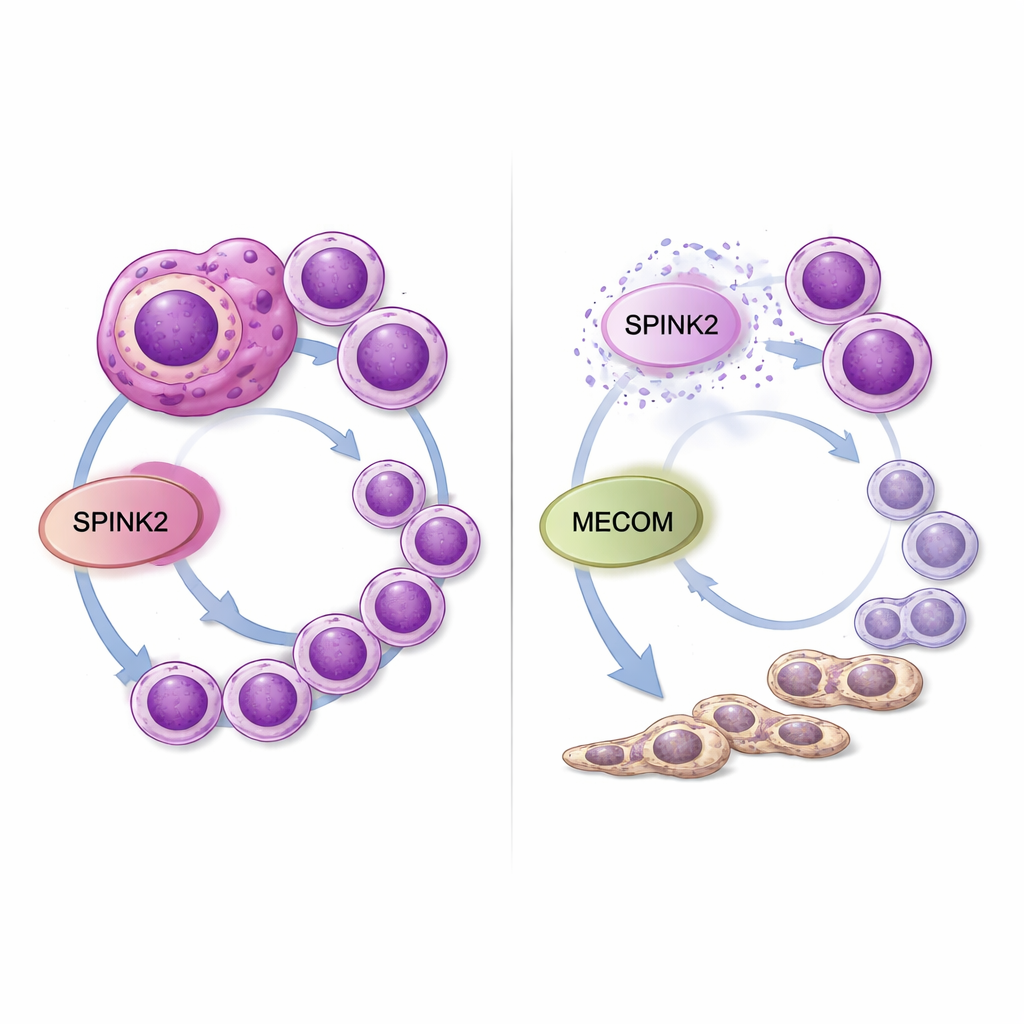
O que isso significa para tratamentos futuros
Para um observador leigo, esses achados sugerem que SPINK2 age como um botão oculto nas células leucêmicas que está regulado alto demais: ele mantém as células em um estado jovem, semelhante a tronco, e as estimula a se multiplicar descontroladamente. Reduzir o SPINK2 no laboratório tanto desacelera as células cancerosas quanto as incentiva a se transformarem em células mieloides mais normais, ao mesmo tempo em que reduz a atividade de outro gene perigoso, MECOM. Como o SPINK2 é normalmente restrito a células-tronco sanguíneas precoces e amplamente silenciado na maioria dos tecidos adultos, fármacos que atinjam essa molécula ou sua parceria com MECOM podem enfraquecer seletivamente a LMA agressiva—especialmente os casos de cariótipo complexo—sem prejudicar severamente a produção sanguínea normal. Serão necessários estudos adicionais em modelos animais e esforços de desenvolvimento de fármacos, mas este estudo aponta o SPINK2 como uma nova vulnerabilidade promissora em uma forma de leucemia que precisa urgentemente de melhores opções.
Citação: Ventura, A.B., Loconte, T., Ahmed, A. et al. SPINK2 silencing suppresses leukemic proliferation and restores myeloid commitment via MECOM downregulation in acute myeloid leukaemia. Cell Death Discov. 12, 135 (2026). https://doi.org/10.1038/s41420-026-02988-1
Palavras-chave: leucemia mieloide aguda, SPINK2, células-tronco leucêmicas, MECOM, diferenciação mieloide