Clear Sky Science · fr
La silenciation de SPINK2 supprime la prolifération leucémique et restaure l’engagement myéloïde via la régulation à la baisse de MECOM dans la leucémie myéloïde aiguë
Pourquoi c’est important pour les cancers du sang
La leucémie myéloïde aiguë (LMA) est un cancer du sang à évolution rapide dans lequel des globules blancs immatures envahissent la moelle osseuse, étouffant la production normale de cellules sanguines. De nombreux patients, en particulier ceux dont les cellules leucémiques présentent de nombreuses anomalies chromosomiques (les « karyotypes complexes »), répondent mal aux traitements actuels. Cette étude met en évidence une molécule, SPINK2, comme un auxiliaire clé qui permet aux cellules leucémiques de continuer à se diviser tout en refusant de mûrir en cellules sanguines normales. Parce que SPINK2 peut être expérimentellement désactivée, elle offre potentiellement un nouveau moyen de ralentir la maladie et de pousser les cellules cancéreuses vers un devenir plus sain.
Un interrupteur retrouvé dans les premières cellules souches sanguines
Les chercheurs ont d’abord cherché où SPINK2 s’exprime normalement dans la moelle osseuse saine. En utilisant des données de séquençage d’ARN unicellulaire, qui mesurent l’activité génique cellule par cellule, ils ont trouvé que SPINK2 est principalement activée dans les cellules souches et progénitrices sanguines les plus primitives marquées par CD34. Il s’agit de cellules quiescentes, à faible fréquence de division, situées au sommet de l’arbre de développement des cellules sanguines. À mesure que les cellules mûrissent selon les voies myéloïde ou lymphoïde, l’activité de SPINK2 chute fortement et est essentiellement absente dans les cellules sanguines complètement différenciées. Ce profil suggère que SPINK2 fait partie du programme définissant les cellules très précoces de type souche et est normalement éteinte une fois que les cellules s’engagent dans une fonction spécifique.
Quand le même interrupteur alimente la croissance leucémique
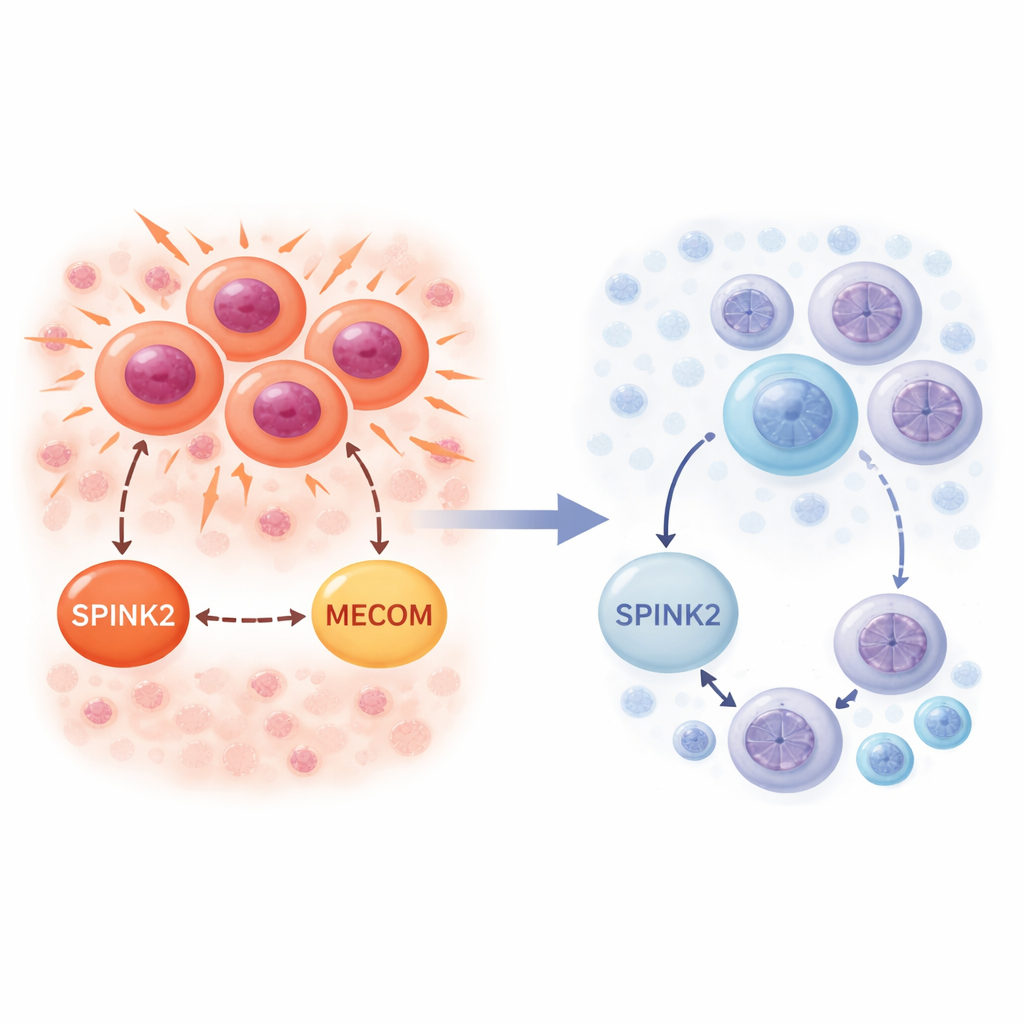
L’équipe a ensuite examiné SPINK2 dans la moelle leucémique de patients atteints de LMA. Là encore, à partir de données unicellulaires, SPINK2 s’est révélée active dans les cellules leucémiques qui ressemblent le plus à des cellules souches, ainsi que dans les blastes de LMA à division rapide. Contrairement au contexte sain, ici SPINK2 coïncidait avec de forts signaux provenant de gènes du cycle cellulaire, en particulier ceux qui pilotent la phase S de réplication de l’ADN. Dans des cohortes groupées de patients issues de grands projets de génomique du cancer, des niveaux plus élevés de SPINK2 étaient associés à une survie plus mauvaise et étaient particulièrement élevés chez les personnes ayant une LMA à karyotype complexe. Ensemble, ces observations indiquent que les cellules leucémiques ont détourné un gène propre aux cellules souches, utilisant SPINK2 pour soutenir une division implacable tout en préservant une identité primitive.
Désactiver SPINK2 freine le cancer et favorise la maturation
Pour déterminer si SPINK2 est seulement un marqueur ou un véritable moteur, les scientifiques ont modifié une lignée cellulaire de LMA appelée FUJIOKA—représentant la maladie à karyotype complexe—pour porter un ARN court en épingle inductible par la doxycycline ciblant spécifiquement SPINK2. Lorsque SPINK2 a été éteinte, les cellules leucémiques se sont divisées beaucoup plus lentement. Une analyse détaillée du cycle cellulaire a montré que de nombreuses cellules restaient bloquées en phase G0/G1 et n’avançaient pas en S et G2/M, sans augmentation notable de la mort cellulaire. Dans le même temps, les cellules ont commencé à exprimer des niveaux plus élevés de marqueurs de surface typiques des cellules myéloïdes matures, indiquant que le blocage habituel du développement s’atténuait. En d’autres termes, la perte de SPINK2 supprimait à la fois la poussée proliférative et relâchait le frein sur la différenciation.
Un lien moléculaire avec un autre moteur de la leucémie
Le séquençage de l’ARN des cellules FUJIOKA avant et après la silenciation de SPINK2 a révélé des changements étendus de l’activité génique. Des centaines de gènes contrôlant le cycle cellulaire, la ségrégation des chromosomes et les points de contrôle mitotiques ont été réprimés, tandis que des ensembles liés à la synthèse protéique et aux réponses immunitaires ont été activés. Un élément remarquable était MECOM, un facteur de transcription bien connu favorisant la leucémie qui aide les cellules de type souche à s’auto-renouveler et empêche la maturation myéloïde. L’expression de MECOM a chuté fortement lorsque SPINK2 a été silencée. Des analyses d’un large jeu de données pédiatriques de LMA ont confirmé que les niveaux de SPINK2 et de MECOM tendent à augmenter et diminuer de concert, spécifiquement chez les patients à karyotype complexe. Cela suggère un axe SPINK2–MECOM qui pourrait coordonner l’auto-renouvellement excessif et la division dans les LMA à haut risque.
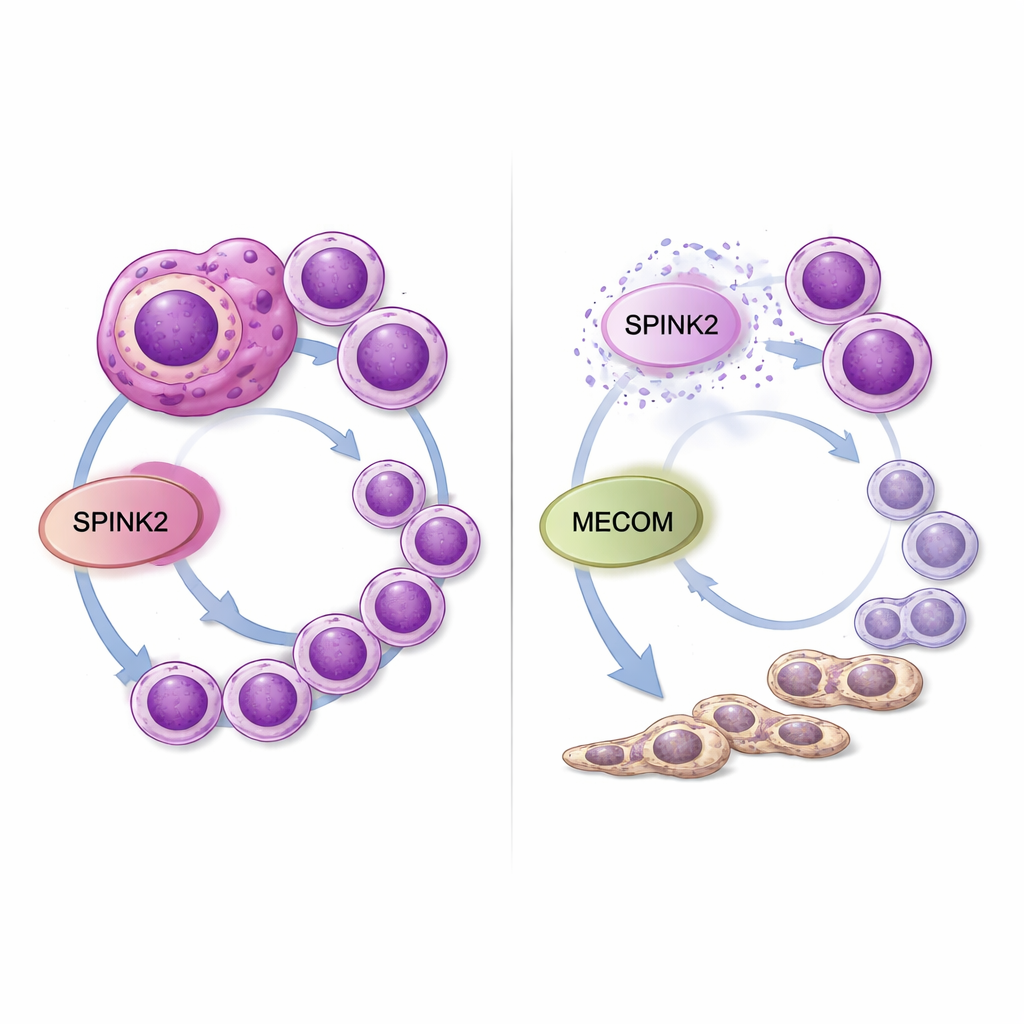
Ce que cela signifie pour les traitements futurs
Pour un lecteur non spécialiste, ces résultats suggèrent que SPINK2 fonctionne comme un réglage caché dans les cellules leucémiques, trop activé : il maintient les cellules dans un état juvénile de type souche et les incite à se multiplier de manière incontrôlée. Abaisser SPINK2 en laboratoire ralentit les cellules cancéreuses et les encourage à évoluer en cellules myéloïdes plus normales, tout en réduisant l’activité d’un autre gène dangereux, MECOM. Parce que SPINK2 est normalement limitée aux premières cellules souches sanguines et largement silencieuse dans la plupart des tissus adultes, des médicaments ciblant cette molécule ou son interaction avec MECOM pourraient affaiblir sélectivement les LMA agressives—en particulier les cas à karyotype complexe—sans nuire gravement à la production sanguine normale. Des travaux supplémentaires sur des modèles animaux et des efforts de développement de médicaments seront nécessaires, mais cette étude désigne SPINK2 comme une vulnérabilité prometteuse dans une forme de leucémie qui manque cruellement de meilleures options.
Citation: Ventura, A.B., Loconte, T., Ahmed, A. et al. SPINK2 silencing suppresses leukemic proliferation and restores myeloid commitment via MECOM downregulation in acute myeloid leukaemia. Cell Death Discov. 12, 135 (2026). https://doi.org/10.1038/s41420-026-02988-1
Mots-clés: leucémie myéloïde aiguë, SPINK2, cellules souches leucémiques, MECOM, différenciation myéloïde