Clear Sky Science · it
La silenziamento di SPINK2 sopprime la proliferazione leucemica e ripristina l’impegno mieloide tramite la downregulation di MECOM nella leucemia mieloide acuta
Perché questo è importante per le malattie del sangue
La leucemia mieloide acuta (LMA) è un tumore ematologico rapido in cui cellule bianche immature invadono il midollo osseo, soffocando la produzione di sangue normale. Molti pazienti, in particolare quelli le cui cellule leucemiche mostrano numerose anomalie cromosomiche (i cosiddetti cariotipi complessi), rispondono male alle terapie attuali. Questo studio individua una molecola chiamata SPINK2 come un fattore chiave che permette alle cellule leucemiche di continuare a dividersi evitando di maturare in cellule del sangue normali. Poiché SPINK2 può essere sperimentalmente inattivata, potrebbe offrire un nuovo modo per rallentare la malattia e spingere le cellule tumorali verso un destino più sano.
Un interruttore trovato nelle cellule staminali ematopoietiche precoci
I ricercatori hanno innanzitutto verificato dove SPINK2 è normalmente espresso nel midollo osseo sano. Utilizzando dati di single‑cell RNA sequencing, che misurano l’attività genica cellula per cellula, hanno scoperto che SPINK2 è acceso principalmente nelle cellule staminali e progenitrici del sangue più primitive, contrassegnate da CD34. Si tratta di cellule quiescenti, a bassa proliferazione, che si trovano al vertice dell’albero genealogico delle cellule del sangue. Man mano che le cellule maturano lungo le vie mieloide o linfoide, l’espressione di SPINK2 cala bruscamente ed è praticamente assente nelle cellule completamente differenziate. Questo schema suggerisce che SPINK2 faccia parte del programma che definisce le cellule molto precoci simili a staminali ed è normalmente spento una volta che la cellula si impegna in una funzione specifica.
Quando lo stesso interruttore alimenta la crescita della leucemia
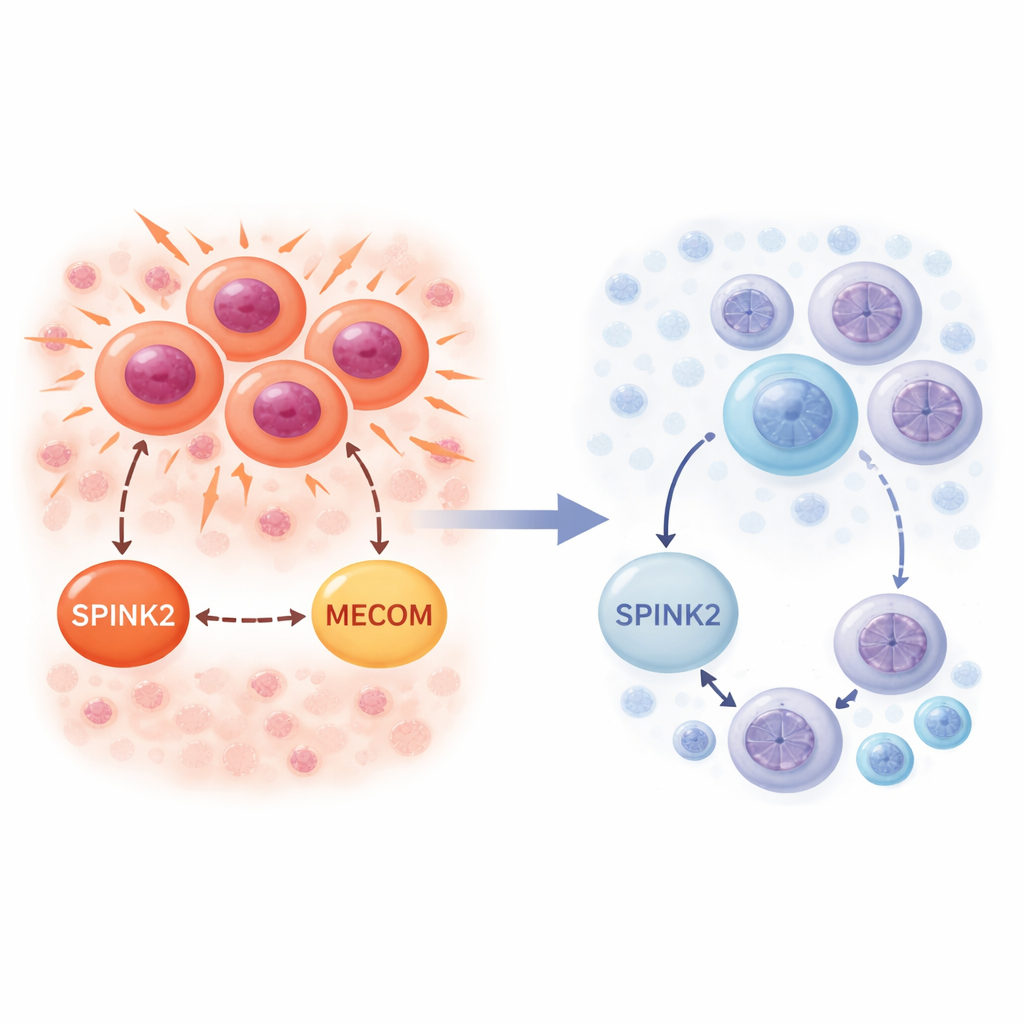
Il gruppo ha quindi esaminato SPINK2 nel midollo leucemico di pazienti con LMA. Sempre usando dati single‑cell, hanno trovato SPINK2 attivo nelle cellule leucemiche che più somigliano a cellule staminali, così come nei blasti AML a rapido ciclo. In contrasto con il tessuto sano, qui SPINK2 era associato a forti segnali dai geni del ciclo cellulare, in particolare quelli che guidano la fase S di replicazione del DNA. In coorti di pazienti analizzate in studi genomici oncologici su larga scala, livelli più alti di SPINK2 erano correlati a una sopravvivenza peggiore e risultavano particolarmente elevati nei soggetti con LMA a cariotipo complesso. Nel complesso, queste osservazioni indicano che le cellule leucemiche hanno "dirottato" un gene tipico delle staminali, usando SPINK2 per sostenere una divisione incessante pur mantenendo un’identità primitiva.
Spegnere SPINK2 rallenta il tumore e lo spinge a maturare
Per stabilire se SPINK2 sia solo un marcatore o un vero fattore causale, gli scienziati hanno ingegnerizzato una linea cellulare AML chiamata FUJIOKA—rappresentativa della malattia a cariotipo complesso—per esprimere un short hairpin RNA inducibile con doxiciclina che silenzia selettivamente SPINK2. Quando SPINK2 è stato spento, le cellule leucemiche si sono divise molto più lentamente. Un’analisi dettagliata del ciclo cellulare ha mostrato che molte cellule rimanevano bloccate nella fase G0/G1 e non riuscivano a progredire attraverso le fasi S e G2/M, senza un aumento significativo della morte cellulare. Contemporaneamente, le cellule hanno iniziato a mostrare livelli più alti di marcatori di superficie tipici delle cellule mieloidi mature, indicando che il blocco dello sviluppo si stava attenuando. In altre parole, la perdita di SPINK2 sia ha rimosso lo stimolo alla proliferazione sia ha allentato il freno sulla differenziazione.
Un collegamento molecolare a un altro promotore di leucemia
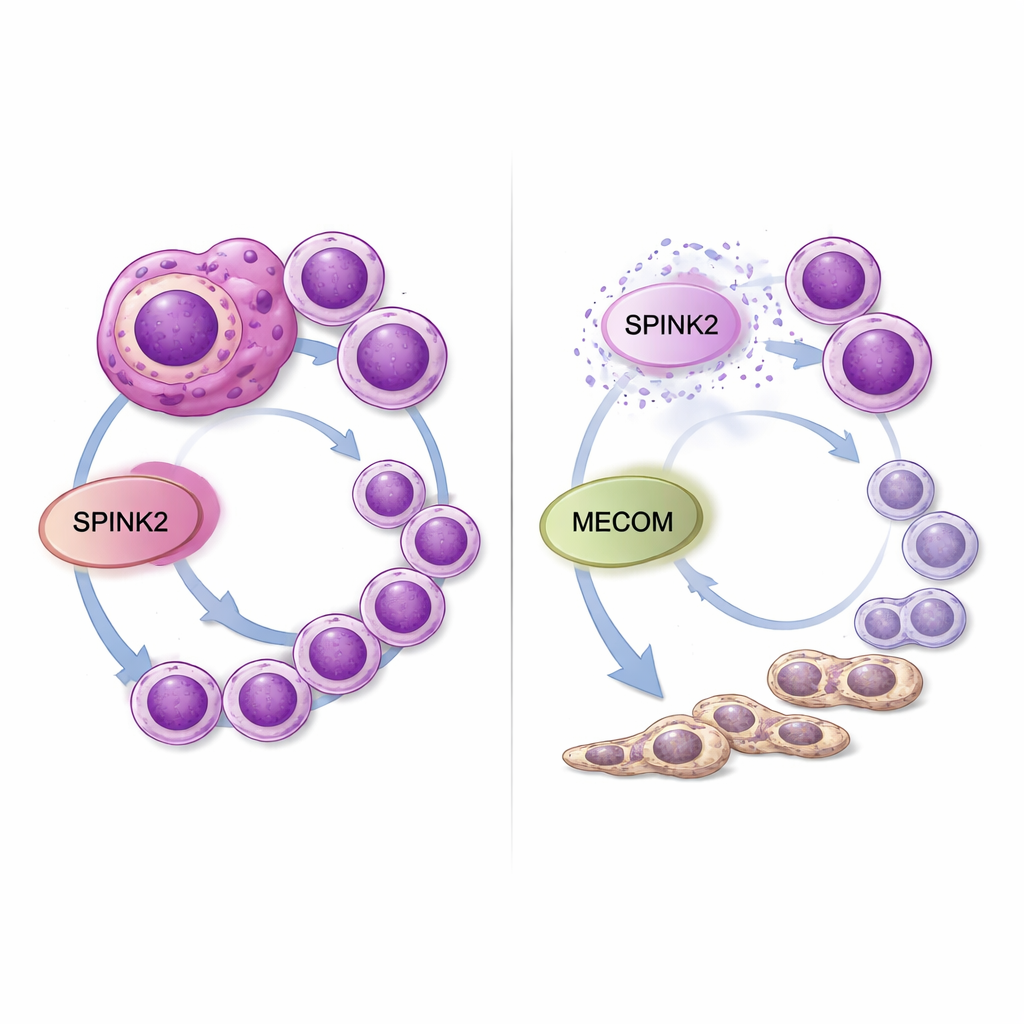
Il sequenziamento dell’RNA delle cellule FUJIOKA prima e dopo il silenziamento di SPINK2 ha rivelato ampi cambiamenti nell’attività genica. Centinaia di geni che controllano il ciclo cellulare, la segregazione dei cromosomi e i checkpoint mitotici sono stati downregolati, mentre sono stati upregolati set di geni legati alla sintesi proteica e alle risposte immunitarie. Una nota di rilievo è stata MECOM, un noto fattore di trascrizione promotore di leucemia che favorisce l’autorenovamento delle cellule simili a staminali e impedisce la maturazione mieloide. L’espressione di MECOM è diminuita nettamente quando SPINK2 è stata silenziata. Analisi su un ampio dataset pediatrico di LMA hanno confermato che i livelli di SPINK2 e MECOM tendono a salire e scendere insieme in modo specifico nei pazienti con cariotipi complessi. Ciò suggerisce un asse SPINK2–MECOM che potrebbe coordinare l’eccessivo autorinnovamento e la divisione nelle LMA ad alto rischio.
Implicazioni per i trattamenti futuri
Per un lettore non specialistico, questi risultati suggeriscono che SPINK2 funziona come una manopola nascosta nelle cellule leucemiche che è impostata troppo alta: mantiene le cellule in uno stato giovanile, simile alle staminali, e ne favorisce la moltiplicazione incontrollata. Ridurre SPINK2 in laboratorio rallenta le cellule tumorali e le incoraggia a differenziarsi in cellule mieloidi più normali, riducendo al contempo l’attività di un altro gene pericoloso, MECOM. Poiché SPINK2 è normalmente limitato alle prime cellule staminali ematopoietiche ed è per lo più silente nella maggior parte dei tessuti adulti, farmaci che prendano di mira questa molecola o la sua interazione con MECOM potrebbero indebolire selettivamente le LMA aggressive—in particolare i casi a cariotipo complesso—senza danneggiare gravemente la produzione ematica normale. Sono necessari ulteriori studi su modelli animali e sforzi di sviluppo farmacologico, ma questo lavoro individua SPINK2 come una vulnerabilità promettente in una forma di leucemia che necessita urgentemente di opzioni migliori.
Citazione: Ventura, A.B., Loconte, T., Ahmed, A. et al. SPINK2 silencing suppresses leukemic proliferation and restores myeloid commitment via MECOM downregulation in acute myeloid leukaemia. Cell Death Discov. 12, 135 (2026). https://doi.org/10.1038/s41420-026-02988-1
Parole chiave: leucemia mieloide acuta, SPINK2, cellule staminali leucemiche, MECOM, differenziazione mieloide