Clear Sky Science · de
SPINK2‑Stilllegung unterdrückt leukämisches Wachstum und stellt myeloide Verpflichtung über MECOM‑Herunterregulierung bei akuter myeloischer Leukämie wieder her
Warum das für Blutkrebs wichtig ist
Die akute myeloische Leukämie (AML) ist ein schnell fortschreitender Blutkrebs, bei dem unreife weiße Blutkörperchen das Knochenmark besetzen und die normale Blutbildung verdrängen. Viele Patientinnen und Patienten, besonders jene, deren Leukämiezellen zahlreiche chromosomale Veränderungen aufweisen (sogenannte komplexe Karyotypen), sprechen schlecht auf die verfügbaren Therapien an. In dieser Studie wird das Molekül SPINK2 als ein zentraler Helfer identifiziert, der es leukämischen Zellen ermöglicht, sich weiter zu teilen und gleichzeitig die Reifung zu normalen, funktionellen Blutzellen zu verweigern. Da SPINK2 experimentell ausgeschaltet werden kann, bietet es möglicherweise einen neuen Ansatz, das Fortschreiten der Krankheit zu verlangsamen und Krebszellen zu einem gesünderen Schicksal zurückzulenken.
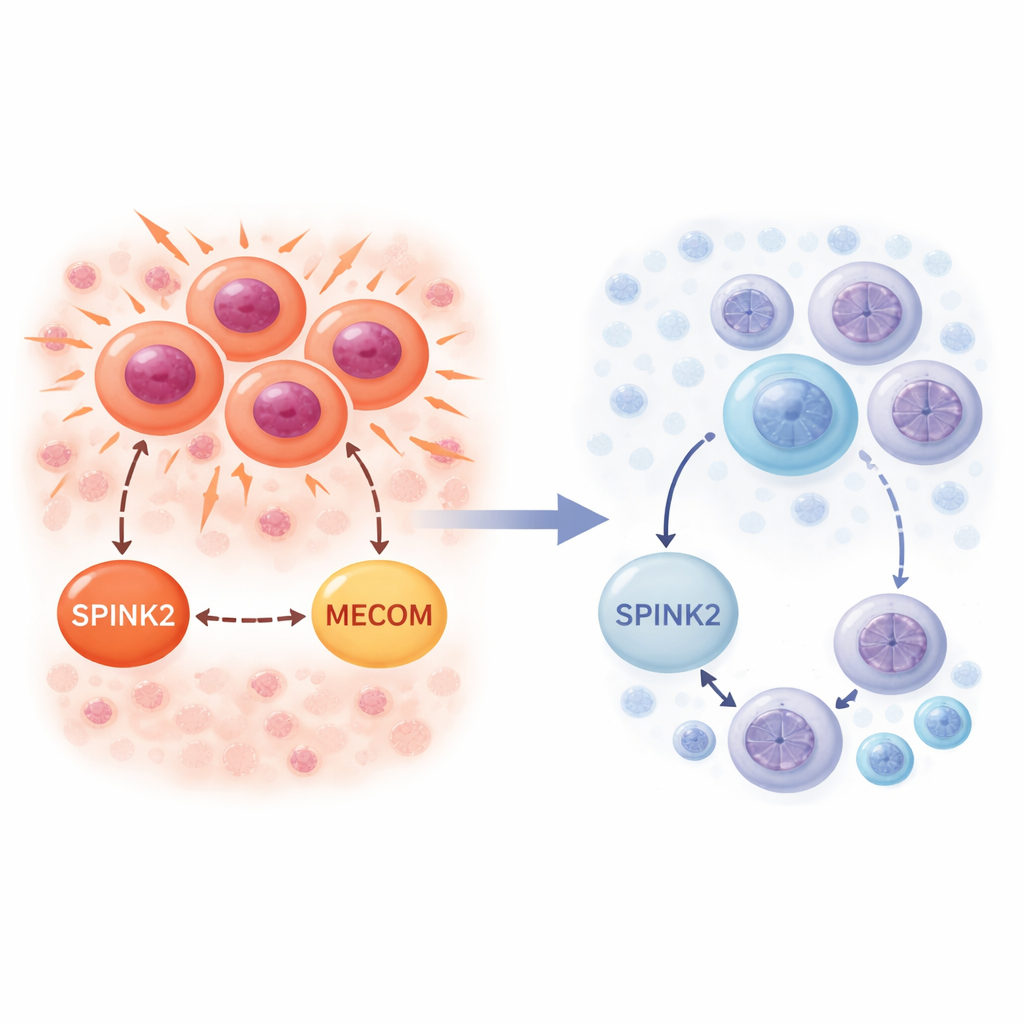
Ein Schalter, gefunden in frühen Blutstammzellen
Die Forschenden fragten zunächst, wo SPINK2 normalerweise im gesunden Knochenmark vorkommt. Mithilfe von Einzelzell‑RNA‑Sequenzierungsdaten, die Genaktivität auf Einzelzellebene messen, fanden sie, dass SPINK2 vor allem in den primitivsten Blutstamm‑ und Vorläuferzellen mit dem Marker CD34 eingeschaltet ist. Dies sind ruhende, langsam teilende Zellen, die an der Spitze des hämatopoetischen Stammbaums sitzen. Während der Reifung entlang der myeloiden oder lymphatischen Linie fällt die SPINK2‑Aktivität stark ab und ist in vollständig entwickelten Blutzellen praktisch nicht mehr vorhanden. Dieses Muster deutet darauf hin, dass SPINK2 Teil des Programms ist, das sehr frühe stammzellähnliche Zustände definiert und normalerweise ausgeschaltet wird, sobald Zellen sich zu einer bestimmten Funktion verpflichten.
Wenn derselbe Schalter das Leukämiewachstum antreibt
Das Team untersuchte anschließend SPINK2 im leukämischen Knochenmark von AML‑Patientinnen und ‑Patienten. Wieder mit Einzelzell‑Daten fanden sie SPINK2 aktiv in Leukämiezellen, die Stammzellen am ähnlichsten sind, sowie in schnell teilenden AML‑Blasten. Im Gegensatz zum gesunden Kontext ging hier SPINK2 mit starken Signalen aus Zellzyklusgenen einher, insbesondere solchen, die die DNA‑Replikation in der S‑Phase antreiben. In umfangreichen Patientenkohorten aus großen Krebs‑Genomikprojekten korrelierten höhere SPINK2‑Spiegel mit schlechterem Überleben und waren besonders in Fällen mit komplexem Karyotyp erhöht. Zusammengenommen deuten diese Beobachtungen darauf hin, dass Leukämiezellen ein Stammzellgen gekapert haben und SPINK2 nutzen, um unaufhörliche Teilung zu unterstützen und gleichzeitig eine primitive Identität zu bewahren.
SPINK2 auszuschalten verlangsamt den Krebs und fördert Reifung
Um zu prüfen, ob SPINK2 nur ein Marker oder ein treibender Faktor ist, konstruierten die Wissenschaftlerinnen und Wissenschaftler eine AML‑Zelllinie namens FUJIOKA—ein Modell für Erkrankungen mit komplexem Karyotyp—mit einer doxycyclininduzierbaren kurzen Haar‑RNA, die SPINK2 selektiv stilllegt. Sobald SPINK2 abgeschaltet wurde, teilten sich die Leukämiezellen deutlich langsamer. Detaillierte Analysen des Zellzyklus zeigten, dass viele Zellen im G0/G1‑Abschnitt stecken blieben und nicht durch S und G2/M vorrückten, ohne dass eine deutliche Zunahme des Zelltods beobachtet wurde. Gleichzeitig zeigten die Zellen erhöhte Oberflächenmarker, die typisch für reife myeloide Zellen sind, was darauf hindeutet, dass die übliche Entwicklungsblockade nachließ. Mit anderen Worten: Der Verlust von SPINK2 nahm sowohl den Wachstumsantrieb weg als auch die Bremse der Differenzierung heraus.
Eine molekulare Verbindung zu einem weiteren Leukämietreiber
RNA‑Sequenzierung von FUJIOKA‑Zellen vor und nach SPINK2‑Stilllegung offenbarte weitreichende Veränderungen der Genaktivität. Hunderte Gene, die den Zellzyklus, die Chromosomenaufteilung und mitotische Kontrollpunkte steuern, wurden herunterreguliert, während Genmengen, die mit Proteinsynthese und Immunantworten assoziiert sind, hochreguliert wurden. Auffällig war MECOM, ein bekannter leukämiefördernder Transkriptionsfaktor, der stammzellähnliche Selbsterneuerung unterstützt und die myeloide Reifung verhindert. Die MECOM‑Expression fiel stark ab, wenn SPINK2 stillgelegt wurde. Analysen eines großen pädiatrischen AML‑Datensatzes bestätigten, dass SPINK2‑ und MECOM‑Spiegel dazu tendieren, insbesondere bei Patientinnen und Patienten mit komplexen Karyotypen gemeinsam zu steigen und zu fallen. Das deutet auf eine SPINK2–MECOM‑Achse hin, die übermäßige Selbsterneuerung und Teilung in Hochrisiko‑AML koordinieren könnte.
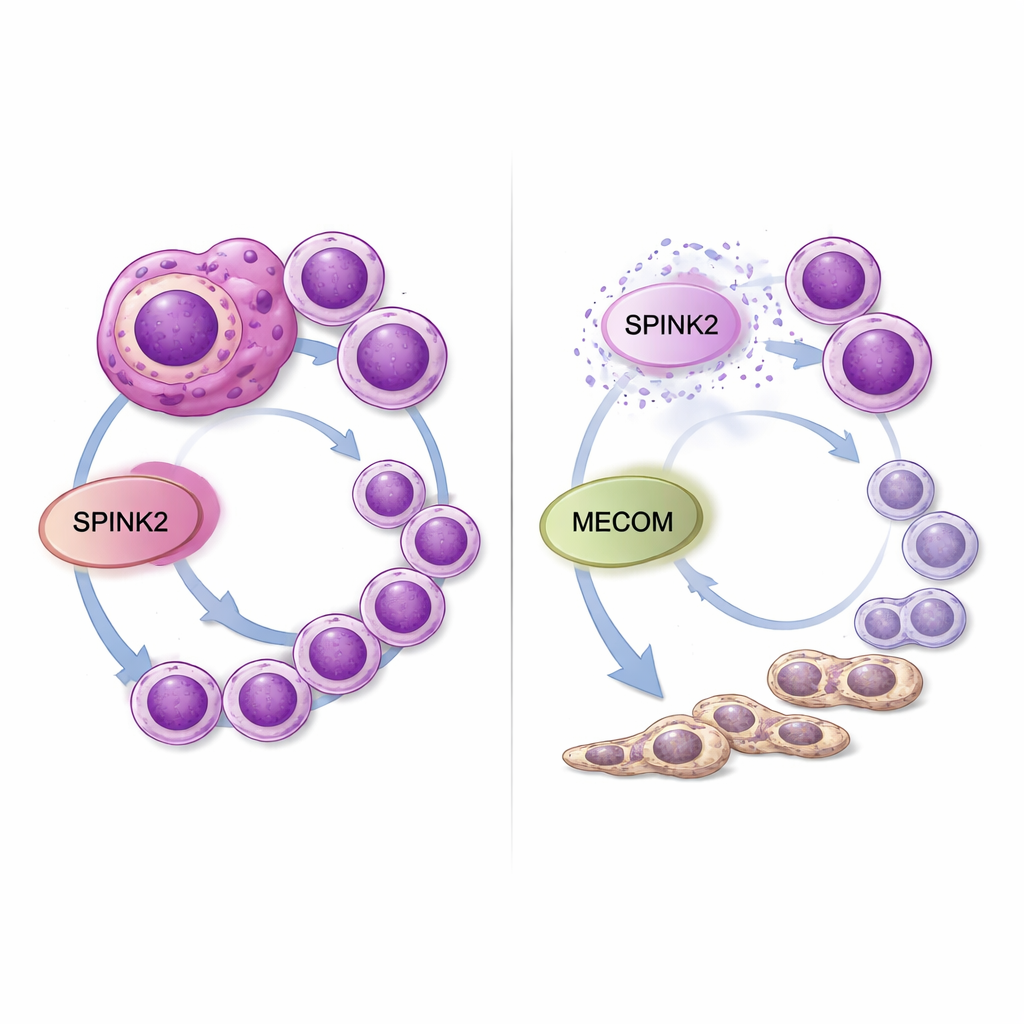
Was das für künftige Behandlungen bedeutet
Für eine nicht‑fachliche Leserschaft legen diese Befunde nahe, dass SPINK2 wie ein verstecktes Stellrad in Leukämiezellen wirkt, das zu hoch gedreht ist: Es hält die Zellen in einem jugendlichen, stammzellähnlichen Zustand und fördert ihre unkontrollierte Vermehrung. SPINK2 im Labor herunterzuregeln verlangsamt die Krebszellen und fördert gleichzeitig ihre Reifung zu normaleren myeloiden Zellen, während außerdem die Aktivität eines weiteren gefährlichen Gens, MECOM, reduziert wird. Da SPINK2 normalerweise auf frühe Blutstammzellen beschränkt ist und in den meisten erwachsenen Geweben weitgehend stillgelegt ist, könnten Wirkstoffe, die dieses Molekül oder seine Verbindung zu MECOM angreifen, aggressive AML—insbesondere Fälle mit komplexem Karyotyp—selektiv schwächen, ohne die normale Blutbildung stark zu schädigen. Weitere Arbeiten in Tiermodellen und Entwicklungen im Bereich Wirkstoffforschung sind erforderlich, doch diese Studie macht SPINK2 zu einer vielversprechenden neuen Verwundbarkeit einer Leukämieform, die dringend bessere Optionen braucht.
Zitation: Ventura, A.B., Loconte, T., Ahmed, A. et al. SPINK2 silencing suppresses leukemic proliferation and restores myeloid commitment via MECOM downregulation in acute myeloid leukaemia. Cell Death Discov. 12, 135 (2026). https://doi.org/10.1038/s41420-026-02988-1
Schlüsselwörter: akute myeloische Leukämie, SPINK2, Leukämie‑Stammzellen, MECOM, myeloide Differenzierung