Clear Sky Science · nl
Het tot zwijgen brengen van SPINK2 remt leukemische proliferatie en herstelt myeloïde toewijding via downregulatie van MECOM bij acute myeloïde leukemie
Waarom dit belangrijk is voor bloedkanker
Acute myeloïde leukemie (AML) is een snel voortschrijdende bloedkanker waarbij onrijpe witte bloedcellen het beenmerg overnemen en de normale bloedvorming verdringen. Veel patiënten, vooral wie leukemiecellen met talrijke chromosomale afwijkingen hebben (zogeheten complexe karyotypen), reageren slecht op de huidige geneesmiddelen. Deze studie identificeert een molecuul genaamd SPINK2 als een belangrijke helper die leukemische cellen in staat stelt door te blijven delen terwijl ze weigeren zich te ontwikkelen tot normale, rijpe bloedcellen. Omdat SPINK2 experimenteel kan worden uitgeschakeld, biedt het mogelijk een nieuwe manier om de ziekte te vertragen en kankercellen terug te duwen naar een gezondere ontwikkeling.
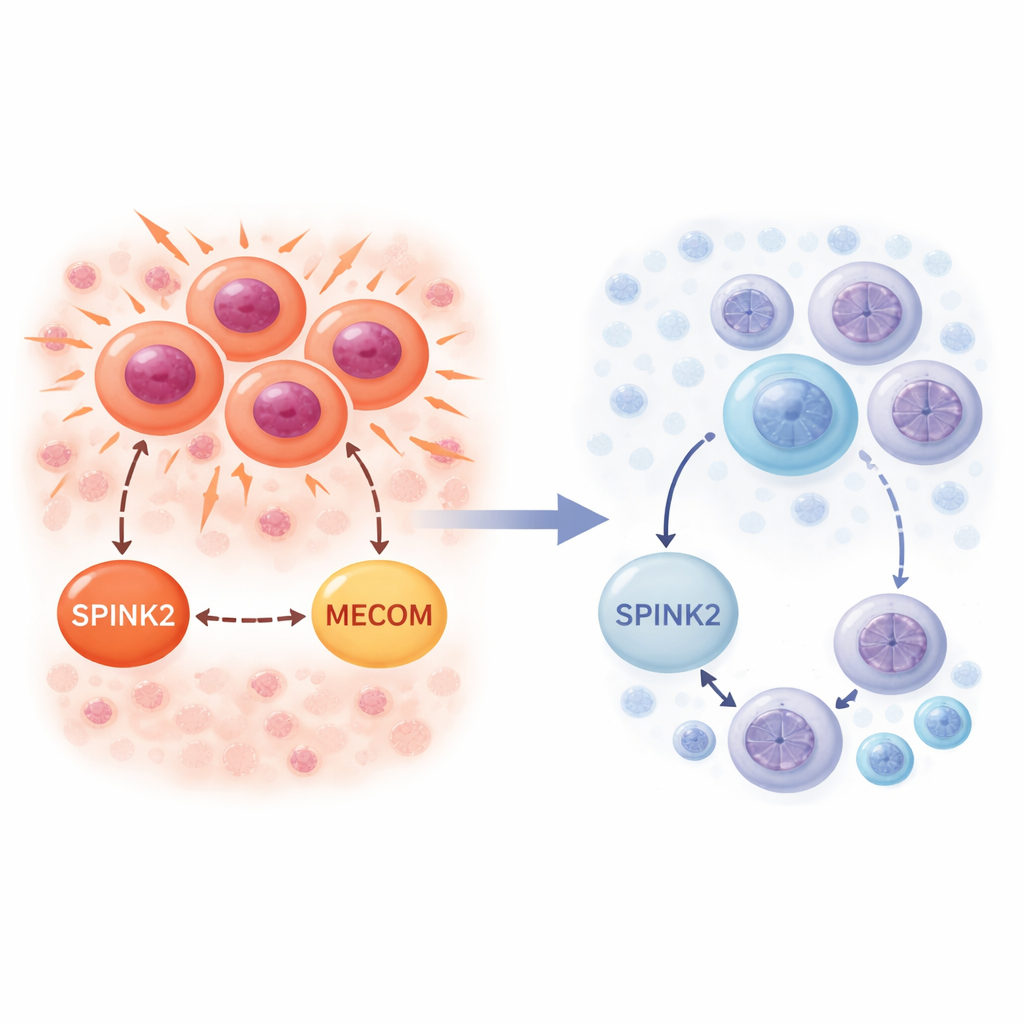
Een schakel gevonden in vroege bloedstamcellen
De onderzoekers vroegen zich eerst af waar SPINK2 normaal gesproken tot expressie komt in gezond beenmerg. Met single‑cell RNA‑sequencinggegevens, die genactiviteit per cel meten, vonden ze dat SPINK2 vooral is ingeschakeld in de meest primitieve bloedstam‑ en voorlopercellen die CD34 tot expressie brengen. Dit zijn quiescente, langzaam delende cellen die aan de top van de bloedcelstamboom staan. Naarmate cellen rijpen langs de myeloïde of lymfoïde trajecten, daalt de SPINK2‑activiteit scherp en is deze in volledig ontwikkelde bloedcellen nagenoeg afwezig. Dit patroon suggereert dat SPINK2 deel uitmaakt van het programma dat zeer vroege stamcelachtige eigenschappen definieert en normaal gesproken wordt uitgeschakeld zodra cellen zich aan een specifieke taak toewijden.
Wanneer dezelfde schakel leukemiegroei voedt
Het team onderzocht vervolgens SPINK2 in leukemisch beenmerg van AML‑patiënten. Opnieuw met single‑cell data vonden ze SPINK2 actief in leukemiecellen die het meest op stamcellen lijken, evenals in snel delende AML‑blasten. In tegenstelling tot de gezonde situatie ging SPINK2 hier gepaard met sterke signalen van celcyclusgenen, met name diegenen die de S‑fase voor DNA‑replicatie aansturen. In bulkcohorten van grote kanker‑genoomprojecten werden hogere SPINK2‑niveaus in verband gebracht met slechtere overleving en waren ze bijzonder verhoogd bij mensen met complexe karyotype‑AML. Samen wijzen deze observaties erop dat leukemiecellen een stamcelgen hebben gekaapt en SPINK2 gebruiken om onophoudelijke deling te ondersteunen terwijl ze een primitieve identiteit behouden.
SPINK2 uitzetten vertraagt kanker en zet aan tot rijping
Om te testen of SPINK2 slechts een marker is of een werkelijke aandrijver, bouwden de onderzoekers een AML‑celijn genaamd FUJIOKA—die complexe karyotype‑ziekte representeert—met een doxycycline‑induceerbare short hairpin RNA die SPINK2 selectief zwijgt. Toen SPINK2 werd uitgeschakeld, deelden de leukemische cellen veel langzamer. Gedetailleerde analyse van de celcyclus toonde aan dat veel cellen vastliepen in de G0/G1‑fase en niet verder kwamen naar S en G2/M, zonder noemenswaardige toename van celdood. Tegelijkertijd begonnen de cellen hogere niveaus te vertonen van oppervlaktemarkers die typerend zijn voor rijpe myeloïde cellen, wat aangeeft dat de gebruikelijke ontwikkelingsblokkade afnam. Met andere woorden: verlies van SPINK2 nam zowel de groeistimulans weg als de rem op differentiatie.
Een moleculaire link naar een andere leukemieaandrijver
RNA‑sequencing van FUJIOKA‑cellen voor en na het zwijgen van SPINK2 toonde brede veranderingen in genactiviteit. Honderden genen die de celcyclus, chromatide‑segmentatie en mitotische controles regelen werden omlaag gereguleerd, terwijl sets die gekoppeld zijn aan eiwitsynthese en immuunreacties werden opgevoerd. Een opvallende was MECOM, een goed bekend transcriptiefactor die leukemie bevordert, stamcelachtige zelfvernieuwing helpt en myeloïde rijping tegengaat. MECOM‑expressie daalde sterk toen SPINK2 werd uitgeschakeld. Analyses van een grote pediatrische AML‑dataset bevestigden dat SPINK2‑ en MECOM‑niveaus de neiging hebben samen te stijgen en te dalen, specifiek bij patiënten met complexe karyotypen. Dit wijst op een SPINK2–MECOM‑as die mogelijk overmatige zelfvernieuwing en deling coördineert bij hoogrisico‑AML.
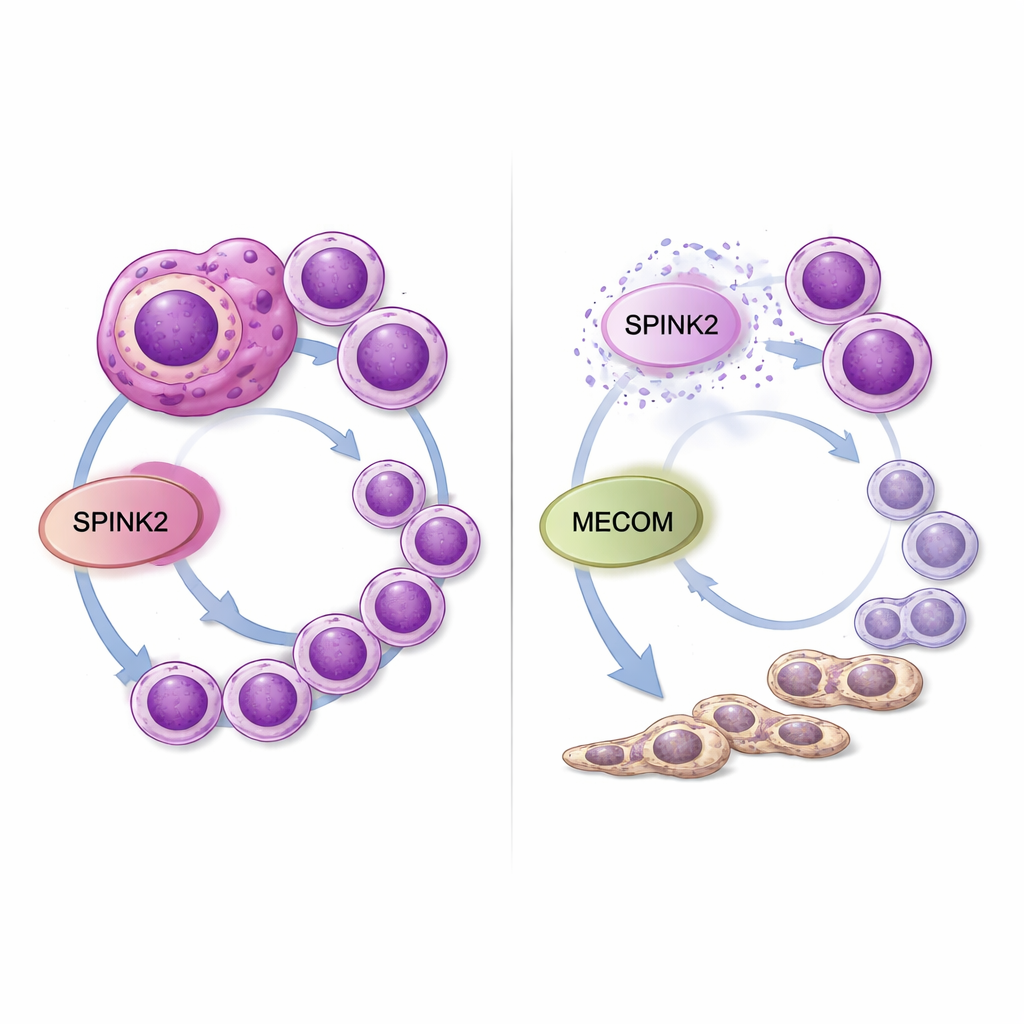
Wat dit betekent voor toekomstige behandelingen
Voor een leek suggereren deze bevindingen dat SPINK2 fungeert als een verborgen knop in leukemiecellen die te ver is opengedraaid: het houdt cellen in een jeugdige, stamcelachtige toestand en stimuleert hen om ongeremd te vermenigvuldigen. Het terugdraaien van SPINK2 in het laboratorium vertraagt zowel de kankercellen als zet hen aan tot differentiatie richting meer normale myeloïde cellen, terwijl het ook de activiteit van een ander gevaarlijk gen, MECOM, vermindert. Omdat SPINK2 normaal gesproken beperkt is tot vroege bloedstamcellen en grotendeels stil is in de meeste volwassen weefsels, zouden geneesmiddelen die dit molecuul of zijn samenwerking met MECOM richten agressieve AML—vooral gevallen met complexe karyotypen—selectief kunnen verzwakken zonder de normale bloedvorming ernstig te schaden. Verder werk in diermodellen en geneesmiddelenontwikkeling is nodig, maar deze studie plaatst SPINK2 als een veelbelovende nieuwe kwetsbaarheid in een vorm van leukemie die dringend betere opties nodig heeft.
Bronvermelding: Ventura, A.B., Loconte, T., Ahmed, A. et al. SPINK2 silencing suppresses leukemic proliferation and restores myeloid commitment via MECOM downregulation in acute myeloid leukaemia. Cell Death Discov. 12, 135 (2026). https://doi.org/10.1038/s41420-026-02988-1
Trefwoorden: acute myeloïde leukemie, SPINK2, leukemische stamcellen, MECOM, myeloïde differentiatie