Clear Sky Science · es
La silenciamiento de SPINK2 suprime la proliferación leucémica y restaura el compromiso mieloide mediante la regulación a la baja de MECOM en la leucemia mieloide aguda
Por qué importa esto para el cáncer de la sangre
La leucemia mieloide aguda (LMA) es un cáncer sanguíneo de curso rápido en el que glóbulos blancos inmaduros ocupan la médula ósea, desplazando la producción normal de sangre. Muchos pacientes, en especial aquellos cuyos blastos leucémicos presentan numerosas anomalías cromosómicas (los llamados cariotipos complejos), responden mal a los tratamientos actuales. Este estudio identifica una molécula llamada SPINK2 como un colaborador clave que permite a las células leucémicas seguir dividiéndose mientras se resisten a madurar en células sanguíneas normales. Dado que SPINK2 puede silenciarse experimentalmente, podría ofrecer un nuevo modo de frenar la enfermedad y empujar a las células cancerosas hacia un destino más sano.
Un interruptor hallado en las primeras células madre sanguíneas
Los investigadores empezaron preguntando dónde aparece SPINK2 en la médula ósea sana. Empleando datos de secuenciación de ARN unicelular, que miden la actividad génica célula por célula, hallaron que SPINK2 se activa principalmente en las células madre y progenitoras sanguíneas más primitivas marcadas por CD34. Estas son células quiescentes y de ciclo lento que ocupan la cúspide del árbol de linaje sanguíneo. Conforme las células maduran por las vías mieloide o linfoide, la actividad de SPINK2 cae bruscamente y está esencialmente ausente en células sanguíneas plenamente desarrolladas. Este patrón sugiere que SPINK2 forma parte del programa que define células muy tempranas con carácter de progenitor y normalmente se apaga una vez que las células se comprometen a una función específica.
Cuando el mismo interruptor alimenta el crecimiento de la leucemia
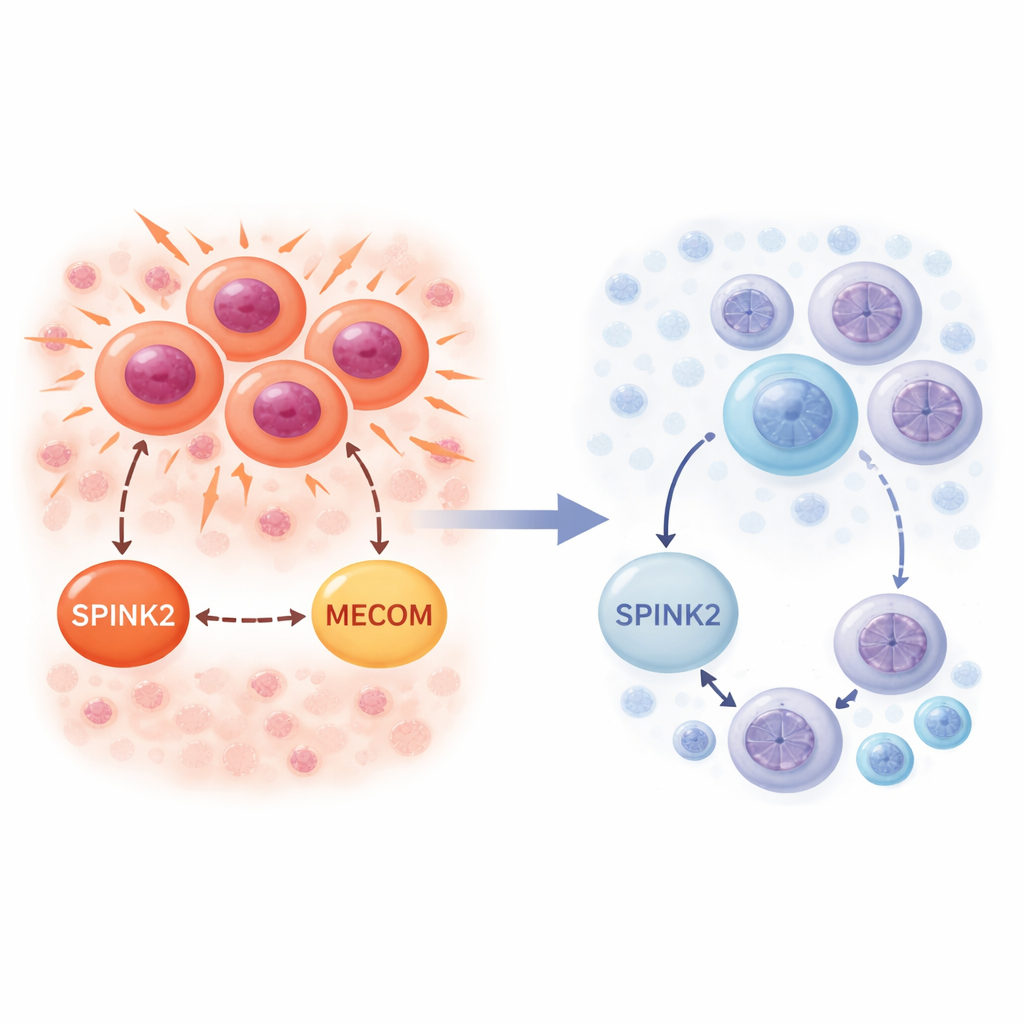
El equipo examinó luego SPINK2 en médula ósea leucémica de pacientes con LMA. Nuevamente con datos unicelulares, encontraron SPINK2 activo en las células leucémicas que más se asemejan a células madre, así como en blastos de LMA que se dividen rápidamente. En contraste con el entorno sano, aquí SPINK2 se correlacionó con señales fuertes de genes del ciclo celular, especialmente aquellos que impulsan la fase S de replicación del ADN. En cohortes masivas de pacientes de proyectos genómicos del cáncer, niveles elevados de SPINK2 se asociaron con peor supervivencia y fueron particularmente altos en personas con LMA de cariotipo complejo. En conjunto, estas observaciones indican que las células leucémicas han secuestrado un gen propio de células madre, usando SPINK2 para sostener una división imparable mientras conservan una identidad primitiva.
Apagar SPINK2 frena el cáncer y lo empuja a madurar
Para probar si SPINK2 es sólo un marcador o un verdadero impulsor, los científicos diseñaron una línea celular de LMA llamada FUJIOKA—representativa de la enfermedad con cariotipo complejo—para portar un ARN de horquilla corta inducible por doxiciclina que silencia selectivamente SPINK2. Cuando SPINK2 se apagó, las células leucémicas se dividieron mucho más despacio. El análisis detallado del ciclo celular mostró que muchas células quedaron retenidas en la fase G0/G1 y no progresaron a través de S y G2/M, sin un aumento notable de muerte celular. Al mismo tiempo, las células empezaron a mostrar niveles más altos de marcadores de superficie típicos de células mieloides maduras, lo que indica que el bloqueo de desarrollo habitual se estaba aliviando. En otras palabras, la pérdida de SPINK2 tanto eliminó el impulso proliferativo como liberó el freno de la diferenciación.
Un vínculo molecular con otro impulsor de la leucemia
La secuenciación de ARN de las células FUJIOKA antes y después del silenciamiento de SPINK2 reveló cambios extensos en la actividad génica. Cientos de genes que controlan el ciclo celular, la segregación cromosómica y los puntos de control mitóticos se reprimieron, mientras que se activaron conjuntos asociados a la síntesis proteica y las respuestas inmunitarias. Un gen destacado fue MECOM, un factor de transcripción bien conocido que promueve la leucemia, ayuda a que las células de tipo madre se autorrenueven y previene la maduración mieloide. La expresión de MECOM cayó drásticamente al silenciar SPINK2. Análisis de un gran conjunto pediátrico de LMA confirmaron que los niveles de SPINK2 y MECOM tienden a subir y bajar conjuntamente, específicamente en pacientes con cariotipos complejos. Esto apunta a un eje SPINK2–MECOM que podría coordinar la autorrenovación y la división excesivas en LMA de alto riesgo.
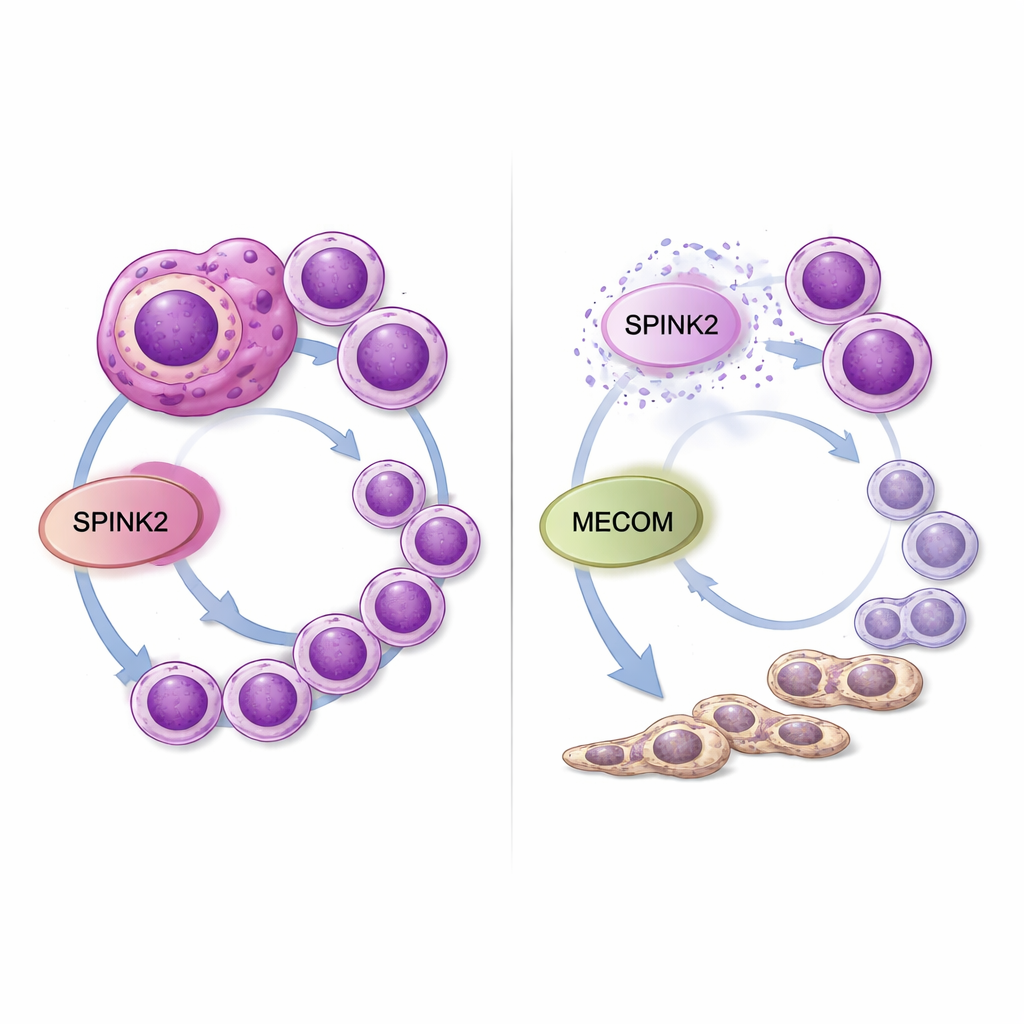
Qué significa esto para tratamientos futuros
Para un lector no especialista, estos hallazgos sugieren que SPINK2 actúa como un dial oculto en las células leucémicas que está regulado demasiado alto: mantiene a las células en un estado joven y similar a la célula madre y las anima a multiplicarse de forma descontrolada. Bajar SPINK2 en el laboratorio ralentiza las células cancerosas y las incentiva a madurar hacia células mieloides más normales, al tiempo que reduce la actividad de otro gen peligroso, MECOM. Dado que SPINK2 está normalmente restringido a las primeras células madre sanguíneas y en gran medida inactivo en la mayoría de los tejidos adultos, fármacos que apunten a esta molécula o a su asociación con MECOM podrían debilitar selectivamente la LMA agresiva—especialmente los casos de cariotipo complejo—sin dañar gravemente la producción sanguínea normal. Serán necesarios más estudios en modelos animales y esfuerzos de desarrollo farmacológico, pero este trabajo señala a SPINK2 como una vulnerabilidad prometedora en una forma de leucemia que necesita con urgencia mejores opciones.
Cita: Ventura, A.B., Loconte, T., Ahmed, A. et al. SPINK2 silencing suppresses leukemic proliferation and restores myeloid commitment via MECOM downregulation in acute myeloid leukaemia. Cell Death Discov. 12, 135 (2026). https://doi.org/10.1038/s41420-026-02988-1
Palabras clave: leucemia mieloide aguda, SPINK2, células madre leucémicas, MECOM, diferenciación mieloide