Clear Sky Science · pl
Wyciszenie SPINK2 tłumi proliferację białaczkową i przywraca zaangażowanie mieloidalne poprzez obniżenie MECOM w ostrej białaczce szpikowej
Dlaczego to ma znaczenie dla nowotworów krwi
Ostra białaczka szpikowa (AML) to szybko postępujący nowotwór krwi, w którym niedojrzałe białe krwinki przejmują szpik kostny, wypierając normalną produkcję krwi. Wielu pacjentów, zwłaszcza tych, których komórki białaczkowe mają liczne nieprawidłowości chromosomalne (tzw. złożone kariotypy), słabo odpowiada na dostępne leki. W badaniu tym zidentyfikowano cząsteczkę nazwaną SPINK2 jako kluczowego pomocnika, który pozwala komórkom białaczkowym nadal się dzielić, jednocześnie blokując ich dojrzewanie do normalnych, dojrzałych komórek krwi. Ponieważ SPINK2 można eksperymentalnie wyłączyć, może to dawać nową strategię spowolnienia choroby i skłonienia komórek nowotworowych do powrotu w stronę zdrowszego losu.
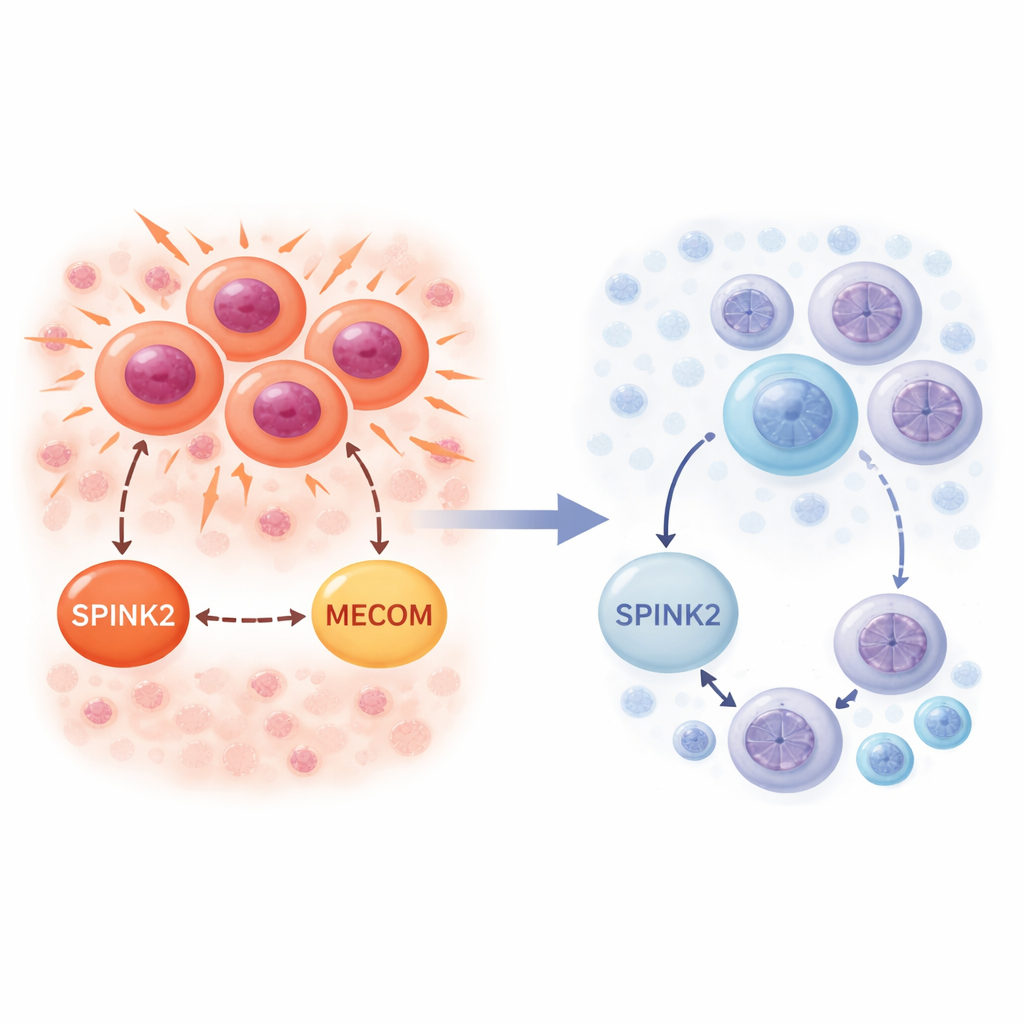
Włącznik znaleziony we wczesnych komórkach macierzystych krwi
Naukowcy najpierw zbadali, gdzie SPINK2 występuje w zdrowym szpiku. Korzystając z sekwencjonowania RNA pojedynczych komórek, które mierzy aktywność genów komórka po komórce, stwierdzili, że SPINK2 jest głównie aktywna w najpierwotniejszych komórkach macierzystych i progenitorowych oznaczonych markerem CD34. Są to spokojne, wolno dzielące się komórki, które zajmują najwyższe miejsce w drzewie rozwojowym krwi. W miarę jak komórki dojrzewają w kierunku szlaku mieloidalnego lub limfoidalnego, aktywność SPINK2 gwałtownie spada i jest praktycznie nieobecna w w pełni rozwiniętych komórkach krwi. Ten wzór sugeruje, że SPINK2 jest częścią programu definiującego bardzo wczesne komórkowe właściwości podobne do komórek macierzystych i zwykle jest wyłączana, gdy komórki angażują się w określoną funkcję.
Kiedy ten sam włącznik napędza wzrost białaczki
Zespół następnie przyjrzał się SPINK2 w białaczkowym szpiku pacjentów z AML. Ponownie, używając danych z sekwencjonowania pojedynczych komórek, znaleziono aktywną SPINK2 w komórkach białaczkowych najbardziej przypominających komórki macierzyste, a także w szybko dzielących się blastycznych komórkach AML. W przeciwieństwie do zdrowego kontekstu, tu SPINK2 współwystępowała z silnymi sygnałami płynącymi z genów cyklu komórkowego, zwłaszcza tych napędzających fazę S, w której kopiowane jest DNA. W analizach dużych zbiorów pacjentów z projektów genomiki nowotworów wyższe poziomy SPINK2 wiązały się ze gorszym przeżyciem i były szczególnie podwyższone u osób z AML o złożonym kariotypie. Razem te obserwacje wskazują, że komórki białaczkowe przejęły gen charakterystyczny dla komórek macierzystych, używając SPINK2 do podtrzymania nieustającego podziału przy zachowaniu prymitywnej tożsamości.
Wyłączenie SPINK2 hamuje nowotwór i skłania go do dojrzewania
Aby sprawdzić, czy SPINK2 jest tylko markerem, czy prawdziwym mechanizmem napędowym, naukowcy zmodyfikowali linię komórkową AML o nazwie FUJIOKA—reprezentującą chorobę z złożonym kariotypem—tak, by zawierała doksycyklinowo indukowalne krótkie RNA w kształcie spinki, selektywnie wyciszające SPINK2. Po wyłączeniu SPINK2 komórki białaczkowe dzieliły się znacznie wolniej. Szczegółowa analiza cyklu komórkowego wykazała, że wiele komórek utknęło w fazie G0/G1 i nie przechodziło przez fazy S i G2/M, bez zauważalnego wzrostu śmierci komórek. Jednocześnie komórki zaczęły wykazywać wyższe poziomy markerów powierzchniowych typowych dla dojrzałych komórek mieloidalnych, co wskazuje, że zwykły blok rozwojowy ulegał rozluźnieniu. Innymi słowy, utrata SPINK2 zarówno usuwała impuls wzrostu, jak i zwalniała hamulec różnicowania.
Molekularne powiązanie z innym czynnikiem białaczkowym
Sekwencjonowanie RNA komórek FUJIOKA przed i po wyciszeniu SPINK2 ujawniło szerokie zmiany w aktywności genów. Setki genów kontrolujących cykl komórkowy, segregację chromosomów i punkty kontrolne mitozy zostały przygaszone, podczas gdy zestawy związane z syntezą białek i odpowiedziami immunologicznymi zostały wzmocnione. Jednym z wyróżniających się był MECOM, dobrze znany czynnik transkrypcyjny sprzyjający białaczce, który pomaga komórkom podobnym do macierzystych samoodnawiać się i zapobiega dojrzewaniu mieloidalnemu. Ekspresja MECOM gwałtownie spadła po wyciszeniu SPINK2. Analizy dużego pediatrycznego zestawu danych AML potwierdziły, że poziomy SPINK2 i MECOM mają tendencję do wspólnego wzrostu i spadku, zwłaszcza u pacjentów z złożonym kariotypem. Wskazuje to na oś SPINK2–MECOM, która może koordynować nadmierne samoodnawianie i podziały w wysokiego ryzyka AML.
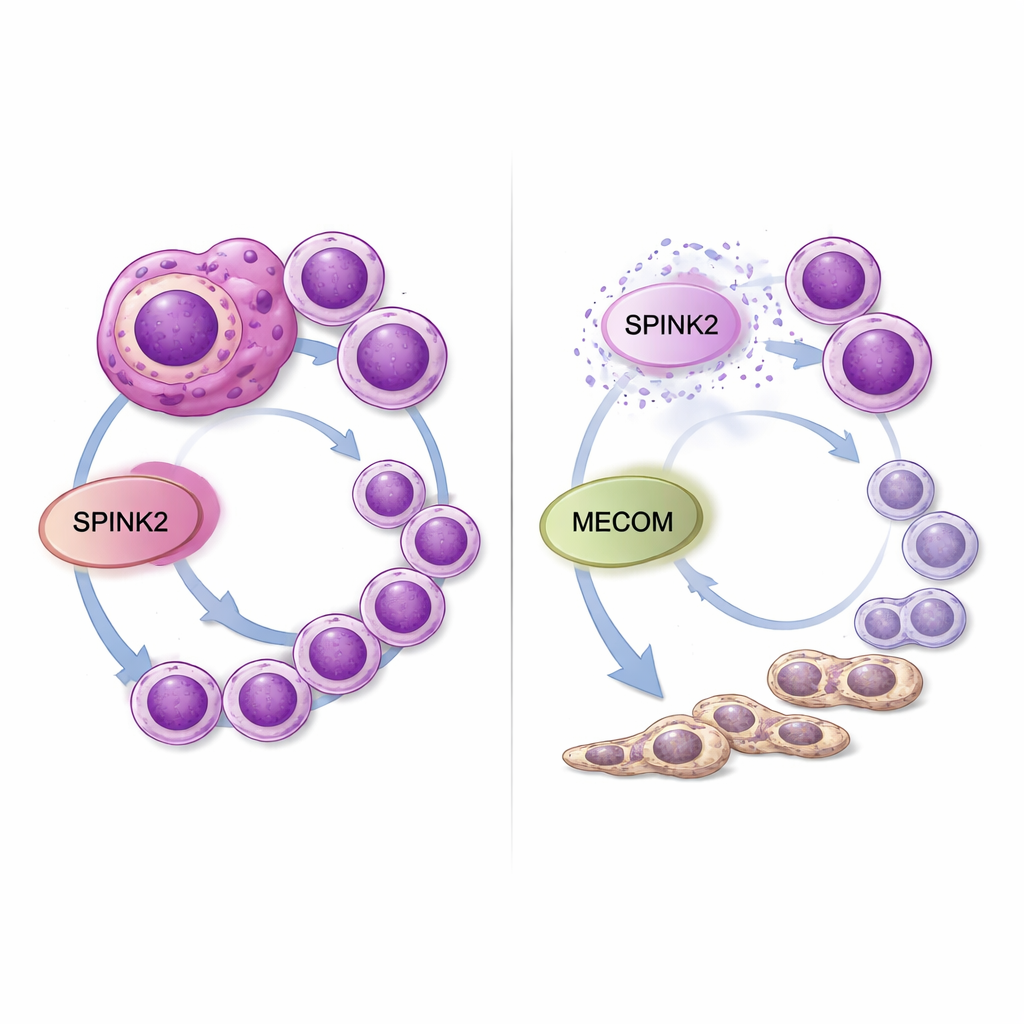
Co to oznacza dla przyszłych terapii
Dla obserwatora z zewnątrz te wyniki sugerują, że SPINK2 działa jak ukryty regulator w komórkach białaczkowych, ustawiony zbyt wysoko: utrzymuje komórki w młodzieńczym, podobnym do macierzystych stanie i pobudza je do niekontrolowanego mnożenia. Zmniejszenie aktywności SPINK2 w laboratorium zarówno spowalnia komórki nowotworowe, jak i sprzyja ich przekształceniu w bardziej normalne komórki mieloidalne, jednocześnie obniżając aktywność innego groźnego genu, MECOM. Ponieważ SPINK2 jest normalnie ograniczona do wczesnych komórek macierzystych krwi i w dużej mierze nieaktywna w większości tkanek dorosłego organizmu, leki celujące w tę cząsteczkę lub jej związek z MECOM mogłyby selektywnie osłabić agresywne AML—szczególnie przypadki z złożonym kariotypem—bez poważnego uszczerbku dla normalnej produkcji krwi. Potrzebne będą dalsze badania w modelach zwierzęcych i prace nad rozwojem leków, ale to badanie wskazuje SPINK2 jako obiecującą nową słabość w formie białaczki, która pilnie potrzebuje lepszych opcji terapeutycznych.
Cytowanie: Ventura, A.B., Loconte, T., Ahmed, A. et al. SPINK2 silencing suppresses leukemic proliferation and restores myeloid commitment via MECOM downregulation in acute myeloid leukaemia. Cell Death Discov. 12, 135 (2026). https://doi.org/10.1038/s41420-026-02988-1
Słowa kluczowe: ostra białaczka szpikowa, SPINK2, komórki macierzyste białaczki, MECOM, różnicowanie mieloidalne