Clear Sky Science · zh
Sirt2–Nur77 轴通过表观遗传—代谢协同调节肌肉干细胞静止与衰老
为什么肌肉随年龄变弱
随着年龄增长,虚弱常常悄然出现:爬楼梯更吃力,拧罐头更费劲,腿更容易疲劳。本文研究探索了这种日常体验背后的一个基本问题:负责修复和重建肌肉的肌肉干细胞为何会随年龄失去功能?通过发现这些细胞内的一个关键控制开关,作者指向了未来可能用药物减缓甚至逆转年龄相关肌肉流失的新途径。
肌肉干细胞内的隐秘开关
骨骼肌由一小队常处于静息状态的肌肉干细胞持续维护,直到受伤或运动将它们唤醒。在年老的动物中,这些细胞唤醒更慢,修复能力下降,并且数量逐渐减少,促成了肌少症——随年龄而来的肌肉质量和力量丧失。研究人员聚焦于两种在多种器官中随年龄改变的蛋白:Nur77(下降)和 Sirt2(上升)。他们怀疑这两种相反的变化构成了一个普遍的衰老“轴”,并着手检验其在骨骼肌中的具体作用。
Sirt2 如何耗损 Nur77
在肌肉干细胞内,Nur77 是一种基因调控因子,帮助决定静止的干细胞何时激活并开始构建新的肌纤维。研究团队发现 Sirt2 在细胞核内与 Nur77 结合,并化学性地去除 Nur77 上一个精确位点的小型乙酰基(小鼠中称为 K310 的单个氨基酸位点)。当该乙酰标记被去除,Nur77 变得不稳定:它被标记为需降解,进入细胞的废弃处理机制被分解,水平下降。反之,当乙酰标记存在时,Nur77 得以稳定并更有效地结合靶基因的 DNA。
从分子调整到修复失效
在该情境中,Nur77 最重要的靶基因是 Myf5,一个促使肌肉干细胞从深度静息进入准备修复状态的基因。研究人员显示,乙酰化的 Nur77 强烈结合 Myf5 的调控区并激活它,促进干细胞及时激活和损伤后新肌纤维的形成。当完全缺失 Nur77,或将 K310 位点锁定为去乙酰状态时,肌纤维发育更小、损伤后再生不良并伴随更多瘢痕。干细胞分裂方式也不利,倾向于耗尽干细胞库,而非在自我更新与分化之间保持平衡。在老年小鼠中,Sirt2 增高、Nur77 降低时,这种不平衡尤为明显。
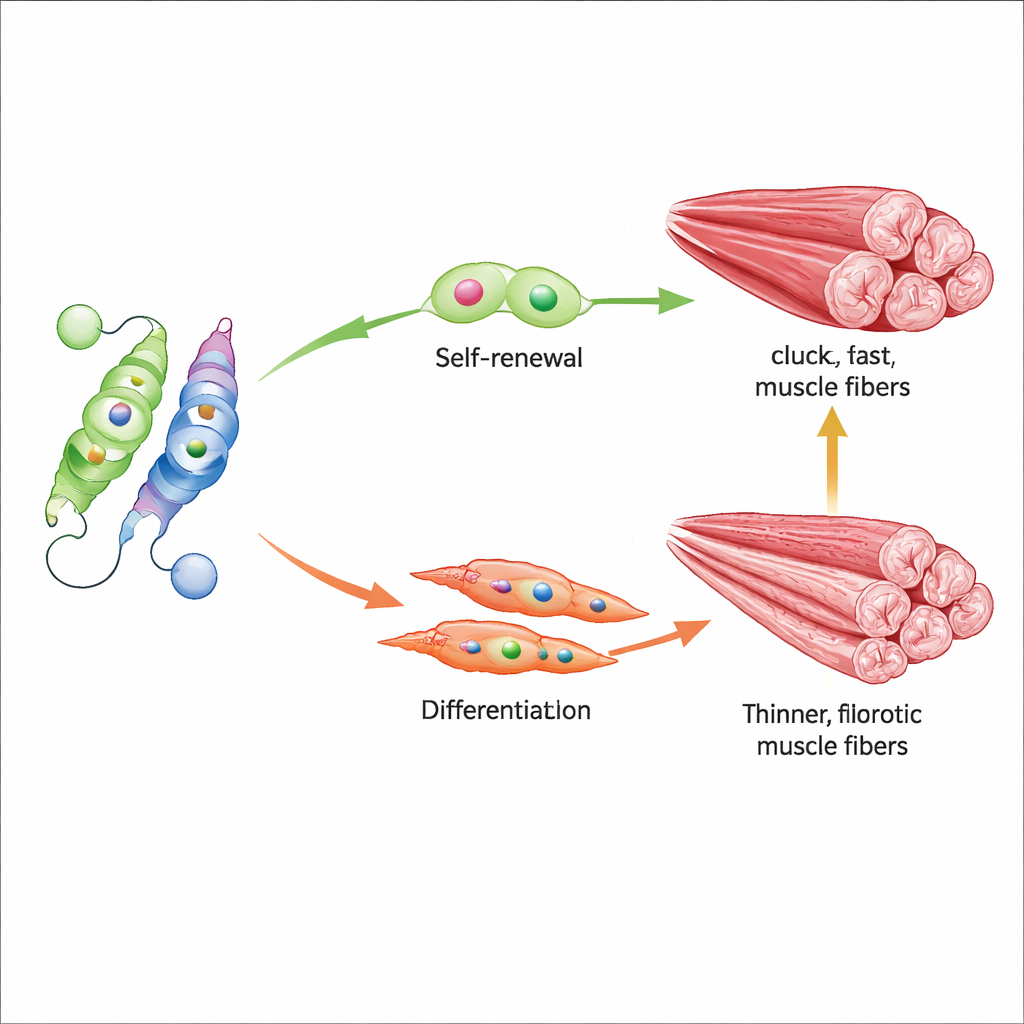
将平衡轻推回来的药物
研究还检验了两种能将这对分子跷跷板向相反方向推动的小分子化合物。AGK2 抑制 Sirt2,间接保留 Nur77 上的乙酰标记并阻止其被降解,而 CSNB 则直接激活 Nur77。在年老小鼠中,任一化合物处理都提高了 Nur77 活性,提升了 Myf5 及早期肌肉生成蛋白的表达,并在握力和跑动距离上出现可测量的改善。在组织层面,处理过的肌肉更好地维持了快速、有力的肌纤维并显示出更少的纤维化,这表明调节这一单一乙酰化位点可以同时影响干细胞行为与整体肌肉质量。
对健康老龄化的意义
综述而言,这项工作勾勒出一条简单但强有力的事件链:随着年龄增长,Sirt2 上升剥离了 Nur77 的保护性化学标签,Nur77 变得不稳定并下降,像 Myf5 这样的关键修复基因活性降低,干细胞的更新与修复效率下降,肌肉逐步萎缩并出现瘢痕。通过恢复 Nur77 的乙酰化形式——无论是抑制 Sirt2 还是直接刺激 Nur77——作者能够部分重置这条链并在老年小鼠中回春肌肉功能。尽管在将此类策略安全应用于人类之前还有许多工作要做,该研究突出了一个特定的分子开关,未来有望成为帮助人们在晚年保持更强健、更灵活、更独立的靶点。
引用: Wang, Y., Yang, Y., Yu, W. et al. The Sirt2–Nur77 axis regulates muscle stem cell quiescence and senescence via epigenetic–metabolic synergy. Cell Death Dis 17, 429 (2026). https://doi.org/10.1038/s41419-026-08645-w
关键词: 肌肉老化, 肌肉干细胞, Nur77, Sirt2, 肌少症