Clear Sky Science · pl
Oś Sirt2–Nur77 reguluje uśpienie i starzenie się komórek macierzystych mięśni poprzez synergiczne działanie epigenetyczno‑metaboliczne
Dlaczego mięśnie stają się słabsze z wiekiem
Starzenie się często podstępnie objawia się jako zwykła słabość: wchodzenie po schodach staje się trudniejsze, słoiki trudniej otworzyć, a nogi szybciej tracą wytrzymałość. To badanie stawia fundamentalne pytanie kryjące się za tym codziennym doświadczeniem: dlaczego nasze komórki macierzyste mięśni, które zwykle naprawiają i odbudowują mięsień, tracą sprawność z wiekiem? Odkrywając kluczowy przełącznik wewnątrz tych komórek, autorzy wskazują nowe drogi, dzięki którym w przyszłości leki mogłyby spowolnić, a nawet odwrócić związane z wiekiem zaniki mięśni.
Ukryty przełącznik wewnątrz komórek macierzystych mięśni
Mięsień szkieletowy jest stale utrzymywany przez małą rezerwę komórek macierzystych mięśni, które zwykle spoczywają w stanie uśpienia, aż uraz lub ćwiczenie nie wezwą ich do działania. U starszych zwierząt komórki te budzą się wolniej, regenerują mięśnie mniej efektywnie i stopniowo zanikają, przyczyniając się do sarkopenii, czyli związanej z wiekiem utraty masy i siły mięśniowej. Badacze skupili się na dwóch białkach, których poziomy zmieniają się z wiekiem w wielu narządach: Nur77, którego ilość spada, oraz Sirt2, którego poziom rośnie. Podejrzewali, że te przeciwstawne zmiany tworzą wspólną „oś” starzenia i postanowili zbadać jej rolę konkretnie w mięśniu szkieletowym.
Jak Sirt2 osłabia Nur77
W komórkach macierzystych mięśni Nur77 działa jako czynnik kontrolujący geny, pomagając decydować, kiedy uśpiona komórka macierzysta powinna się aktywować i rozpocząć budowę nowych włókien. Zespół odkrył, że Sirt2 wiąże się fizycznie z Nur77 w jądrze komórkowym i chemicznie usuwa małe grupy acetylowe z precyzyjnego miejsca na Nur77 (pojedynczego aminokwasu o pozycji nazwanej K310 u myszy). Gdy znak acetylowy zostaje usunięty, Nur77 staje się niestabilny: zostaje oznaczony do zniszczenia, rozkładany przez komórkowe mechanizmy utylizacyjne i jego poziom spada. Gdy znak acetylowy jest obecny, Nur77 jest stabilizowany i może skuteczniej wiązać DNA docelowych genów.
Od molekularnej modyfikacji do zawodzącej naprawy mięśni
Najważniejszym celem Nur77 w tym kontekście jest Myf5, gen, który pomaga przesunąć komórki macierzyste mięśni z głębokiego spoczynku w stan gotowości do naprawy. Badacze wykazali, że acetylowany Nur77 silnie wiąże się z regionem kontrolnym Myf5 i go aktywuje, promując terminową aktywację komórek macierzystych oraz tworzenie nowych włókien mięśniowych po urazie. Gdy Nur77 jest całkowicie nieobecny albo kiedy miejsce K310 jest trwale zdeacetylowane, mięśnie rozwijają mniejsze włókna, regenerują się słabiej po uszkodzeniu i wykazują więcej bliznowacenia. Komórki macierzyste również dzielą się w sposób mniej korzystny, mając tendencję do wyczerpywania rezerwy zamiast równoważenia samoodnawiania z różnicowaniem. U starych myszy, u których Sirt2 jest wyższe, a Nur77 niższe, ta nierównowaga jest szczególnie wyraźna.
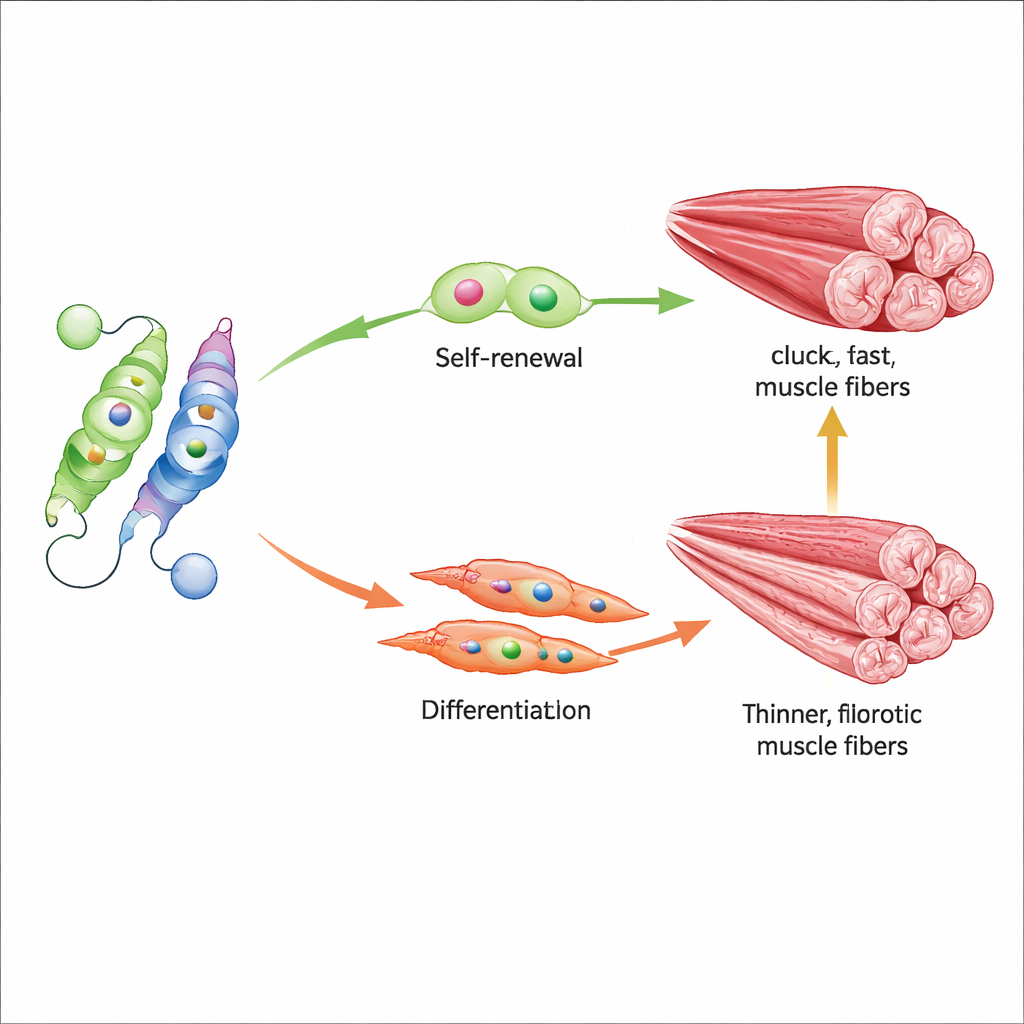
Leki przesuwające równowagę z powrotem
W badaniu przetestowano także dwie małe molekuły, które popychają to molekularne wahadło w przeciwne strony. AGK2 blokuje Sirt2, pośrednio zachowując znak acetylowy na Nur77 i zapobiegając jego zniszczeniu, podczas gdy CSNB bezpośrednio aktywuje Nur77. U starych myszy leczenie którymkolwiek z tych związków zwiększało aktywność Nur77, podnosiło poziomy Myf5 i wczesnych białek budujących mięsień oraz mierzalnie poprawiało siłę chwytu i dystans biegu. Na poziomie tkankowym leczone mięśnie lepiej utrzymywały szybkie, silne włókna i wykazywały mniej włóknienia, co sugeruje, że dostrojenie tego pojedynczego miejsca acetylacji może wpływać zarówno na zachowanie komórek macierzystych, jak i na ogólną jakość mięśnia.
Co to oznacza dla zdrowego starzenia
W sumie praca opisuje prosty, lecz silny łańcuch zdarzeń: z wiekiem rosnący Sirt2 zdziera ochronny chemiczny znacznik z Nur77, Nur77 staje się niestabilny i jego poziom spada, kluczowe geny naprawcze takie jak Myf5 są mniej aktywne, komórki macierzyste odnawiają i naprawiają słabiej, a mięśnie stopniowo zanikają i bliznowacieją. Przywracając acetylowaną formę Nur77 — albo przez inhibicję Sirt2, albo bezpośrednią stymulację Nur77 — autorom udało się częściowo zresetować ten ciąg i odmłodzić funkcję mięśni u starych myszy. Chociaż przed bezpiecznym zastosowaniem takich strategii u ludzi pozostaje jeszcze wiele pracy, badanie wskazuje konkretny molekularny przełącznik, który pewnego dnia może zostać wykorzystany, by pomóc ludziom pozostać silniejszymi, bardziej ruchliwymi i bardziej niezależnymi w późniejszym wieku.
Cytowanie: Wang, Y., Yang, Y., Yu, W. et al. The Sirt2–Nur77 axis regulates muscle stem cell quiescence and senescence via epigenetic–metabolic synergy. Cell Death Dis 17, 429 (2026). https://doi.org/10.1038/s41419-026-08645-w
Słowa kluczowe: starzenie się mięśni, komórki macierzyste mięśni, Nur77, Sirt2, sarkopenia