Clear Sky Science · ru
Ось Sirt2–Nur77 регулирует покой и сенесценцию мышечных стволовых клеток через эпигенетико‑метаболическое взаимодействие
Почему мышцы с возрастом становятся слабее
Старение часто подкрадывается незаметно в виде простой слабости: подниматься по лестнице становится труднее, банки сложнее открыть, а ноги устают быстрее. В этом исследовании поставлен фундаментальный вопрос, лежащий в основе такого повседневного опыта: почему наши мышечные стволовые клетки, которые обычно восстанавливают и перестраивают мышцы, с возрастом теряют свои возможности? Обнаружив ключевой управляющий переключатель внутри этих клеток, авторы указывают на новые пути, с помощью которых в будущем лекарство может замедлить или даже обратить возрастную потерю мышечной массы.
Скрытый переключатель внутри мышечных стволовых клеток
Скелетные мышцы постоянно поддерживаются небольшой резервной армией мышечных стволовых клеток, которые обычно тихо пребывают в покое до тех пор, пока травма или физическая нагрузка не призовут их в действие. У старых животных эти клетки пробуждаются медленнее, хуже регенерируют мышцы и постепенно исчезают, что способствует саркопении — возрастной потере мышечной массы и силы. Исследователи сосредоточились на двух белках, уровни которых меняются с возрастом во многих органах: Nur77, который снижается, и Sirt2, который повышается. Они предположили, что эти противоположные изменения образуют общую ось старения и решили проверить её роль конкретно в скелетных мышцах.
Как Sirt2 подтачивает Nur77
Внутри мышечных стволовых клеток Nur77 действует как фактор регуляции генов, который помогает решать, когда отдыхающая стволовая клетка должна активироваться и начать формировать новые волокна. Команда обнаружила, что Sirt2 физически связывается с Nur77 в ядре клетки и химически удаляет небольшие ацетильные группы с точечного места на Nur77 (одна аминокислотная позиция, называемая K310 у мышей). Когда этот ацетильный маркер снят, Nur77 становится неустойчивым: он помечается для разрушения, расщепляется системой утилизации клетки, и его уровень падает. Когда ацетильная метка присутствует, Nur77 стабилен и может эффективнее связываться с ДНК целевых генов.
От молекулярной модификации к нарушенному восстановлению мышц
Самая важная мишень Nur77 в этом контексте — ген Myf5, который помогает подтолкнуть мышечные стволовые клетки от глубокого покоя в состояние, готовое к ремонту. Исследователи показали, что ацетилированный Nur77 сильно связывается с регуляторной областью Myf5 и включает его, способствуя своевременной активации стволовых клеток и образованию новых мышечных волокон после повреждения. Когда Nur77 полностью отсутствует или когда сайт K310 зафиксирован в деацетилированном состоянии, в мышцах развиваются более мелкие волокна, регенерация после повреждений ухудшается, и наблюдается больше рубцевания. Стволовые клетки также делятся менее благоприятно, склоняясь к истощению пула вместо поддержания баланса между самовозобновлением и дифференцировкой. У старых мышей, где Sirt2 выше, а Nur77 ниже, этот дисбаланс особенно выражен.
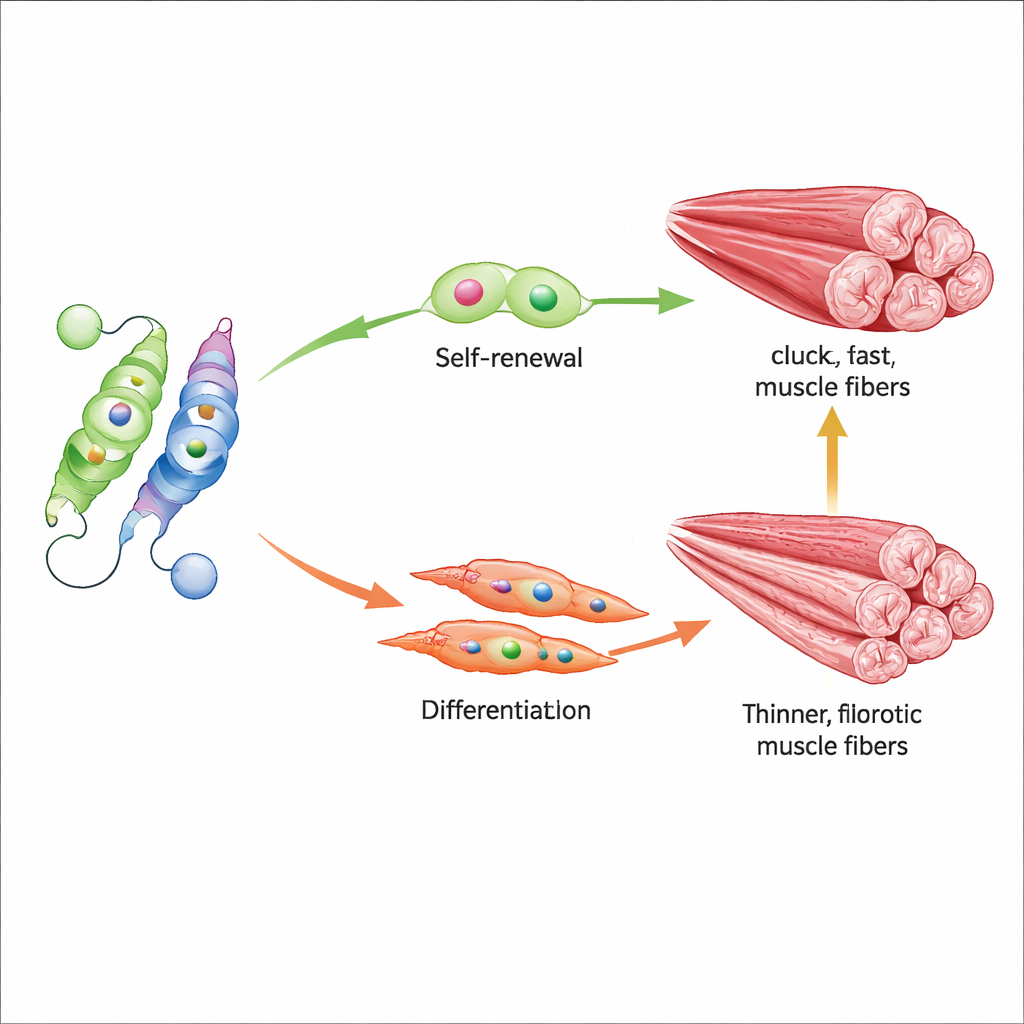
Препараты, сдвигающие баланс обратно
В исследовании также протестировали две малые молекулы, которые толкают это молекулярное качание в противоположные стороны. AGK2 блокирует Sirt2, косвенно сохраняя ацетильную метку на Nur77 и предотвращая его разрушение, тогда как CSNB напрямую активирует Nur77. У старых мышей лечение любой из этих соединений повышало активность Nur77, усиливало Myf5 и ранние белки, участвующие в сборке мышц, и ощутимо улучшало силу захвата и дистанцию бега. На уровне ткани леченые мышцы лучше сохраняли быстрые, мощные волокна и демонстрировали меньше фиброза, что указывает на то, что настройка этой единственной ацетилированной позиции может влиять и на поведение стволовых клеток, и на общее качество мышц.
Что это означает для здорового старения
В совокупности работа выстраивает простую, но мощную цепочку событий: с возрастом повышающийся Sirt2 снимает защитную химическую метку с Nur77, Nur77 становится неустойчивым и снижается, ключевые гены восстановления, такие как Myf5, становятся менее активными, стволовые клетки реже обновляют и ремонтируют ткани эффективно, и мышцы постепенно атрофируются и рубцуются. Восстановив ацетилированную форму Nur77 — либо путем ингибирования Sirt2, либо прямой стимуляцией Nur77 — авторы смогли частично перезапустить эту цепочку и омолодить функцию мышц у старых мышей. Хотя до безопасного применения таких стратегий у людей предстоит проделать ещё много работы, исследование выделяет конкретный молекулярный переключатель, который однажды может стать целью для того, чтобы люди оставались сильнее, более подвижными и более независимыми в поздней жизни.
Цитирование: Wang, Y., Yang, Y., Yu, W. et al. The Sirt2–Nur77 axis regulates muscle stem cell quiescence and senescence via epigenetic–metabolic synergy. Cell Death Dis 17, 429 (2026). https://doi.org/10.1038/s41419-026-08645-w
Ключевые слова: старение мышц, мышечные стволовые клетки, Nur77, Sirt2, саркопения