Clear Sky Science · fr
L’axe Sirt2–Nur77 régule la quiescence et la sénescence des cellules souches musculaires via une synergie épigénétique–métabolique
Pourquoi les muscles s’affaiblissent avec l’âge
Le vieillissement se manifeste souvent par une faiblesse diffuse : monter des escaliers devient plus difficile, ouvrir des bocaux demande plus d’effort, et les jambes se fatiguent plus vite. Cette étude cherche à élucider une question fondamentale sous-jacente à cette expérience quotidienne : pourquoi nos cellules souches musculaires, qui réparent et reconstruisent normalement le muscle, perdent-elles leur efficacité avec l’âge ? En identifiant un interrupteur clé à l’intérieur de ces cellules, les auteurs indiquent de nouvelles voies par lesquelles des médicaments pourraient un jour ralentir voire inverser la perte musculaire liée à l’âge.
Un interrupteur caché à l’intérieur des cellules souches musculaires
Le muscle squelettique est entretenu en continu par une petite réserve de cellules souches musculaires qui restent normalement au repos jusqu’à ce qu’une blessure ou l’exercice les mobilise. Chez les animaux âgés, ces cellules se réveillent plus lentement, régénèrent le muscle moins efficacement et disparaissent progressivement, contribuant à la sarcopénie, la perte d’ampleur et de force musculaire liée à l’âge. Les chercheurs se sont concentrés sur deux protéines dont les niveaux changent avec l’âge dans de nombreux organes : Nur77, qui diminue, et Sirt2, qui augmente. Ils ont émis l’hypothèse que ces changements opposés forment un « axe » commun du vieillissement et ont cherché à en tester le rôle spécifiquement dans le muscle squelettique.
Comment Sirt2 use Nur77
Dans les cellules souches musculaires, Nur77 agit comme un facteur de contrôle des gènes qui aide à décider quand une cellule souche au repos doit s’activer et commencer à construire de nouvelles fibres. L’équipe a découvert que Sirt2 se lie physiquement à Nur77 dans le noyau cellulaire et enlève chimiquement de petits groupes acétyle à un site précis de Nur77 (un seul acide aminé appelé K310 chez la souris). Lorsque cette marque acétyle est retirée, Nur77 devient instable : il est marqué pour destruction, dégradé par les mécanismes d’élimination cellulaire, et son niveau baisse. Lorsque la marque acétyle est présente, Nur77 est stabilisé et peut se lier plus efficacement à l’ADN des gènes cibles.
Du réglage moléculaire à l’échec de la réparation musculaire
La cible la plus importante de Nur77 dans ce contexte est Myf5, un gène qui aide à pousser les cellules souches musculaires du repos profond vers un état prêt à réparer. Les chercheurs ont montré que Nur77 acétylé se lie fortement à la région de contrôle de Myf5 et l’active, favorisant l’activation en temps utile des cellules souches et la formation de nouvelles fibres musculaires après une lésion. Lorsque Nur77 manque complètement, ou lorsque le site K310 est verrouillé dans un état désacétylé, les muscles développent des fibres plus petites, régénèrent mal après une atteinte et présentent davantage de cicatrices. Les cellules souches se divisent aussi d’une manière moins favorable, tendant à épuiser leur réservoir plutôt qu’à équilibrer auto-renouvellement et différenciation. Chez les souris âgées, où Sirt2 est plus élevé et Nur77 plus faible, ce déséquilibre est particulièrement marqué.
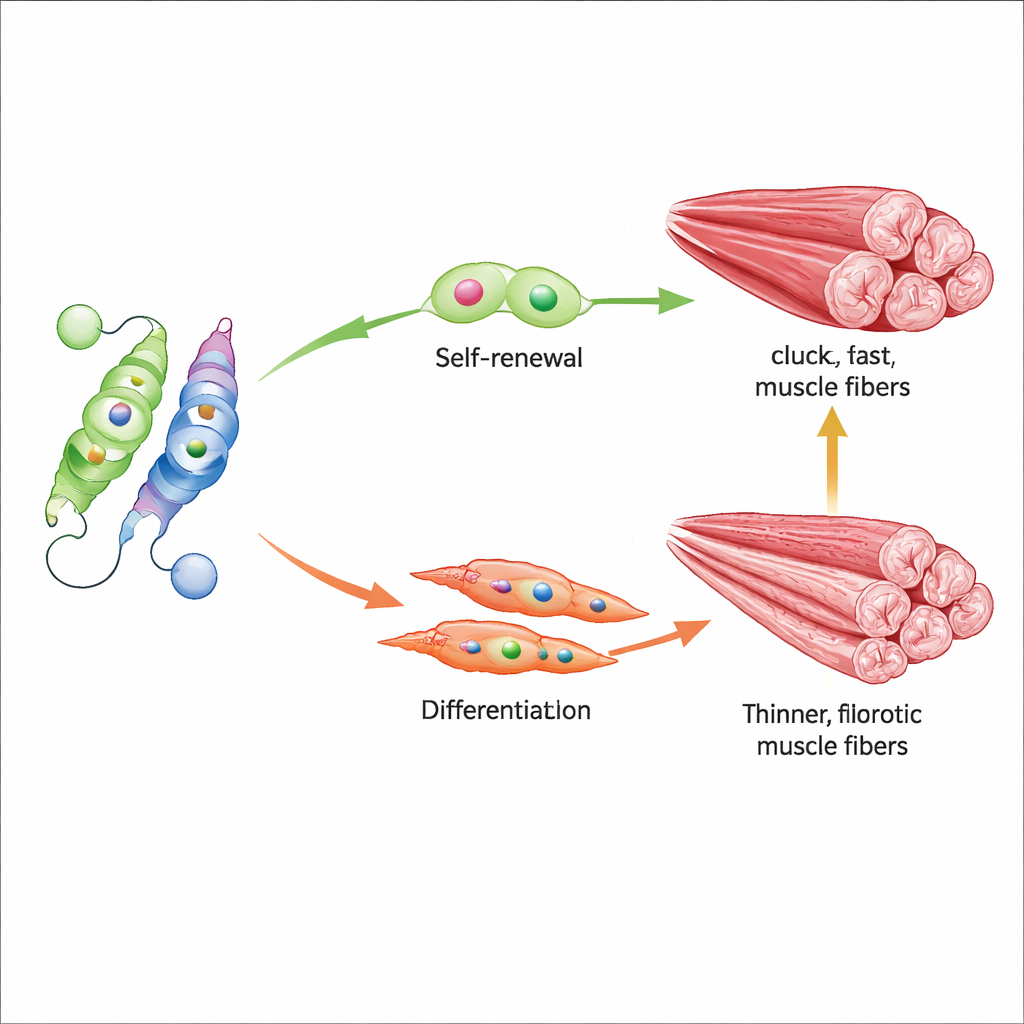
Des médicaments qui rééquilibrent la balance
L’étude a également testé deux petites molécules qui poussent cette balance moléculaire dans des directions opposées. AGK2 bloque Sirt2, préservant indirectement la marque acétyle sur Nur77 et empêchant sa destruction, tandis que CSNB active directement Nur77. Chez les souris âgées, le traitement par l’une ou l’autre de ces molécules a augmenté l’activité de Nur77, stimulé Myf5 et des protéines précoces de construction musculaire, et amélioré de façon mesurable la force de préhension et la distance de course. Au niveau du tissu, les muscles traités ont mieux conservé des fibres rapides et puissantes et ont montré moins de fibrose, suggérant que la modulation de ce seul site d’acétylation peut influencer à la fois le comportement des cellules souches et la qualité musculaire globale.
Quelles implications pour un vieillissement en bonne santé
Ensemble, ces travaux décrivent une chaîne d’événements simple mais puissante : avec l’âge, l’augmentation de Sirt2 enlève une étiquette chimique protectrice de Nur77, Nur77 devient instable et décroît, des gènes de réparation clés comme Myf5 sont moins actifs, les cellules souches renouvellent et réparent moins efficacement, et les muscles s’atrophient et se cicatrisent progressivement. En restaurant la forme acétylée de Nur77—soit en inhibant Sirt2, soit en stimulant directement Nur77—les auteurs ont pu réinitialiser partiellement cette cascade et rajeunir la fonction musculaire chez des souris âgées. Bien que beaucoup reste à faire avant que de telles stratégies puissent être appliquées en toute sécurité à l’humain, l’étude met en lumière un interrupteur moléculaire spécifique qui pourrait un jour être ciblé pour aider les personnes à rester plus fortes, plus mobiles et plus indépendantes en fin de vie.
Citation: Wang, Y., Yang, Y., Yu, W. et al. The Sirt2–Nur77 axis regulates muscle stem cell quiescence and senescence via epigenetic–metabolic synergy. Cell Death Dis 17, 429 (2026). https://doi.org/10.1038/s41419-026-08645-w
Mots-clés: vieillissement musculaire, cellules souches musculaires, Nur77, Sirt2, sarcopénie