Clear Sky Science · sv
Sirt2–Nur77-axeln reglerar muskelstamcellskviescens och senescens via epigenetisk–metabolisk synergi
Varför muskler blir svagare med åldern
Åldrandet smyger sig ofta på oss som enkel svaghet: att gå i trappor känns tyngre, burkar är svårare att öppna och benen tröttnar snabbare. Den här studien ställer en grundläggande fråga bakom den vardagliga upplevelsen: varför tappar våra muskelstamceller, som normalt reparerar och bygger upp muskler, sin skärpa med åldern? Genom att avslöja en nyckelkontrollpunkt inne i dessa celler pekar författarna på nya sätt som läkemedel en dag kan bromsa eller till och med vända åldersrelaterad muskelförlust.
En dold strömbrytare inne i muskelstamceller
Skelettmuskulatur underhålls ständigt av en liten reservstyrka av muskelstamceller som normalt vilar tyst tills skada eller träning kallar dem till handling. Hos äldre djur vaknar dessa celler långsammare, regenererar muskler mindre effektivt och försvinner gradvis, vilket bidrar till sarkopeni — den åldersrelaterade förlusten av muskelmassa och styrka. Forskarna inriktade sig på två proteiner vars nivåer förändras med åldern i många organ: Nur77, som minskar, och Sirt2, som ökar. De misstänkte att dessa motsatta förändringar bildar en gemensam åldrings"axel" och gav sig i kast med att testa dess roll specifikt i skelettmuskulatur.
Hur Sirt2 bryter ner Nur77
Inne i muskelstamceller fungerar Nur77 som en genreglerande faktor som hjälper till att avgöra när en vilande stamcell ska aktiveras och börja bygga nya fibrer. Teamet upptäckte att Sirt2 fysiskt binder till Nur77 i cellkärnan och kemiskt tar bort små acetylgrupper från en exakt plats på Nur77 (en enskild aminosyraställning kallad K310 hos möss). När denna acetylmarkör avlägsnas blir Nur77 instabilt: det märks för nedbrytning, kasseras av cellens avfallsmekanismer och dess nivåer sjunker. När acetylmarkören finns kvar stabiliseras Nur77 och kan binda målgenernas DNA mer effektivt.
Från molekylär justering till misslyckad muskelreparation
Nur77s viktigaste mål i detta sammanhang är Myf5, en gen som hjälper till att föra muskelstamceller från djup vila till ett reparationsredo tillstånd. Forskarna visade att acetylerat Nur77 binder starkt till Myf5:s kontrollregion och slår på den, vilket gynnar tidig aktivering av stamceller och bildandet av nya muskelfibrer efter skada. När Nur77 saknas helt, eller när K310-stället är låst i ett deacetylerat tillstånd, utvecklar musklerna mindre fibrer, regenererar dåligt efter skada och uppvisar mer ärrbildning. Stamceller delar sig också på ett mindre gynnsamt sätt, med tendens att tömma sin reserv istället för att balansera självgenerering och differentiering. Hos åldrade möss, där Sirt2 är högre och Nur77 lägre, är denna obalans särskilt uttalad.
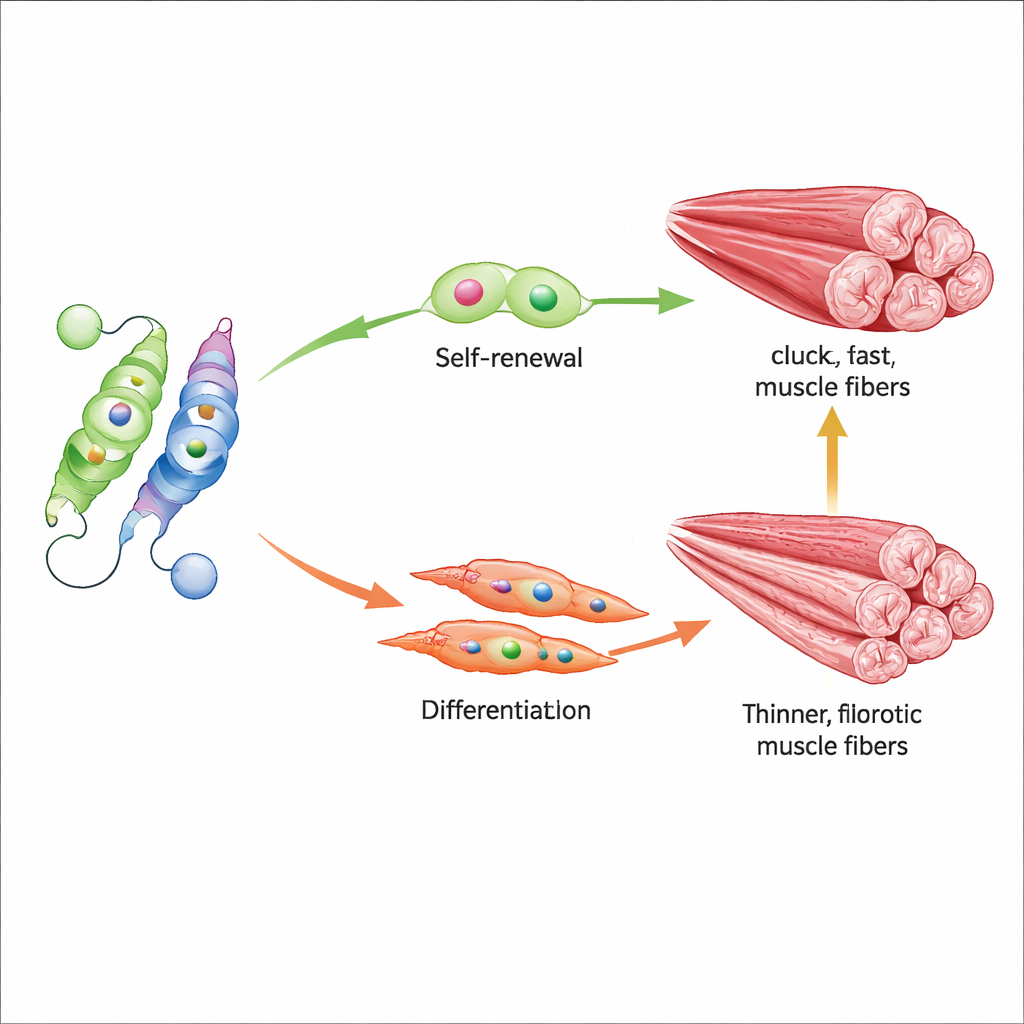
Läkemedel som återställer balansen
Studien testade också två små molekyler som skjuter denna molekylära gungbräda i motsatta riktningar. AGK2 blockerar Sirt2 och bevarar indirekt acetylmärket på Nur77 och förhindrar dess nedbrytning, medan CSNB direkt aktiverar Nur77. Hos gamla möss ökade behandling med någon av föreningarna Nur77-aktiviteten, boostade Myf5 och tidiga muskeluppbyggande proteiner och förbättrade mätbart greppstyrka och löpsträcka. På vävnadsnivå behöll behandlade muskler bättre snabba, kraftfulla fibrer och visade mindre fibros, vilket tyder på att justering av denna enda acetyleringsplats kan påverka både stamcellsbeteende och den övergripande muskelkvaliteten.
Vad detta betyder för ett hälsosamt åldrande
Sammantaget beskriver arbetet en enkel men kraftfull kedja av händelser: med åldern tar stigande Sirt2 bort en skyddande kemisk markör från Nur77, Nur77 blir instabilt och minskar, nyckelreparationsgener som Myf5 blir mindre aktiva, stamceller förnyar och reparerar mindre effektivt och musklerna gradvis atroferar och ärras. Genom att återställa den acetylerade formen av Nur77 — antingen genom att hämma Sirt2 eller genom att direkt stimulera Nur77 — kunde författarna delvis nollställa denna kedja och föryngra muskelfunktion hos gamla möss. Mycket återstår att göra innan sådana strategier kan tillämpas säkert på människor, men studien lyfter fram en specifik molekylär strömbrytare som en dag kan riktas mot för att hjälpa människor att förbli starkare, mer rörliga och mer självständiga senare i livet.
Citering: Wang, Y., Yang, Y., Yu, W. et al. The Sirt2–Nur77 axis regulates muscle stem cell quiescence and senescence via epigenetic–metabolic synergy. Cell Death Dis 17, 429 (2026). https://doi.org/10.1038/s41419-026-08645-w
Nyckelord: muskelåldrande, muskelstamceller, Nur77, Sirt2, sarkopeni