Clear Sky Science · de
Die Sirt2–Nur77‑Achse reguliert die Quieszenz und Seneszenz von Muskels Stammzellen durch epigenetisch‑metabolische Synergie
Warum Muskeln mit dem Alter schwächer werden
Altern zeigt sich oft als schleichende Schwäche: Treppensteigen fällt schwerer, Gläser lassen sich schwieriger öffnen und die Beine ermüden schneller. Diese Studie stellt eine grundlegende Frage hinter dieser alltäglichen Erfahrung: Warum verlieren unsere Muskels Stammzellen, die normalerweise Muskeln reparieren und aufbauen, mit dem Alter ihre Leistungsfähigkeit? Indem die Autoren einen wichtigen Kontrollschalter in diesen Zellen aufdecken, verweisen sie auf neue Wege, mit denen Medikamente eines Tages altersbedingtem Muskelabbau verlangsamen oder sogar umkehren könnten.
Ein verborgener Schalter in Muskels Stammzellen
Skelettmuskulatur wird ständig von einer kleinen Reserve von Muskels Stammzellen erhalten, die in Ruhe verharren, bis Verletzung oder Bewegung sie aktivieren. Bei älteren Tieren wachen diese Zellen langsamer auf, regenerieren Muskeln weniger effektiv und gehen nach und nach verloren, was zur Sarkopenie, dem altersbedingten Verlust von Muskelmasse und -kraft, beiträgt. Die Forscher konzentrierten sich auf zwei Proteine, deren Spiegel mit dem Alter in vielen Organen verschieben: Nur77, das abnimmt, und Sirt2, das ansteigt. Sie vermuteten, dass diese entgegengesetzten Veränderungen eine gemeinsame Alterungs‑„Achse“ bilden, und prüften ihre Rolle speziell im Skelettmuskel.
Wie Sirt2 Nur77 zermürbt
In Muskels Stammzellen wirkt Nur77 als Genregulator, der mitentscheidet, wann eine ruhende Stammzelle aktiviert werden und mit dem Aufbau neuer Fasern beginnen soll. Das Team fand heraus, dass Sirt2 im Zellkern physisch an Nur77 bindet und kleine Acetylgruppen an einer genauen Stelle von Nur77 chemisch entfernt (eine einzelne Aminosäureposition, K310 bei Mäusen). Wird diese Acetylmarke entfernt, wird Nur77 instabil: Es erhält ein Abbausignal, wird von der zellulären Entsorgungsmaschinerie abgebaut und sein Spiegel sinkt. Ist die Acetylmarke vorhanden, wird Nur77 stabilisiert und kann stärker an die DNA von Zielgenen binden.
Vom molekularen Eingriff zur versagenden Muskelreparatur
Das wichtigste Ziel von Nur77 in diesem Zusammenhang ist Myf5, ein Gen, das Muskels Stammzellen aus tiefer Ruhe in einen reparaturbereiten Zustand schiebt. Die Forscher zeigten, dass acetylierter Nur77 stark an die Kontrollregion von Myf5 bindet und es einschaltet, wodurch die rechtzeitige Aktivierung von Stammzellen und die Bildung neuer Muskelfasern nach Verletzung gefördert wird. Fehlt Nur77 vollständig oder ist die K310‑Stelle dauerhaft deacetyliniert, entwickeln Muskeln kleinere Fasern, regenerieren nach Schäden schlecht und zeigen mehr Narbenbildung. Die Stammzellen teilen sich außerdem weniger günstig und neigen dazu, ihren Bestand zu erschöpfen, anstatt Selbst erneuerung und Differenzierung auszubalancieren. In alten Mäusen, in denen Sirt2 erhöht und Nur77 erniedrigt ist, ist dieses Ungleichgewicht besonders ausgeprägt.
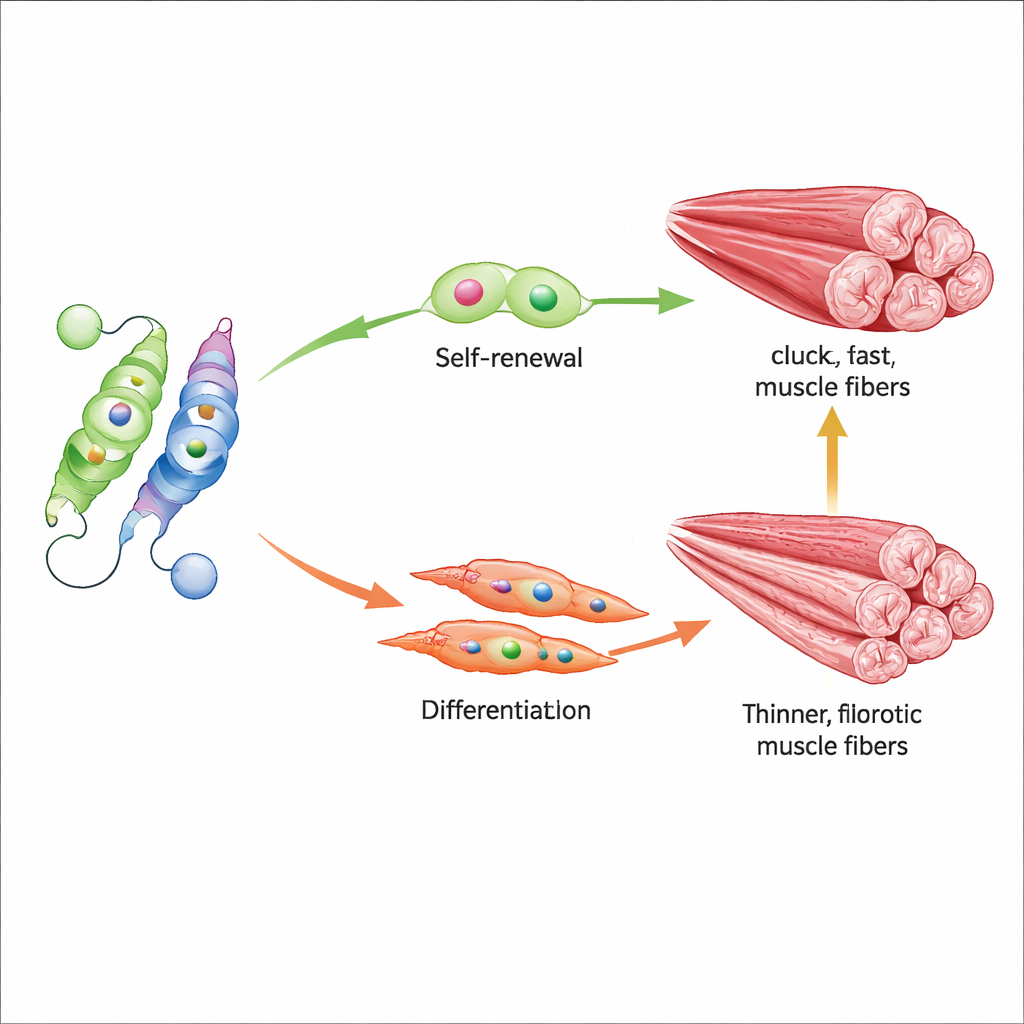
Medikamente, die das Gleichgewicht wieder verschieben
Die Studie testete außerdem zwei kleine Moleküle, die diese molekulare Wippe in entgegengesetzte Richtungen bewegen. AGK2 blockiert Sirt2 und erhält damit indirekt die Acetylmarke auf Nur77 und verhindert dessen Abbau, während CSNB Nur77 direkt aktiviert. Bei alten Mäusen erhöhte die Behandlung mit einem der beiden Wirkstoffe die Nur77‑Aktivität, steigerte Myf5 und frühe muskelaufbauende Proteine und verbesserte messbar Griffkraft und Laufleistung. Auf Gewebeebene erhielten behandelte Muskeln besser schnelle, kraftvolle Fasern und zeigten weniger Fibrose, was nahelegt, dass die Feinabstimmung dieser einzelnen Acetylierungsstelle sowohl das Verhalten der Stammzellen als auch die allgemeine Muskelqualität beeinflussen kann.
Was das für gesundes Altern bedeutet
In der Summe skizziert die Arbeit eine einfache, aber wirkungsvolle Kette von Ereignissen: Mit dem Alter entfernt das ansteigende Sirt2 eine schützende chemische Markierung von Nur77, Nur77 wird instabil und nimmt ab, Schlüsselreparaturgene wie Myf5 sind weniger aktiv, Stammzellen erneuern und reparieren weniger effizient, und Muskeln atrophieren und vernarben allmählich. Durch die Wiederherstellung der acetylierten Form von Nur77 — entweder durch Hemmung von Sirt2 oder durch direkte Stimulierung von Nur77 — konnten die Autoren diese Kette teilweise zurücksetzen und die Muskelfunktion in alten Mäusen verjüngen. Zwar ist noch viel zu tun, bevor solche Strategien sicher beim Menschen angewendet werden können, doch die Studie rückt einen spezifischen molekularen Schalter ins Blickfeld, der eines Tages angegriffen werden könnte, damit Menschen im Alter stärker, mobiler und selbstständiger bleiben.
Zitation: Wang, Y., Yang, Y., Yu, W. et al. The Sirt2–Nur77 axis regulates muscle stem cell quiescence and senescence via epigenetic–metabolic synergy. Cell Death Dis 17, 429 (2026). https://doi.org/10.1038/s41419-026-08645-w
Schlüsselwörter: Muskelsalterung, Muskels Stammzellen, Nur77, Sirt2, Sarkopenie