Clear Sky Science · ja
Sirt2–Nur77軸はエピジェネティクスと代謝の協調を介して筋肉幹細胞の休止と老化を制御する
なぜ筋力は年とともに衰えるのか
年齢とともにこっそり進行するのは、単純な筋力低下です。階段がつらく感じられ、瓶の蓋が開けにくくなり、脚がすぐ疲れる。今回の研究は、その日常的な実感の背後にある根本的な疑問を問い直します。すなわち、通常は筋肉を修復・再生する筋肉幹細胞が加齢とともにどうして機能を失っていくのか。著者らはこれらの細胞内にある重要な制御スイッチを明らかにすることで、将来的に加齢に伴う筋肉量の減少を遅らせたり逆転させたりする薬の手がかりを示しています。
筋肉幹細胞の内部に隠れたスイッチ
骨格筋は、普段は静かに休んでいる少数の筋肉幹細胞の備えによって常に維持されています。損傷や運動があるとこれらの細胞が呼び出されて働きますが、高齢の動物では細胞の応答が遅く、再生能力が低下し、遺失していくため、筋肉量と筋力の加齢性喪失であるサルコペニアに寄与します。研究者らは多くの臓器で加齢に伴って変動する二つのタンパク質に注目しました。すなわち加齢で減少するNur77と増加するSirt2です。彼らはこれらの相反する変化が共通の老化“軸”を形成していると仮定し、骨格筋に特化してその役割を検証しました。
Sirt2がNur77をどのように傷めつけるか
筋肉幹細胞内でNur77は遺伝子制御因子として働き、休止中の幹細胞がいつ活性化して新しい線維を作り始めるかを決める助けをします。研究チームはSirt2が細胞核内でNur77に物理的に結合し、Nur77の特定の位置(マウスではK310と呼ばれる単一のアミノ酸残基)から小さなアセチル基を化学的に除去することを見いだしました。このアセチル修飾が外されるとNur77は不安定になり、細胞の分解系によって破壊されやすくなり、その量が減少します。逆にアセチル化が維持されているとNur77は安定化し、標的遺伝子のDNAにより強く結合できます。
分子レベルの変化から筋修復不全へ
この文脈でNur77の最も重要な標的はMyf5であり、これは筋肉幹細胞を深い休止から修復準備の状態へ押し上げるのに寄与する遺伝子です。研究者らはアセチル化されたNur77がMyf5の制御領域に強く結合してそれを活性化し、損傷後の幹細胞の迅速な活性化と新しい筋線維の形成を促進することを示しました。Nur77が完全に欠損するか、K310部位が脱アセチル化状態に固定されると、筋繊維は小さくなり、損傷後の再生は不良となり、瘢痕化が増えます。幹細胞の分裂様式も好ましくなくなり、自己複製と分化のバランスが崩れてプールが枯渇しやすくなります。Sirt2が高くNur77が低い高齢マウスでは、この不均衡が特に顕著です。
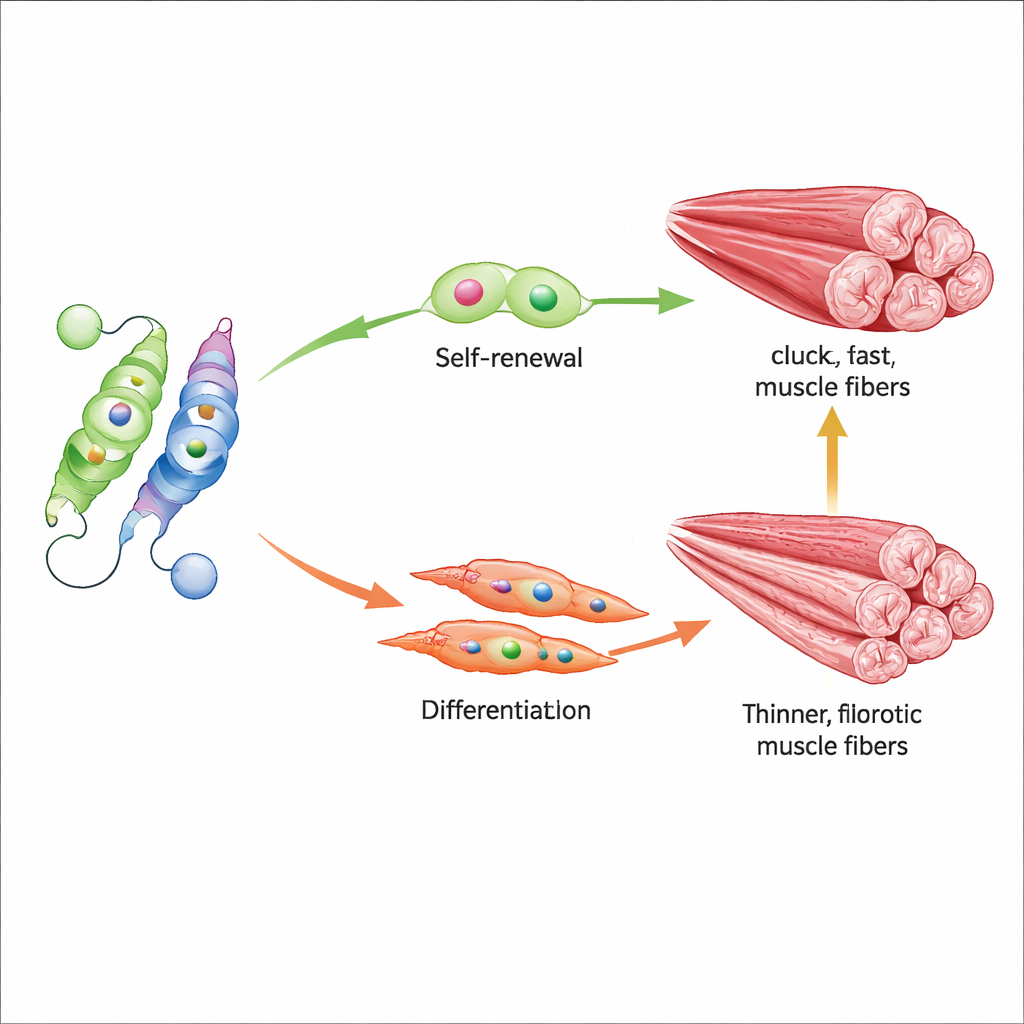
バランスを元に戻す薬剤
研究では分子の天秤を逆方向に傾ける二つの低分子も試しました。AGK2はSirt2を阻害し、間接的にNur77のアセチル基を保持してその破壊を防ぎます。一方CSNBはNur77を直接活性化します。高齢マウスにいずれかの化合物を投与するとNur77の活性が増し、Myf5や初期の筋形成タンパク質が上昇し、握力や走行距離が測定上改善しました。組織レベルでは、処置された筋は速く強力な線維をよりよく維持し、線維化が少なく、単一のアセチル化部位の調整が幹細胞挙動と筋全体の質に影響を与えうることを示唆します。
健康な老化に向けての意義
総じてこの研究はシンプルだが強力な一連の連鎖を描き出します。加齢に伴いSirt2が増加してNur77から保護的な化学的タグが剥がれ、Nur77は不安定化して減少し、Myf5のような重要な修復遺伝子の活性が低下し、幹細胞の更新と修復能が落ち、筋は徐々に萎縮し瘢痕化する。Sirt2を阻害するかNur77を直接刺激してアセチル化された形を回復させることで、著者らはこの連鎖を部分的にリセットし高齢マウスの筋機能を若返らせることができました。こうした戦略がヒトに安全に応用されるまでには多くの課題が残りますが、本研究は将来的に人々がより強く、移動しやすく、より自立した高齢期を保つ助けとなりうる具体的な分子スイッチを示しています。
引用: Wang, Y., Yang, Y., Yu, W. et al. The Sirt2–Nur77 axis regulates muscle stem cell quiescence and senescence via epigenetic–metabolic synergy. Cell Death Dis 17, 429 (2026). https://doi.org/10.1038/s41419-026-08645-w
キーワード: 筋肉の老化, 筋肉幹細胞, Nur77, Sirt2, サルコペニア