Clear Sky Science · es
El eje Sirt2–Nur77 regula la quiescencia y la senescencia de las células madre musculares mediante una sinergia epigenético‑metabólica
Por qué los músculos se debilitan con la edad
El envejecimiento suele manifestarse como una debilidad cotidiana: subir escaleras resulta más difícil, abrir tarros es más complicado y las piernas se cansan con mayor rapidez. Este estudio aborda una pregunta fundamental detrás de esa experiencia diaria: ¿por qué nuestras células madre musculares, que normalmente reparan y reconstruyen el músculo, pierden su eficacia con la edad? Al descubrir un interruptor clave dentro de estas células, los autores señalan nuevas vías por las que fármacos podrían algún día ralentizar o incluso revertir la pérdida muscular asociada a la edad.
Un interruptor oculto dentro de las células madre musculares
El músculo esquelético se mantiene constantemente gracias a una pequeña reserva de células madre musculares que normalmente descansan en silencio hasta que una lesión o el ejercicio las recluta. En animales mayores, estas células se activan más lentamente, regeneran el músculo con menos eficacia y desaparecen gradualmente, lo que contribuye a la sarcopenia, la pérdida de masa y fuerza muscular relacionada con la edad. Los investigadores se centraron en dos proteínas cuyos niveles cambian con la edad en muchos órganos: Nur77, que disminuye, y Sirt2, que aumenta. Sospecharon que estos cambios opuestos forman un “eje” común del envejecimiento y se propusieron comprobar su papel específicamente en el músculo esquelético.
Cómo Sirt2 desgasta a Nur77
En el interior de las células madre musculares, Nur77 actúa como un factor de control génico que ayuda a decidir cuándo una célula madre en reposo debe activarse y comenzar a construir nuevas fibras. El equipo descubrió que Sirt2 se une físicamente a Nur77 en el núcleo celular y le quita químicamente pequeños grupos acetilo en un punto preciso de Nur77 (una única posición de aminoácido denominada K310 en ratones). Cuando se elimina esta marca de acetilación, Nur77 se vuelve inestable: queda etiquetada para su destrucción, es degradada por la maquinaria de eliminación celular y sus niveles caen. Cuando la marca de acetilación está presente, Nur77 se estabiliza y puede unirse al ADN de genes diana con mayor eficacia.
Del ajuste molecular a la falla de la reparación muscular
El objetivo más importante de Nur77 en este contexto es Myf5, un gen que ayuda a impulsar a las células madre musculares desde un reposo profundo hacia un estado listo para reparar. Los investigadores demostraron que Nur77 acetilada se une con fuerza a la región de control de Myf5 y la activa, promoviendo la activación oportuna de las células madre y la formación de nuevas fibras musculares tras una lesión. Cuando Nur77 falta por completo, o cuando el sitio K310 está bloqueado en un estado desacetilado, los músculos desarrollan fibras más pequeñas, se regeneran mal tras el daño y muestran más cicatrización. Las células madre también se dividen de forma menos favorable, tendiendo a agotar su reserva en lugar de equilibrar la autorrenovación con la diferenciación. En ratones envejecidos, donde Sirt2 es más alto y Nur77 más bajo, este desequilibrio es especialmente pronunciado.
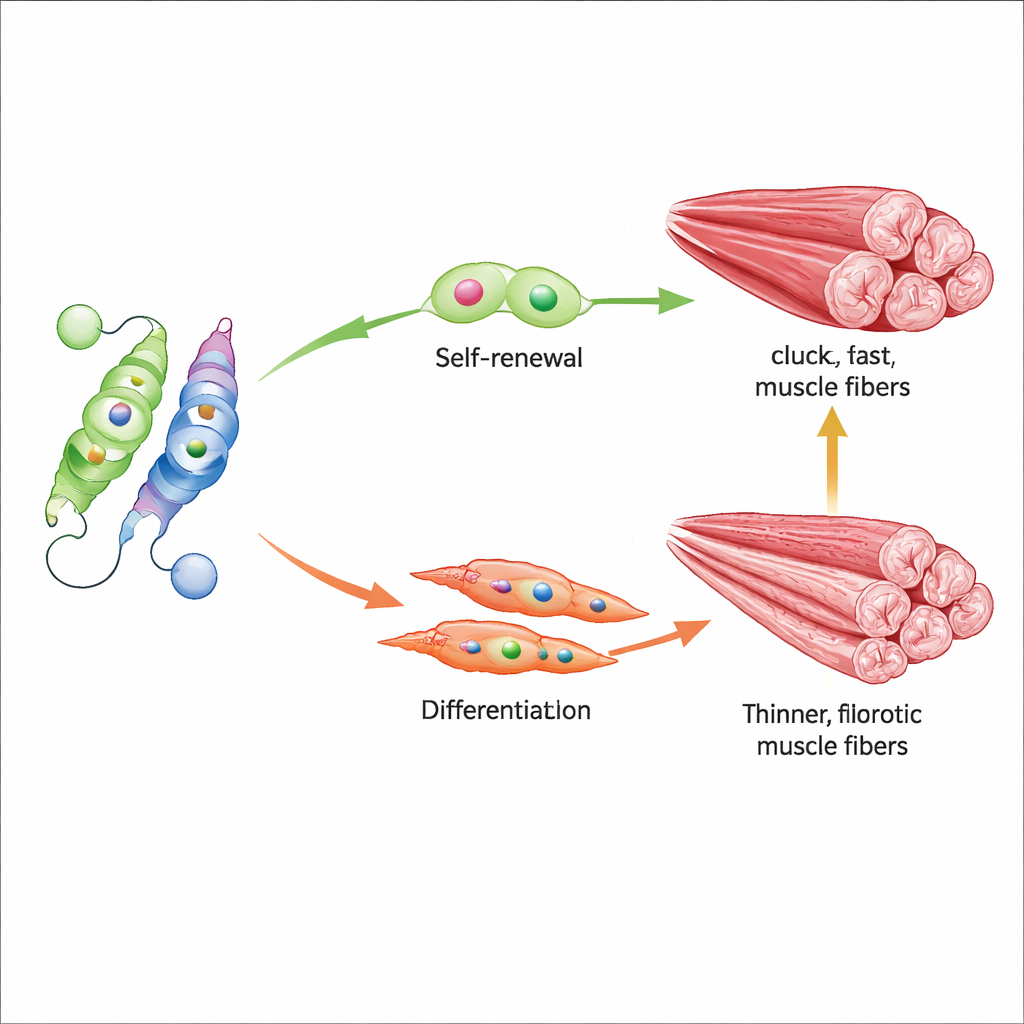
Fármacos que devuelven el equilibrio
El estudio también probó dos pequeñas moléculas que empujan este balancín molecular en direcciones opuestas. AGK2 bloquea Sirt2, preservando indirectamente la marca de acetilación en Nur77 y evitando su destrucción, mientras que CSNB activa Nur77 de forma directa. En ratones viejos, el tratamiento con cualquiera de los compuestos aumentó la actividad de Nur77, elevó Myf5 y las proteínas tempranas implicadas en la construcción muscular, y mejoró de forma mensurable la fuerza de agarre y la distancia recorrida. A nivel tisular, los músculos tratados conservaron mejor las fibras rápidas y potentes y mostraron menos fibrosis, lo que sugiere que ajustar este único sitio de acetilación puede influir tanto en el comportamiento de las células madre como en la calidad muscular global.
Qué significa esto para un envejecimiento saludable
En conjunto, el trabajo describe una cadena de eventos simple pero poderosa: con la edad, el aumento de Sirt2 arranca una etiqueta química protectora de Nur77, Nur77 se vuelve inestable y disminuye, genes clave de reparación como Myf5 están menos activos, las células madre renuevan y reparan con menos eficiencia, y los músculos se atrofian y cicatrizan gradualmente. Al restaurar la forma acetilada de Nur77—ya sea inhibiendo Sirt2 o estimulando directamente Nur77—los autores pudieron reiniciar parcialmente esta cadena y rejuvenecer la función muscular en ratones viejos. Aunque queda mucho por hacer antes de que tales estrategias puedan aplicarse con seguridad en humanos, el estudio pone de relieve un interruptor molecular específico que algún día podría ser objetivo para ayudar a las personas a mantenerse más fuertes, con mayor movilidad y más independientes en la vejez.
Cita: Wang, Y., Yang, Y., Yu, W. et al. The Sirt2–Nur77 axis regulates muscle stem cell quiescence and senescence via epigenetic–metabolic synergy. Cell Death Dis 17, 429 (2026). https://doi.org/10.1038/s41419-026-08645-w
Palabras clave: envejecimiento muscular, células madre musculares, Nur77, Sirt2, sarcopenia