Clear Sky Science · ar
محور Sirt2–Nur77 ينظّم خمود وتقدّم سنّ خلايا جذع العضلات عبر تكامل إبجيني‑تمثيلي
لماذا تضعف العضلات مع التقدم في العمر
غالبًا ما تتسلّل الشيخوخة إلينا على شكل ضعف بسيط: صعود الدرج يصبح أكثر صعوبة، وفتح البرطمانات أصعب، وتتعب الساقان بسرعة أكبر. تطرح هذه الدراسة سؤالًا جوهريًا وراء تلك التجربة اليومية: لماذا تفقد خلايا جذع العضلات، التي عادةً ما تصلح وتعيد بناء العضلات، فعاليتها مع التقدّم في العمر؟ من خلال كشف مفتاح تحكّم رئيسي داخل هذه الخلايا، يشير الباحثون إلى طرق جديدة قد تسمح للأدوية يومًا ما بإبطاء أو حتى عكس فقدان العضلات المرتبط بالعمر.
مفتاح مخفي داخل خلايا جذع العضلات
العضلات الهيكلية تُحافظ عليها باستمرار بواسطة احتياطي صغير من خلايا جذع العضلات التي عادةً ما تبقى ساكنة حتى تستدعيها الإصابة أو التمرين إلى العمل. في الحيوانات الأكبر سنًا، تستيقظ هذه الخلايا ببطء أكبر، وتجدد العضلات بفعالية أقل، وتختفي تدريجيًا، مما يساهم في الساركوبينيا، فقدان الكتلة والقوة العضلية المرتبط بالعمر. ركّز الباحثون على بروتينين تتغير مستوياتهما مع العمر في العديد من الأنسجة: Nur77 الذي ينخفض، وSirt2 الذي يرتفع. شكّوا أن هذه التغيرات المتعاكسة تشكل “محورًا” مشتركًا للشيخوخة وسعوا لاختبار دوره تحديدًا في العضلات الهيكلية.
كيف يضعف Sirt2 دور Nur77
داخل خلايا جذع العضلات، يعمل Nur77 كعامل ضبط للجينات يساعد على تحديد متى يجب على الخلية الجذعية الساكنة أن تنشط وتبدأ في بناء ألياف جديدة. اكتشف الفريق أن Sirt2 يرتبط ماديًا مع Nur77 في نواة الخلية ويزيل كيميائيًا مجموعات أستيل صغيرة من موضع دقيق على Nur77 (موضع حمض أميني واحد يُسمى K310 في الفئران). عند إزالة علامة الأستيل هذه، يصبح Nur77 غير مستقر: يُوسم للتدمير، ويتحلّل بواسطة آليات التخلص من النفايات داخل الخلية، وتنخفض مستوياته. حين توجد علامة الأستيل، يستقر Nur77 ويمكنه الارتباط بحمض نووي محدد للجينات المستهدفة بفعالية أكبر.
من تعديل جزيئي إلى فشل في إصلاح العضلات
أهم هدف لـ Nur77 في هذا السياق هو Myf5، جين يساعد على دفع خلايا جذع العضلات من حالة السكون العميق إلى حالة جاهزة للإصلاح. أظهر الباحثون أن Nur77 المؤستل يرتبط بقوة بمنطقة التحكم في Myf5 ويشغّله، مما يعزّز تنشيط الخلايا الجذعية في الوقت المناسب وتكوين ألياف عضلية جديدة بعد الإصابة. عندما يغيب Nur77 تمامًا، أو عندما يُقفل موضع K310 في حالة منزوعة الأستلة، تتطور العضلات بألياف أصغر، وتتجدّد بشكل أضعف بعد التلف، وتظهر تندبًا أكثر. كما تنقسم الخلايا الجذعية بطريقة أقل ملاءمة، ما يؤدي إلى استنزاف احتياطيها بدلًا من موازنة التجدد الذاتي مع التمايز. في الفئران المسنة حيث يرتفع Sirt2 وينخفض Nur77، يكون هذا الخلل أكثر وضوحًا.
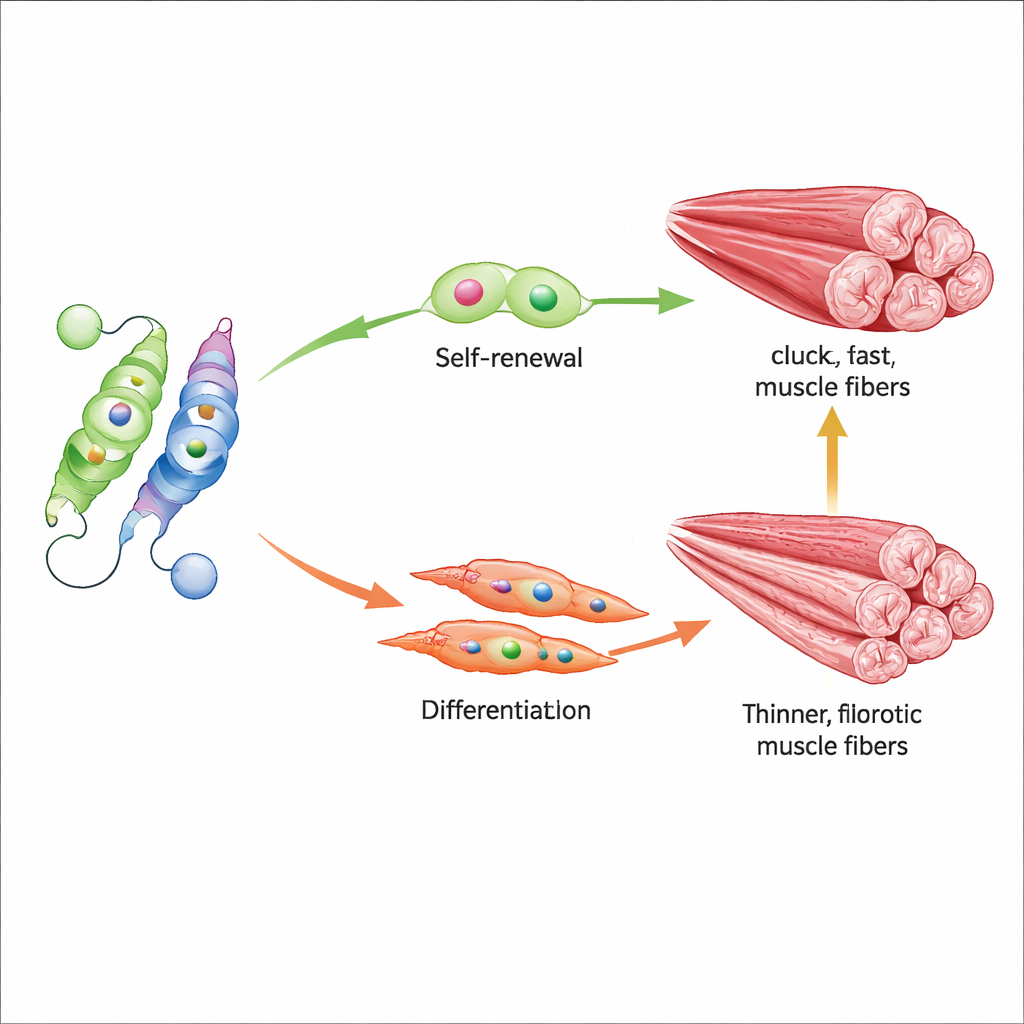
أدوية تضبط الميزان مرة أخرى
اختبرت الدراسة أيضًا جزيئين صغيرين يدفعان هذا الميزان الجزيئي في اتجاهين متعاكسين. يثبط AGK2 عمل Sirt2، محافظًا بشكل غير مباشر على علامة الأستيل على Nur77 وممنعًا تكسيره، بينما ينشّط CSNB Nur77 مباشرةً. في الفئران المسنة، أدى العلاج بأي من المركبين إلى زيادة نشاط Nur77، وتعزيز Myf5 والبروتينات المبكرة المسؤولة عن بناء العضلات، وتحسّن ملحوظ في قوة الإمساك ومسافة الجري. على مستوى النسيج، حافظت العضلات المعالجة على ألياف سريعة وقوية بشكل أفضل وأظهرت تليفًا أقل، ما يوحي بأن تعديل موضع الأستلة هذا يمكن أن يؤثر في سلوك الخلايا الجذعية وجودة العضلات عمومًا.
ما الذي يعنيه هذا لصحة الشيخوخة
توضح النتائج مجتمعة سلسلة بسيطة لكنها قوية من الأحداث: مع التقدّم في العمر، يزيل ارتفاع Sirt2 وسمًا كيميائيًا واقيًا من Nur77، فيصبح Nur77 غير مستقر وينخفض، وتصبح جينات الإصلاح الأساسية مثل Myf5 أقل نشاطًا، وتتجدّد الخلايا الجذعية وتصلح بشكل أقل كفاءة، وتضمحل العضلات تدريجيًا وتتشوّه بتندّب. من خلال استعادة الشكل المؤستل من Nur77 — إما عن طريق تثبيط Sirt2 أو تحفيز Nur77 مباشرة — استطاع الباحثون إعادة ضبط هذه السلسلة جزئيًا وتجديد وظيفة العضلات في الفئران المسنة. وعلى الرغم من أن الكثير لا يزال مطلوبًا قبل أن تُطبق مثل هذه الاستراتيجيات بأمان على البشر، تبرز الدراسة مفتاحًا جزيئيًا محددًا قد يكون يومًا ما هدفًا للمساعدة في بقاء الناس أقوى وأكثر قدرة على الحركة وأكثر استقلالية في مراحل الحياة المتأخرة.
الاستشهاد: Wang, Y., Yang, Y., Yu, W. et al. The Sirt2–Nur77 axis regulates muscle stem cell quiescence and senescence via epigenetic–metabolic synergy. Cell Death Dis 17, 429 (2026). https://doi.org/10.1038/s41419-026-08645-w
الكلمات المفتاحية: شيخوخة العضلات, خلايا جذع العضلات, Nur77, Sirt2, ضمور العضلات المرتبط بالعمر