Clear Sky Science · it
L’asse Sirt2–Nur77 regola la quiescenza e la senescenza delle cellule staminali muscolari tramite sinergia epigenetica‑metabolica
Perché i muscoli si indeboliscono con l’età
L’invecchiamento spesso si manifesta con una debolezza semplice e subdola: salire le scale diventa più faticoso, i vasetti sono più difficili da aprire e le gambe si stancano più rapidamente. Questo studio indaga una domanda fondamentale dietro questa esperienza quotidiana: perché le nostre cellule staminali muscolari, che normalmente riparano e ricostruiscono il muscolo, perdono efficienza con l’età? Scoprendo un interruttore di controllo chiave all’interno di queste cellule, gli autori indicano nuove strade attraverso cui i farmaci potrebbero un giorno rallentare o addirittura invertire la perdita muscolare legata all’età.
Un interruttore nascosto nelle cellule staminali muscolari
Il muscolo scheletrico è continuamente mantenuto da una piccola riserva di cellule staminali muscolari che normalmente restano in uno stato di riposo finché un danno o l’esercizio non le richiamano all’azione. Negli animali anziani queste cellule si attivano più lentamente, rigenerano il muscolo meno efficacemente e scompaiono gradualmente, contribuendo alla sarcopenia, la perdita di massa e forza muscolare legata all’età. I ricercatori si sono concentrati su due proteine i cui livelli cambiano con l’età in molti organi: Nur77, che diminuisce, e Sirt2, che aumenta. Hanno ipotizzato che questi cambiamenti opposti costituiscano un “asse” dell’invecchiamento e hanno voluto testarne il ruolo specifico nel muscolo scheletrico.
Come Sirt2 indebolisce Nur77
All’interno delle cellule staminali muscolari, Nur77 agisce come un fattore di controllo genico che aiuta a decidere quando una cellula staminale in riposo deve attivarsi e iniziare a costruire nuove fibre. Il gruppo ha scoperto che Sirt2 si lega fisicamente a Nur77 nel nucleo cellulare e rimuove chimicamente piccoli gruppi acetilici da un punto preciso di Nur77 (una singola posizione aminoacidica chiamata K310 nei topi). Quando questo marchio acetilico viene rimosso, Nur77 diventa instabile: viene etichettato per la distruzione, degradato dal sistema di smaltimento cellulare e i suoi livelli diminuiscono. Quando il marchio acetilico è presente, Nur77 è stabilizzato e può legare il DNA dei geni target in modo più efficace.
Da una modifica molecolare a una riparazione muscolare fallimentare
Il bersaglio più importante di Nur77 in questo contesto è Myf5, un gene che aiuta a spingere le cellule staminali muscolari dallo stato di riposo profondo a uno stato pronto per la riparazione. I ricercatori hanno mostrato che Nur77 acetilato lega con forza la regione di controllo di Myf5 e la attiva, promuovendo l’attivazione tempestiva delle staminali e la formazione di nuove fibre muscolari dopo l’infortunio. Quando Nur77 manca del tutto, o quando il sito K310 è bloccato in uno stato de‑acetilato, i muscoli sviluppano fibre più piccole, rigenerano male dopo il danno e mostrano più cicatrizzazione. Anche le cellule staminali si dividono in modo meno favorevole, tendendo a esaurire la loro riserva invece di bilanciare auto‑rinnovamento e differenziazione. Nei topi anziani, dove Sirt2 è più alto e Nur77 più basso, questo squilibrio è particolarmente pronunciato.
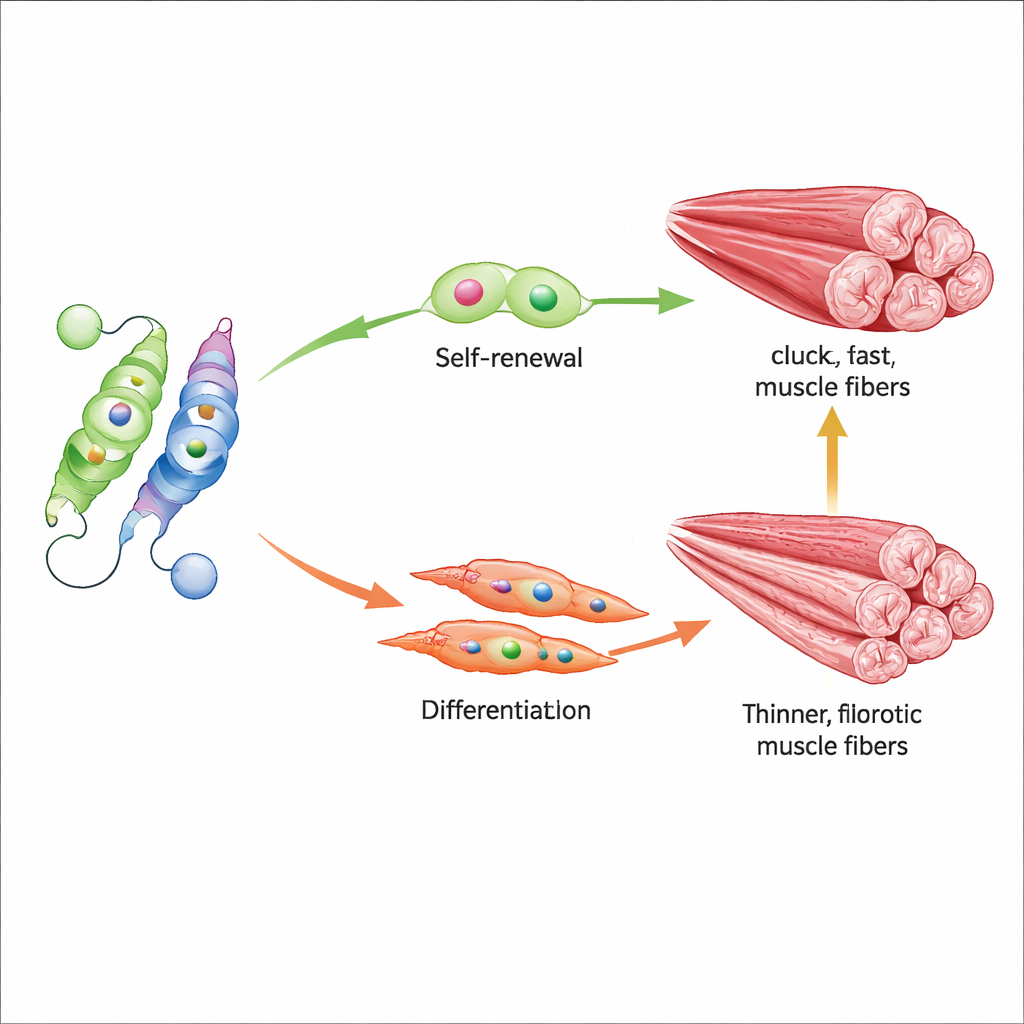
Farmaci che spostano di nuovo l’equilibrio
Lo studio ha anche testato due piccole molecole che spingono questa bilancia molecolare in direzioni opposte. AGK2 blocca Sirt2, preservando indirettamente il marchio acetilico su Nur77 e impedendone la distruzione, mentre CSNB attiva direttamente Nur77. Nei topi vecchi, il trattamento con ciascuno dei due composti ha aumentato l’attività di Nur77, potenziato Myf5 e le proteine precoci della costruzione muscolare, e migliorato in modo misurabile la forza di presa e la distanza di corsa. A livello tissutale, i muscoli trattati mantenevano meglio le fibre rapide e potenti e mostravano meno fibrosi, suggerendo che modulare questo singolo sito di acetilazione può influenzare sia il comportamento delle cellule staminali sia la qualità complessiva del muscolo.
Cosa significa per un invecchiamento sano
Nel complesso, il lavoro delinea una catena di eventi semplice ma potente: con l’età, l’aumento di Sirt2 rimuove un tag chimico protettivo da Nur77, Nur77 diventa instabile e diminuisce, geni chiave per la riparazione come Myf5 sono meno attivi, le cellule staminali si rinnovano e riparano meno efficacemente e i muscoli si atrofizzano e cicatrizzano progressivamente. Ripristinando la forma acetilata di Nur77—sia inibendo Sirt2 sia stimolando direttamente Nur77—gli autori sono riusciti a reimpostare parzialmente questa catena e ringiovanire la funzione muscolare in topi anziani. Pur restando molto da fare prima che tali strategie possano essere applicate in sicurezza negli esseri umani, lo studio mette in luce un interruttore molecolare specifico che un giorno potrebbe essere mirato per aiutare le persone a rimanere più forti, più mobili e più indipendenti nella vita avanzata.
Citazione: Wang, Y., Yang, Y., Yu, W. et al. The Sirt2–Nur77 axis regulates muscle stem cell quiescence and senescence via epigenetic–metabolic synergy. Cell Death Dis 17, 429 (2026). https://doi.org/10.1038/s41419-026-08645-w
Parole chiave: invecchiamento muscolare, cellule staminali muscolari, Nur77, Sirt2, sarcopenia