Clear Sky Science · zh
通过YAP与IGF2通路协同作用,生成具有多极结构的增殖性hESC来源葡萄簇状肝细胞类器官,作为再生对应物
在实验室构建微型肝脏
肝脏在体内默默承担着许多艰巨任务——解毒药物、处理营养物质并管理脂肪与糖类。然而,人类肝组织稀缺,成熟肝细胞在培养皿中很快丧失功能。本研究描述了一种从胚胎干细胞生长出类似葡萄串的微小人肝细胞簇的方法,这些簇不仅能在体外存活并分裂数周,还能复制真实肝组织的关键特征,包括以高度有序的方式运输胆汁和其他物质的能力。
为何肝细胞簇很重要
科学家长期希望构建能像真实肝组织一样工作的三维“类器官”。现有由胆管细胞制成的类器官往往形成中空囊泡,表现为简单的内外极性,这与真实肝细胞的复杂结构不符。在体内,每个肝细胞具有多个“顶端”表面,与相邻细胞连接形成分枝的胆小管网络,同时在其相对侧与血液交换物质。由成体供体肝细胞衍生的葡萄状肝细胞类器官能够模拟这种多极形态与功能,但它们依赖于稀缺且差异较大的供体组织。新研究表明,可以从人胚胎干细胞产生类似的葡萄簇状类器官,提供一种更充足和标准化的来源。
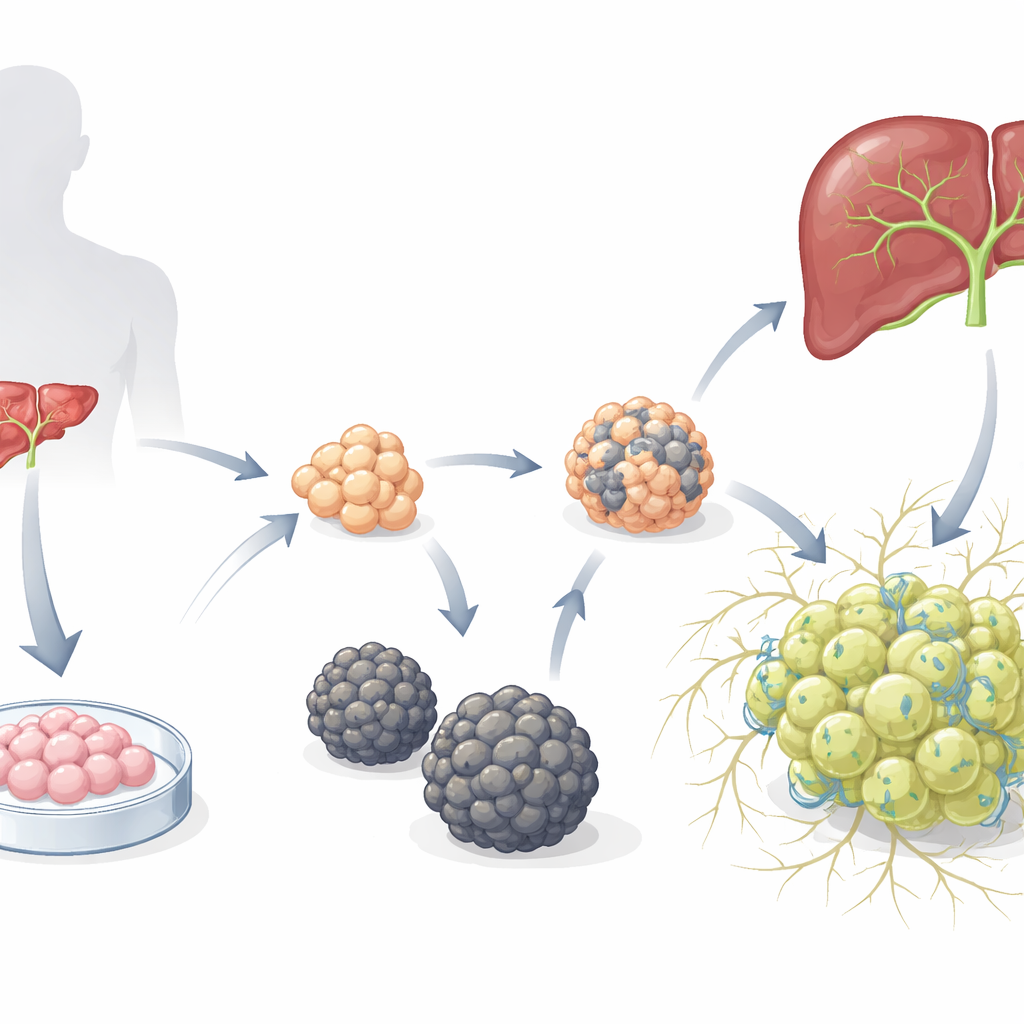
两类截然不同的迷你肝群落
研究者从先前建立的肝芽细胞类器官——由人胚胎干细胞培养得到的未成熟肝前体——开始,并将它们置于有利于肝细胞分化的培养基中。随着时间推移,出现了两种不同类型的类器官。一类形成平滑的球体(S-heporgs),生长欠佳,表现出衰老和细胞死亡迹象,且未能组织出正常的胆小管网络。另一类形成不规则的葡萄状簇(G-heporgs),可扩展到数百微米,包含大量分裂和双核细胞,高表达白蛋白等成熟肝蛋白,并在细胞间构建复杂的分枝管状结构。基因与功能测试表明,G-heporgs在代谢上活跃且具有增殖能力,而S-heporgs则停滞于衰老或损伤样状态。
炎性信号、生长因子与再生开关
一个意外发现是,失败的S-heporgs似乎有助于更成功的G-heporgs的出现。随着S-heporgs老化,它们释放炎性分子并创造出类似受损肝脏的微环境。在这种环境下,G-heporgs激活了以因子IGF2及其受体为中心的生长程序,进而启动已知驱动细胞分裂的PI3K–AKT信号通路。向培养体系中补充额外的IGF2可增加G-heporgs的数量和体积,而阻断其受体或下游信号则几乎消除了这些类器官。与此同时,G-heporgs显示出YAP的强烈激活——一种感应机械和损伤信号、对肝脏损伤后再生至关重要的蛋白。当团队用小分子激动剂人为上调YAP活性时,类器官可在不丧失葡萄状结构的情况下扩增超过两个月并多代传代;关闭YAP则显著抑制生长。
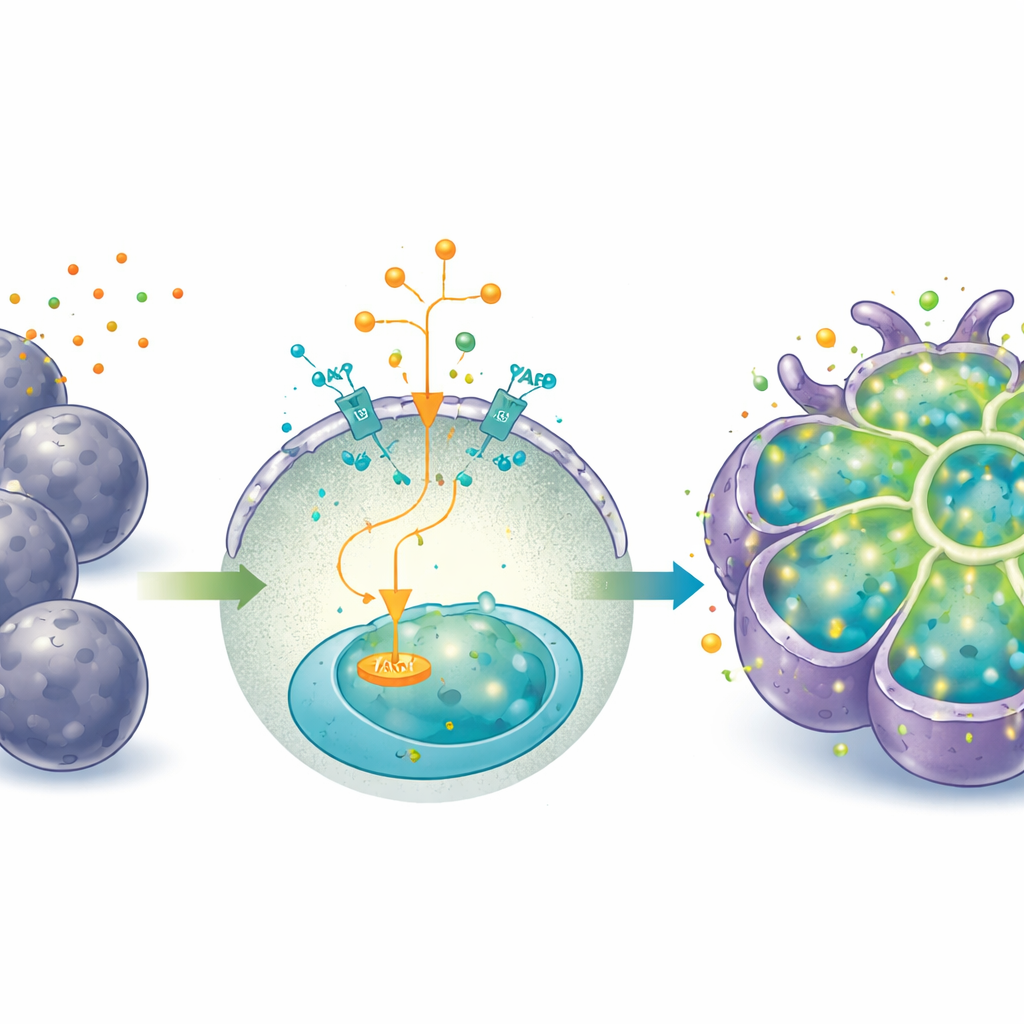
从生长模式到执行模式
尽管持续的YAP激活有利于扩增,但会使细胞保持较为胎儿化、前体样的状态,并抑制部分成熟肝功能。为将类器官从“生长模式”转向“执行模式”,研究者调整了培养基——去除IGF2、YAP激动剂与Wnt激活剂,加入激素地塞米松与细胞因子肿瘤坏死因子M(oncostatin M)。在这些条件下,类器官发育出更大的多边形细胞、较低的核质比和更多双核细胞,这些都是肝细胞成熟的标志。它们产生更多白蛋白与尿素,能将示踪染料(吲哚菁绿)进出细胞,并在暴露于已知酶诱导剂后显著增加关键药物代谢酶的表达。
重现胆汁流动与金属处理
这些类器官的核心成就是能够重建极性运输——即将物质定向移动到细胞特定表面的能力。可扩增的G-heporgs形成由正常在顶端膜富集的蛋白标记的胆小管样通道。活体成像显示荧光测试化合物被泵入这些微小腔道,而在患者中已知会导致胆汁淤积的药物破坏了该管网并导致染料在细胞内积聚,极其类似临床毒性反应。团队还追踪了铜转运蛋白ATP7B(在威尔逊病中突变),发现其在高铜刺激下从细胞内区室迁移到面向胆汁的表面及类溶酶体结构,正如在原生肝组织中观察到的那样。这说明这些类器官能够模拟肝细胞如何以极性方式处理金属及其他分子。
这对未来肝脏研究意味着什么
通过利用IGF2与YAP通路的协同作用,作者们创造出一种可再生的人肝细胞类器官来源,这些类器官组装成葡萄状簇并构建功能性胆小管网络。尽管它们在成熟度上仍略逊于成人肝组织且缺乏非肝细胞的支持细胞,但这些结构捕捉了肝再生、极性与运输的关键方面。对于非专业读者而言,这意味着科学家离体外培养的迷你肝更近了一步——这些迷你肝可用于研究遗传性肝病、测试药物安全性(尤其是与胆汁相关的毒性),并最终探索基于细胞的治疗方案,而无需完全依赖有限的供体器官。
引用: Wu, H., Liu, S., Chen, S. et al. Generation of proliferative hESC-derived grape-clustered hepatocyte organoids with multipolar architecture as regenerative counterpart via synergy of YAP and IGF2 pathways. Cell Death Dis 17, 381 (2026). https://doi.org/10.1038/s41419-026-08635-y
关键词: 肝类器官, 干细胞衍生肝细胞, 胆小管, 肝再生, 药物诱导的肝损伤