Clear Sky Science · es
Generación de organoides hepáticos en racimo tipo uva proliferativos derivados de hESC con arquitectura multipolar como contraparte regenerativa mediante la sinergia de las vías YAP e IGF2
Construyendo hígados diminutos en el laboratorio
El hígado se ocupa discretamente de muchas de las tareas más complejas del organismo: detoxificar fármacos, procesar nutrientes y gestionar grasas y azúcares. Sin embargo, el tejido hepático humano es escaso y las células hepáticas maduras pierden rápidamente su funcionalidad en cultivo. Este estudio describe un método para cultivar diminutos racimos de células hepáticas humanas, semejantes a uvas, a partir de células madre embrionarias que no solo sobreviven y se dividen durante semanas, sino que también reproducen rasgos clave del tejido hepático real, incluida la capacidad de mover la bilis y otras sustancias de forma altamente organizada.
Por qué importan los racimos de células hepáticas
Los científicos llevan tiempo buscando construir “organoides” hepáticos tridimensionales que se comporten como tejido hepático auténtico. Los organoides existentes derivados de células del conducto biliar tienden a formar quistes huecos con una polaridad simple de dentro hacia fuera, lo que no coincide con la estructura compleja de los hepatocitos verdaderos. En el organismo, cada hepatocito posee varias superficies apicales que se unen con las de las células vecinas para formar una red ramificada de canalículos biliares mientras intercambia sustancias con la sangre por su cara opuesta. Los organoides en racimo tipo uva obtenidos de hepatocitos adultos primarios pueden imitar esta forma y función multipolar, pero dependen de tejido donante que es limitado y variable. El nuevo trabajo muestra que organoides similares en racimo pueden producirse a partir de células madre embrionarias humanas, lo que ofrece una fuente potencialmente más abundante y estandarizada.
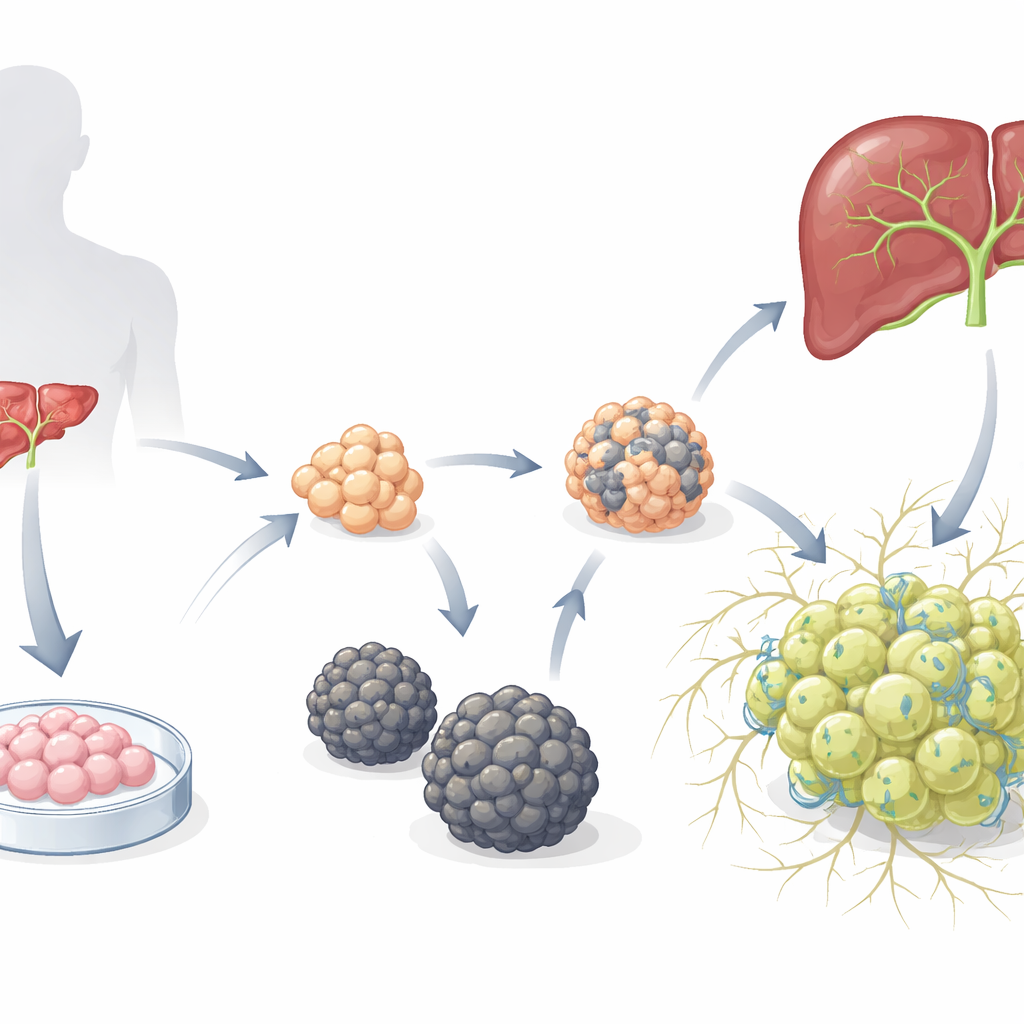
Dos comunidades de mini-hígado muy distintas
Los investigadores partieron de organoides de hepatoblastos ya establecidos —progenitores hepáticos inmaduros derivados de células madre embrionarias humanas— y los colocaron en un medio diseñado para favorecer el desarrollo de hepatocitos. Con el tiempo emergieron dos tipos distintos de organoides. Un tipo formó esferas lisas (S-heporgs) que crecían mal, mostraban signos de envejecimiento y muerte celular, y no lograban organizar una red adecuada de canalículos biliares. El otro tipo formó racimos irregulares semejantes a uvas (G-heporgs) que se expandían hasta varios cientos de micrómetros, contenían muchas células en división y binucleadas, expresaban altos niveles de proteínas hepáticas maduras como la albúmina y construían estructuras canaliculares ramificadas entre células. Pruebas genéticas y funcionales mostraron que los G-heporgs eran metabólicamente activos y proliferativos, mientras que los S-heporgs estaban atrapados en un estado senescente, similar al de tejido lesionado.
Señales inflamatorias, factores de crecimiento y un interruptor regenerativo
Un giro inesperado fue que los S-heporgs fallidos parecían ayudar a la aparición de los G-heporgs más exitosos. A medida que los S-heporgs envejecían, liberaban moléculas inflamatorias y creaban un microambiente que recordaba a un hígado dañado. En este contexto, los G-heporgs activaron un programa de crecimiento centrado en el factor IGF2 y su receptor, que a su vez implicó la vía de señalización PI3K–AKT, conocida por impulsar la división celular. Añadir IGF2 extra al cultivo aumentó tanto el número como el tamaño de los G-heporgs, mientras que bloquear su receptor o la señalización aguas abajo casi los eliminó. Al mismo tiempo, los G-heporgs mostraron una fuerte activación de YAP, una proteína que percibe señales mecánicas y de lesión y que es crucial para la regeneración hepática tras el daño. Cuando el equipo aumentó artificialmente la actividad de YAP con un agonista de pequeña molécula, los organoides pudieron expandirse durante más de dos meses y múltiples pasajes sin perder su arquitectura en racimo; apagar YAP redujo drásticamente el crecimiento.
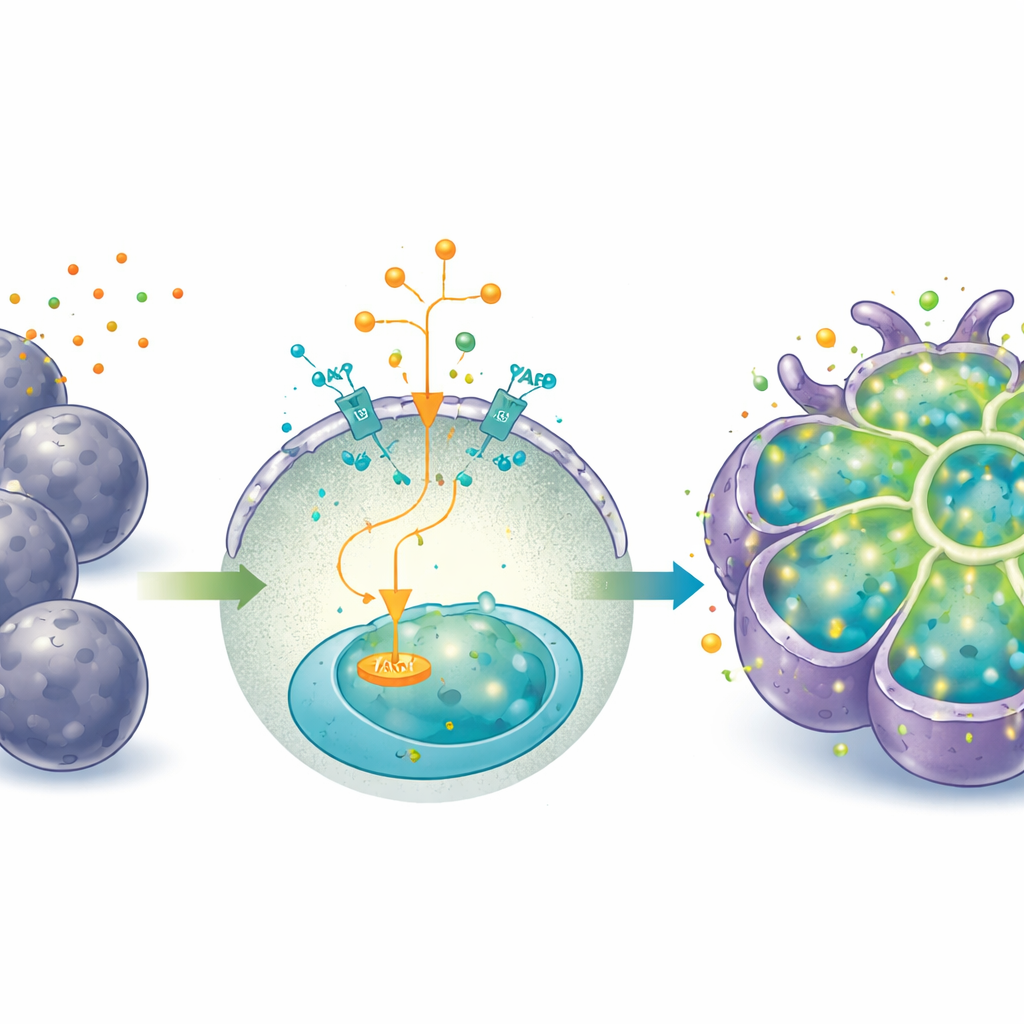
Del modo crecimiento al modo trabajo
La activación prolongada de YAP, aunque excelente para la expansión, mantenía a las células en un estado más fetal y progenitor y atenúaba algunas funciones hepáticas maduras. Para desplazar los organoides de “modo crecimiento” a “modo trabajo”, los investigadores modificaron el medio: retiraron IGF2, el agonista de YAP y un activador de Wnt, y añadieron la hormona dexametasona y la citocina oncostatina M. Bajo estas condiciones, los organoides desarrollaron células más grandes y poligonales con menor proporción núcleo/citoplasma y más células binucleadas, caracteres típicos de hepatocitos en maduración. Produjeron más albúmina y urea, manejaronn un tinte modelo (indocianina verde) entrando y saliendo de las células, e incrementaron enzimas clave metabolizadoras de fármacos, sobre todo tras la exposición a inductores enzimáticos conocidos.
Recrear el flujo biliar y el manejo de metales
Un logro central de estos organoides es su capacidad para recrear el transporte polarizado: el movimiento dirigido de sustancias hacia superficies celulares específicas. Los G-heporgs expandibles formaron canales semejantes a canalículos biliares marcados por proteínas que normalmente se concentran en membranas apicales. La imagen en vivo mostró compuestos fluorescentes de prueba siendo bombeados hacia esos pequeños lúmenes, y fármacos conocidos por causar colestasis en pacientes dañaron esta red canalicular y provocaron que los tintes se acumularan dentro de las células, reproduciendo de forma cercana los efectos tóxicos observados en la clínica. El equipo también rastreó ATP7B, un transportador de cobre mutado en la enfermedad de Wilson, y encontró que en respuesta a altas concentraciones de cobre se desplazó desde compartimentos internos hacia las superficies orientadas a la bilis y hacia estructuras parecidas a lisosomas, tal como ocurre en el hígado nativo. Esto demuestra que los organoides pueden modelar cómo los hepatocitos dirigen metales y otras moléculas de forma polarizada.
Qué significa esto para la investigación hepática futura
Al aprovechar la acción combinada de las vías IGF2 y YAP, los autores crearon una fuente renovable de organoides de hepatocitos humanos que se ensamblan en racimos tipo uva y construyen redes funcionales de canalículos biliares. Aunque todavía algo menos maduros que el tejido hepático adulto y sin células de soporte no hepatocíticas, estas estructuras capturan aspectos clave de la regeneración, la polaridad y el transporte hepáticos. Para el público general, esto significa que los científicos están más cerca de mini-hígados cultivados en laboratorio que pueden usarse para estudiar enfermedades hepáticas hereditarias, evaluar la seguridad de fármacos —especialmente la toxicidad relacionada con la bilis— y, eventualmente, explorar terapias celulares, todo ello sin depender exclusivamente de órganos donantes escasos.
Cita: Wu, H., Liu, S., Chen, S. et al. Generation of proliferative hESC-derived grape-clustered hepatocyte organoids with multipolar architecture as regenerative counterpart via synergy of YAP and IGF2 pathways. Cell Death Dis 17, 381 (2026). https://doi.org/10.1038/s41419-026-08635-y
Palabras clave: organoides hepáticos, hepatocitos derivados de células madre, canalículos biliares, regeneración hepática, lesión hepática inducida por fármacos