Clear Sky Science · he
ייצור אאורונואידים כבדיים מקובצים כענבים, נגזרים מ-hESC ומתאפיינים בארכיטקטורה מולטיפולרית כפסיל שיקומי באמצעות סינרגיה של מסלולי YAP ו-IGF2
בניית כבדונים זעירים במעבדה
הכבד מטפל בשקט ברבים מהמשימות הקשות של הגוף — פירוק רעלים, עיבוד חומרים מזינים וניהול שומנים וסוכרים. בכל זאת, רקמת כבד אנושית נדירה, ותאי כבד בוגרים מאבדים מהר את תפקודם בתרבית. מחקר זה מתאר שיטה לגדל צברי תאים כבדיים קטנים, דמויי-ענבים, מתוך תאי גזע עובריים אנושיים, שאינם רק שורדים ומתחלקים למשך שבועות, אלא משחזרים תכונות מרכזיות של רקמת כבד אמיתית, כולל היכולת להזיז מרה וחומרים אחרים בצורה מתואמת ומאורגנת.
מדוע צברי תאי כבד חשובים
מדענים מקווים מאז ומעולם לבנות "אורגנואידים" תלת-ממדיים של כבד המתנהגים כמו רקמת כבד אמיתית. אורגנואידים קיימים שמקורם בתאי דרכי המרה נוטים ליצור ציסטות חלולות עם קוטביות פשוטה של פנים–חוץ, שאינה תואמת את המבנה המורכב של ההפטוציט האמיתי. בגוף, לכל הפטוציט יש מספר משטחים אפיקליים שמתחברים לשכניו ויוצרים רשת תעלות מרה מסתעפת תוך כדי חילוף חומרים עם הדם בצדם הנגדי. אורגנואידים דמויי-ענבים הנגזרים מתאי כבד מבוגרים ראשוניים מסוגלים לחקות את הצורה והמולטי-פולריות הזו, אך הם תלויים ברקמת תורם שהיא מוגבלת ומשתנה. העבודה החדשה מראה שאותם אורגנואידים מקובצים דמויי-ענבים ניתנים לייצור גם מתאי גזע עובריים אנושיים, ומציעה מקור פוטנציאלי שופע ומאוחד יותר.
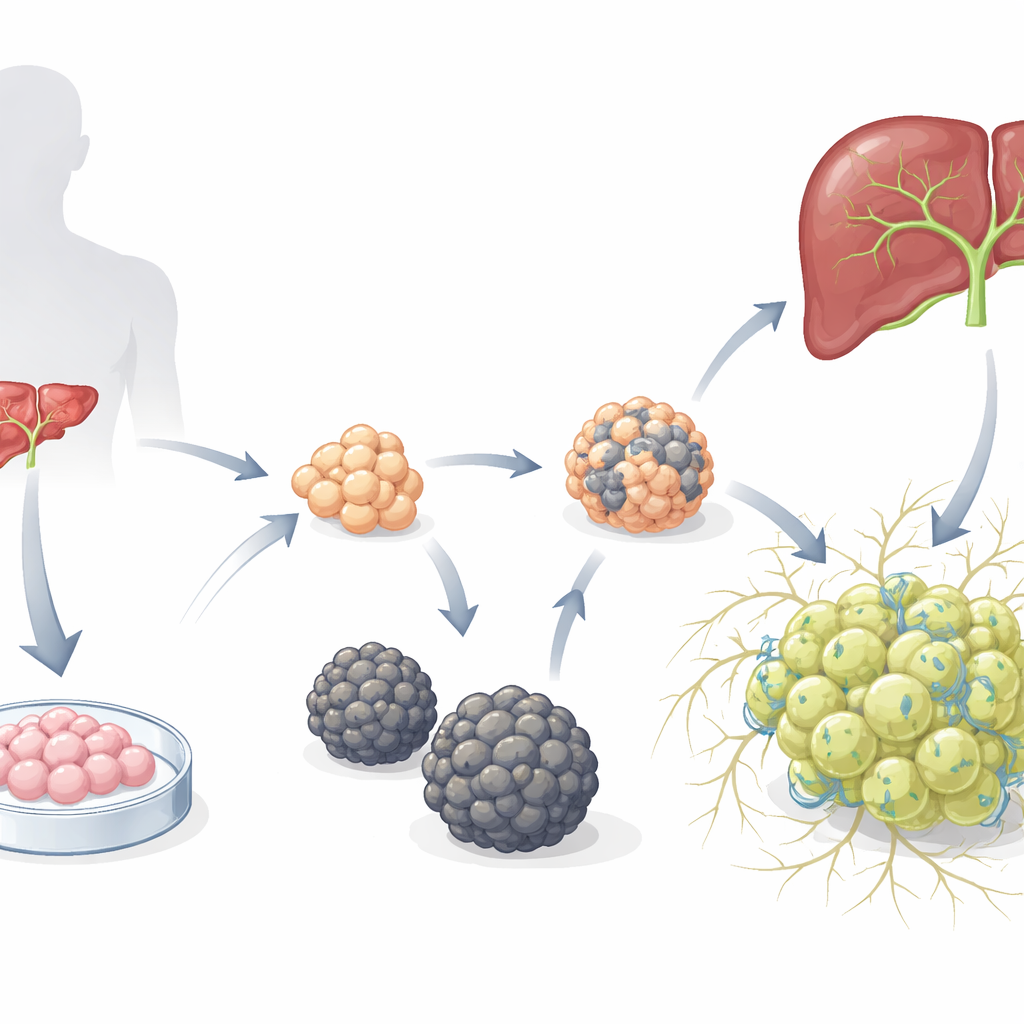
שתי קהילות מיני-כבד שונות מאוד
החוקרים התחילו מאורגנואידים של הפטובלסט שהתפתחו קודם לכן — פרו-מתאי כבד בלתי בוגרים שגודלו מתאי גזע עובריים אנושיים — והניחו אותם בתווך שנועד להטות לפיתוח ההפטוציט. עם הזמן הופיעו שני סוגים מובחנים של אורגנואידים. סוג אחד יצר כדורים חלקים (S-heporgs) שגדלו בקושי, הראו סימני הזדקנות ותמותה תאית וכשלו בארגון רשת תעלות מרה תקינה. הסוג האחר יצר צברים לא סדירים, דמויי-ענבים (G-heporgs) שהתרחבו לעשרות עד כמה מאות מיקרומטרים, הכילו תאים רבים במצב חלוקה ובעלי גרעינים כפולים, הביטוי של חלבוני כבד בוגרים כגון אלבומין היה גבוה, ובנו מבנים מסתעפים מורכבים של תעלות בין תאים. מבחנים גנטיים ותפקודיים הראו ש-G-heporgs היו מטבולית פעילות ומתחלקת, בעוד S-heporgs נותרו במצב של סנצטנציה (הזדקנות) ודמיון לפציעה.
אותות דלקתיים, גורמי גדילה ומתג השחזור
פיתול מפתיע היה שה-S-heporgs הכושלים נראו מאיצים את הופעת ה-G-heporgs המוצלחים יותר. ככל ש-S-heporgs הזדקנו, הם שחררו מולקולות דלקת ויצרו מיקרו-סביבה הדומה לכבד פגוע. בסביבה זו, ה-G-heporgs הפעילו תוכנית גדילה הממוקדת בגורם IGF2 וקולטן שלו, שהפעילו בתורם את מסלול ה-PI3K–AKT הידוע כמניע חלוקה תאית. תוספת של IGF2 לתרבית הגדילה גם את מספר וגודל ה-G-heporgs, בעוד שחסימת הקולטן או איתות מטה-זרימתית כמעט מחקה אותם. במקביל הופעלה ב-G-heporgs פעילות חזקה של YAP, חלבון החוש בהקשרים מכניים ובנזק והוא קריטי לגדילה מחדש של הכבד אחרי פציעה. כאשר הצוות הגביר באופן מלאכותי את פעילות YAP בעזרת אגוניסט מולקולרי קטן, האורגנואידים היו ניתנים להתרחבות ליותר מחודשיים ולעברות רבות בלי לאבד את הארכיטקטורה הדמויה-ענב; כיבוי YAP צמצם את הגדילה בצורה חדה.
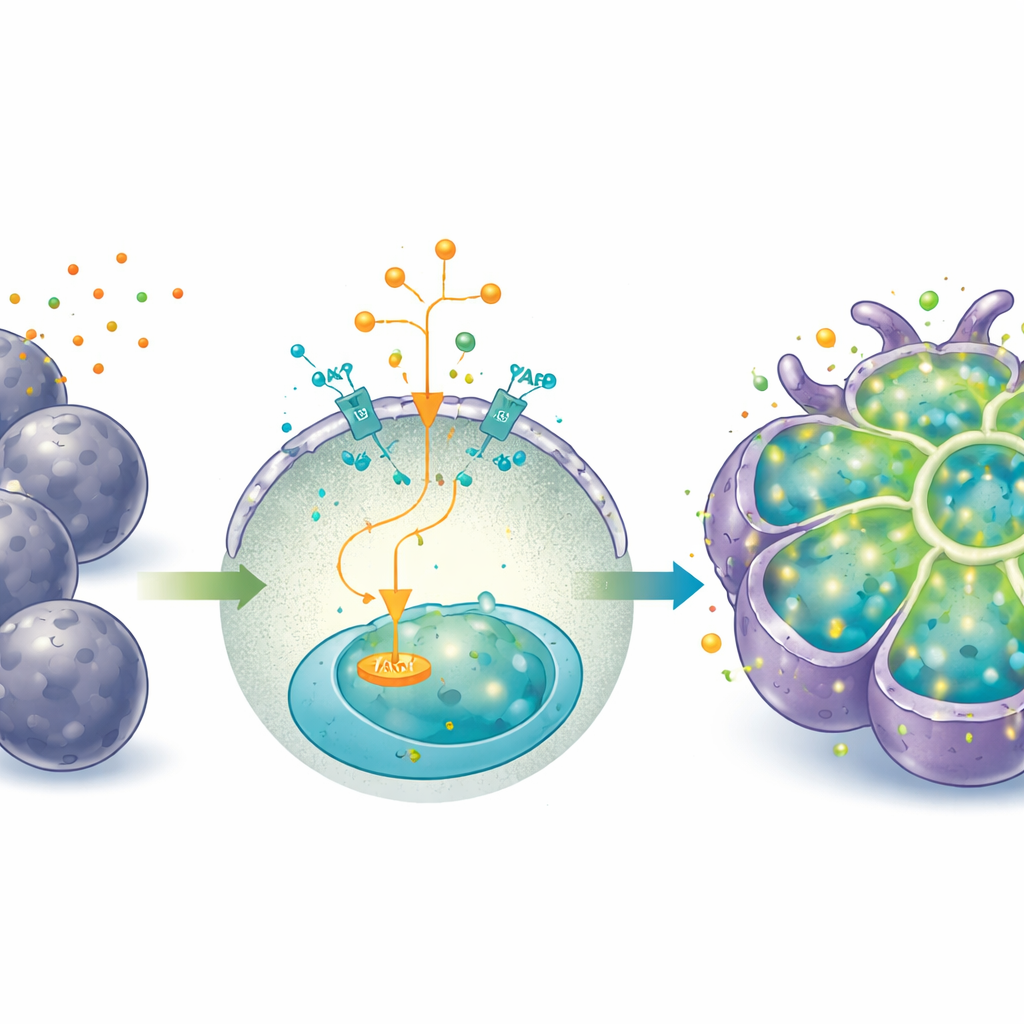
ממצב של גדילה למצב של תפקוד
הפעלת YAP ממושכת, אם כי מצוינת להתרחבות, שמרה על התאים במצב יותר עוברי, פרוגניטורי, והחלישה חלק מתפקודי הכבד הבוגרים. כדי להעביר את האורגנואידים מ"מצב גדילה" ל"מצב עבודה", החוקרים שינו את התווך — הסירו IGF2, אגוניסט YAP ומפעיל Wnt, והוסיפו את ההורמון דקסמתזון והציטוקין oncostatin M. בתנאים אלה התפתחו באורגנואידים תאים גדולים יותר, פורמליים יותר (פוליגונליים) עם יחס גרעין-ציטופלזמה נמוך יותר ויותר תאים בעלי גרעין כפול, כולם סימנים למיגור של הפטוציטים. הם ייצרו יותר אלבומין ואוריאה, טיפלו בצבע דמה (אינדוציאנין גרין) פנימה והחוצה מהתאים, והגבירו אנזימי מטבוליזם תרופות מרכזיים, במיוחד לאחר חשיפה למגרי אנזים ידועים.
שחזור זרימת המרה וטיפול במתכות
הישג מרכזי של אורגנואידים אלה הוא יכולתם לשחזר הובלה מקוטבת — התנועה מכוונת של חומרים למשטחים מסוימים של התא. ה-G-heporgs הניתנים להתרחבות יצרו ערוצי דמויי-תעלות מרה המסומנים בחלבונים שבדרך כלל מרוכזים בממברנות האפיקליות. דימות בחיים הראה תרכובות בדיקה פלואורסצנטיות שנשאבו לתוך החללים הזעירים הללו, ותרופות הידועות כגורמות כולסטאזיס בחולים שיבשו את רשת התעלות הזו וגרמו להצטברות הצבעים בתוך התאים, מה שמשקף מקרוב תופעות רעילות שנצפות במרפאה. הצוות גם עקב אחרי ATP7B, משנע נחושת המוטנט במחלת וילסון, וגילה שבתגובה לנחושת גבוהה הוא נדד ממחסנים פנימיים אל פני השטח הפונים למרה ולמבנים דמויי ליזוזום, בדיוק כפי שבכבד מקורר. זה מדגים שהאורגנואידים יכולים למפות כיצד הפטוציטים מנווטים מתכות ומולקולות אחרות באופן מקוטב.
מה משמעות הדבר למחקר כבד עתידי
על ידי ניצול הפעולה המשולבת של מסלולי IGF2 ו-YAP, המחברים יצרו מקור מתחדש של אורגנואידים הפטוציטיים אנושיים שמסתדרים לצברים דמויי-ענבים ובונים רשתות תעלות מרה פונקציונליות. אף שהם עדיין מעט פחות בוגרים מרקמת כבד מבוגרת וחסרים תאי תמיכה שאינם הפטוציטים, מבנים אלה לוכדים היבטים מרכזיים של שיקומיות הכבד, קוטביות והובלה. עבור לא-מומחים, משמעות הדבר היא שהמדענים מתקרבים לכבדונים מעבדתיים שיכולים לשמש לחקר מחלות כבד תורשתיות, לבחינת בטיחות תרופות — במיוחד רעילות הקשורה למרה — ולבסוף לחקור טיפולים מבוססי תאים, הכל מבלי להסתמך אך ורק על איברי תורם נדירים.
ציטוט: Wu, H., Liu, S., Chen, S. et al. Generation of proliferative hESC-derived grape-clustered hepatocyte organoids with multipolar architecture as regenerative counterpart via synergy of YAP and IGF2 pathways. Cell Death Dis 17, 381 (2026). https://doi.org/10.1038/s41419-026-08635-y
מילות מפתח: אורגנואידים של כבד, הפטוציטים נגזרים מתאים גזע, תעלות נוזל המרה, שחזור הכבד, נזק כבדי מוחזר על ידי תרופות