Clear Sky Science · fr
Génération d’organoïdes hépatiques dérivés d’hESC en grappes de type « raisin » prolifératifs avec architecture multipolaire comme pendant régénératrice via la synergie des voies YAP et IGF2
Construire de petits foies en laboratoire
Le foie prend en charge discrètement nombre des tâches les plus exigeantes de l’organisme — détoxifier les médicaments, traiter les nutriments et gérer les lipides et les sucres. Pourtant, le tissu hépatique humain est rare et les cellules hépatiques matures perdent rapidement leurs fonctions en culture. Cette étude décrit une méthode pour cultiver de petites grappes de cellules hépatiques humaines, semblables à des raisins, à partir de cellules souches embryonnaires : elles non seulement survivent et se divisent pendant des semaines, mais reproduisent aussi des caractéristiques clés du tissu hépatique réel, notamment la capacité à déplacer la bile et d’autres substances de façon hautement organisée.
Pourquoi les grappes de cellules hépatiques sont importantes
Les scientifiques espèrent depuis longtemps construire des « organoïdes » hépatiques tridimensionnels qui se comportent comme du tissu hépatique authentique. Les organoïdes existants dérivés de cellules des conduits biliaires tendent à former des kystes creux avec une polarité simple intérieur–extérieur, ce qui ne correspond pas à la structure complexe des véritables hépatocytes. Dans l’organisme, chaque hépatocyte possède plusieurs surfaces « apicales » qui se joignent aux cellules voisines pour former un réseau biliaire ramifié tout en échangeant des substances avec le sang sur sa face opposée. Des organoïdes d’hépatocytes en grappes, dérivés de cellules hépatiques adultes primaires, peuvent imiter cette forme et cette fonction multipolaires, mais ils dépendent de tissus de donneurs, limités et variables. Les travaux présentés montrent que des organoïdes similaires en grappes peuvent être produits à partir de cellules souches embryonnaires humaines, offrant une source potentiellement plus abondante et standardisée.
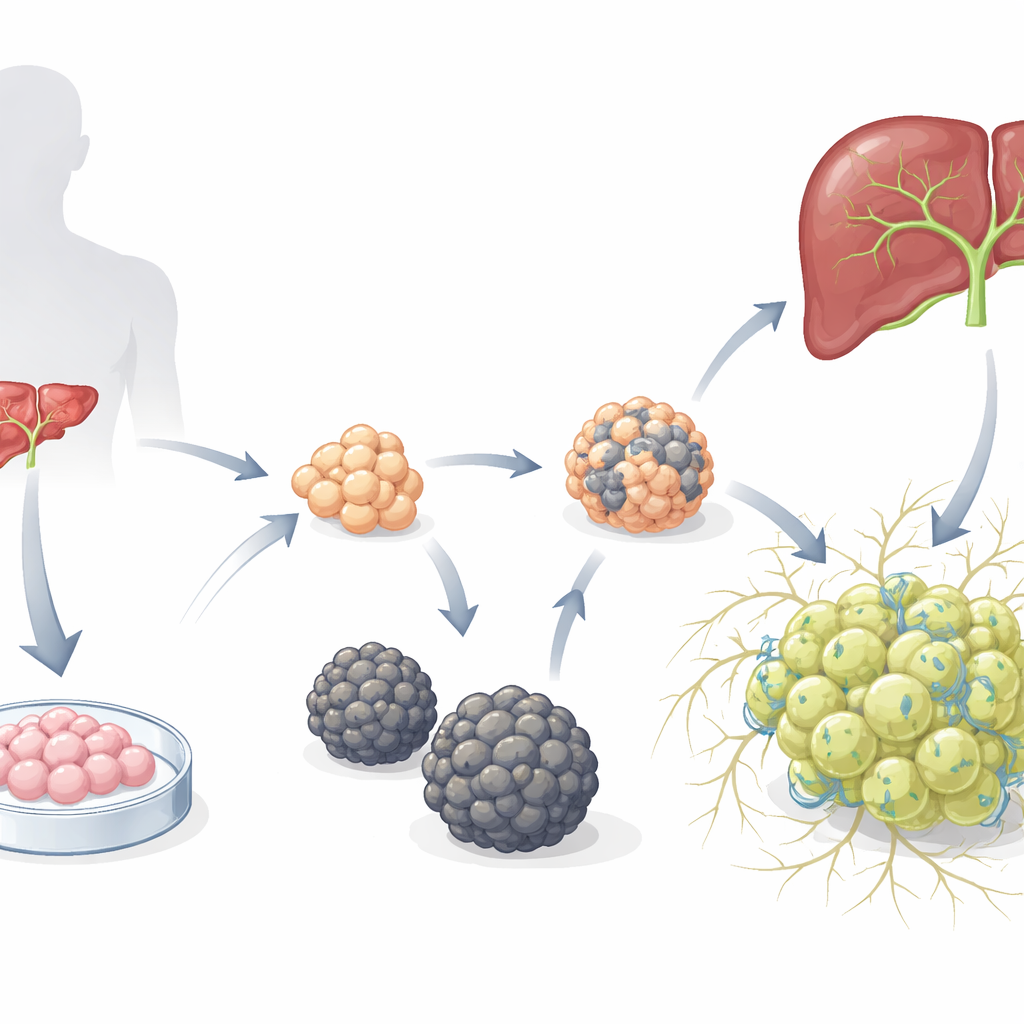
Deux types de mini-foies très différents
Les chercheurs ont commencé avec des organoïdes d’hépatoblastes précédemment établis — des progéniteurs hépatiques immatures issus de cellules souches embryonnaires humaines — et les ont placés dans un milieu conçu pour favoriser le développement des hépatocytes. Au fil du temps, deux types distincts d’organoïdes ont émergé. Un type formait des sphères lisses (S-heporgs) qui croissaient peu, présentaient des signes de vieillissement et de mort cellulaire, et n’organisaient pas correctement un réseau de canalicules biliaires. L’autre type formait des grappes irrégulières, en forme de raisin (G-heporgs), qui s’étendaient jusqu’à plusieurs centaines de micromètres, contenaient de nombreuses cellules en division et binucléées, exprimaient de forts niveaux de protéines hépatiques matures comme l’albumine, et construisaient des structures canaliculaires ramifiées et complexes entre les cellules. Des tests génétiques et fonctionnels ont montré que les G-heporgs étaient métaboliquement actifs et prolifératifs, tandis que les S-heporgs restaient dans un état sénescent évoquant une lésion.
Signaux inflammatoires, facteurs de croissance et commutateur de régénération
Une surprise a été que les S-heporgs défaillants semblaient favoriser l’apparition des G-heporgs plus performants. À mesure que les S-heporgs vieillissaient, ils libéraient des molécules inflammatoires et créaient un microenvironnement ressemblant à un foie endommagé. Dans ce contexte, les G-heporgs activaient un programme de croissance centré sur le facteur IGF2 et son récepteur, qui engageait à son tour la voie de signalisation PI3K–AKT connue pour stimuler la division cellulaire. L’ajout d’IGF2 au milieu augmentait à la fois le nombre et la taille des G-heporgs, tandis que le blocage de son récepteur ou de la signalisation en aval les éliminait presque entièrement. Parallèlement, les G-heporgs présentaient une forte activation de YAP, une protéine détectrice de signaux mécaniques et de lésion essentielle à la régénération hépatique après dommage. Lorsque l’équipe a augmenté artificiellement l’activité de YAP avec un agoniste moléculaire, les organoïdes ont pu être étendus pendant plus de deux mois et de nombreux passages sans perdre leur architecture en grappe ; inhiber YAP réduisait fortement la croissance.
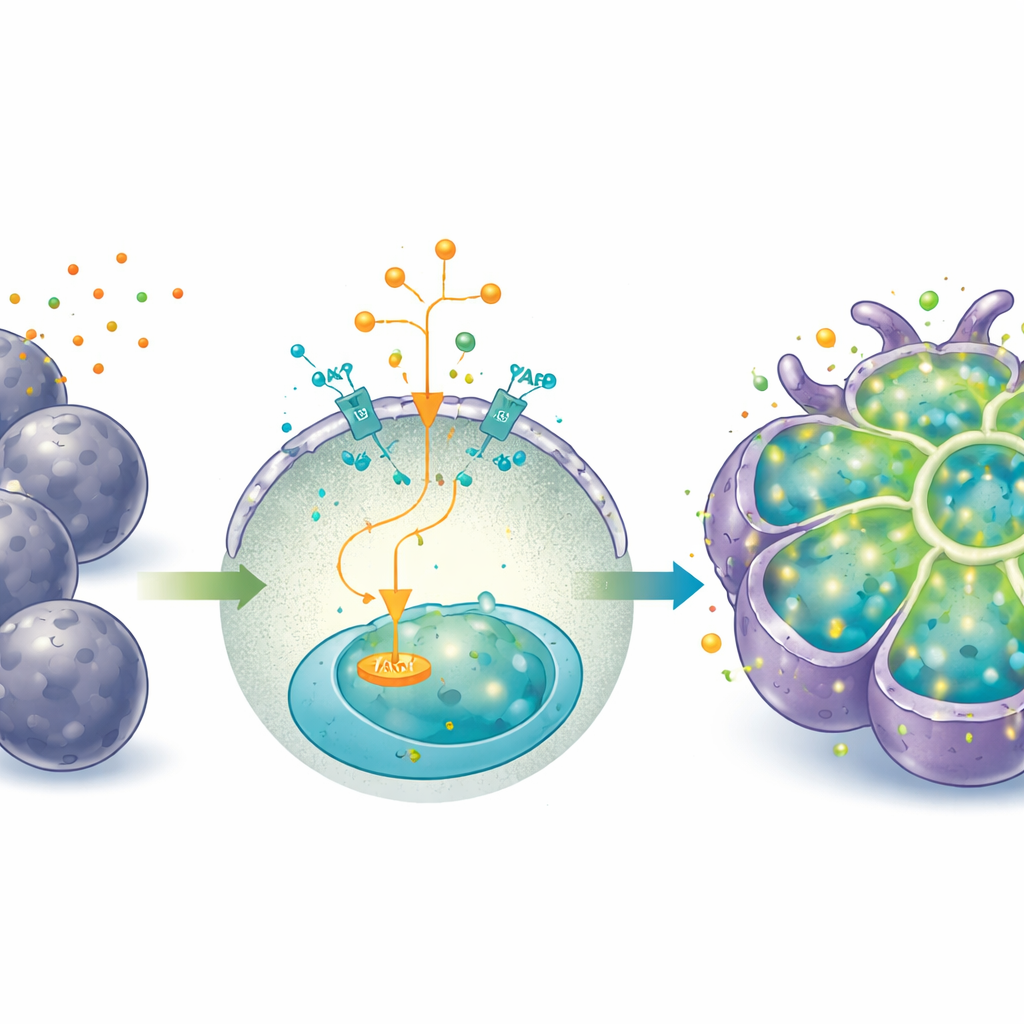
Du mode croissance au mode travail
Une activation prolongée de YAP, bien qu’excellente pour l’expansion, maintenait les cellules dans un état plus fœtal et progéniteur et atténuait certaines fonctions hépatiques matures. Pour faire passer les organoïdes du « mode croissance » au « mode travail », les chercheurs ont modifié le milieu — retirant IGF2, l’agoniste de YAP et un activateur de Wnt, et ajoutant l’hormone dexaméthasone et la cytokine oncostatine M. Dans ces conditions, les organoïdes ont développé des cellules plus grandes et polygonales avec un rapport noyau/cytoplasme réduit et plus de cellules binucléées, autant de traits de maturation des hépatocytes. Elles ont produit davantage d’albumine et d’urée, ont pris en charge un colorant modèle (l’indocyanine verte) entrant et sortant des cellules, et ont augmenté les enzymes clés du métabolisme des médicaments, en particulier après exposition à des inducteurs enzymatiques connus.
Recréer le flux biliaire et la gestion des métaux
Une réussite centrale de ces organoïdes est leur capacité à recréer le transport polarisé — le mouvement dirigé de substances vers des surfaces cellulaires spécifiques. Les G-heporgs extensibles ont formé des canaux ressemblant à des canalicules biliaires marqués par des protéines qui se concentrent normalement sur les membranes apicales. L’imagerie en direct a montré des composés tests fluorescents pompés dans ces petits luminæ, et des médicaments connus pour provoquer une cholestase chez les patients perturbaient ce réseau canaliculaire et entraînaient l’accumulation des colorants à l’intérieur des cellules, reproduisant étroitement les effets toxiques observés en clinique. L’équipe a également suivi ATP7B, un transporteur de cuivre muté dans la maladie de Wilson, et a constaté qu’en réponse à un excès de cuivre, il se déplaçait des compartiments internes vers les surfaces faisant face à la bile et des structures de type lysosome, comme dans le foie natif. Cela montre que les organoïdes peuvent modéliser la façon dont les hépatocytes dirigent les métaux et d’autres molécules de manière polarisée.
Ce que cela signifie pour la recherche hépatique future
En exploitant l’action combinée des voies IGF2 et YAP, les auteurs ont créé une source renouvelable d’organoïdes d’hépatocytes humains qui s’assemblent en grappes et construisent des réseaux fonctionnels de canalicules biliaires. Bien qu’encore un peu moins matures que le tissu hépatique adulte et dépourvus de cellules de soutien non-hépatiques, ces structures capturent des aspects clés de la régénération du foie, de la polarité et du transport. Pour les non-spécialistes, cela signifie que les scientifiques se rapprochent de mini-foies cultivés en laboratoire utilisables pour étudier des maladies hépatiques héréditaires, tester la sécurité des médicaments — en particulier la toxicité liée à la bile — et, éventuellement, explorer des thérapies cellulaires, le tout sans dépendre uniquement des organes de donneurs rares.
Citation: Wu, H., Liu, S., Chen, S. et al. Generation of proliferative hESC-derived grape-clustered hepatocyte organoids with multipolar architecture as regenerative counterpart via synergy of YAP and IGF2 pathways. Cell Death Dis 17, 381 (2026). https://doi.org/10.1038/s41419-026-08635-y
Mots-clés: organoïdes hépatiques, hépatocytes dérivés de cellules souches, canalicules biliaires, régénération du foie, toxicité hépatique induite par les médicaments