Clear Sky Science · de
Erzeugung proliferativer, aus hESC abgeleiteter, traubenförmiger Hepatozyten-Organoide mit multipolarer Architektur als regeneratives Pendant durch Synergie der YAP- und IGF2-Wege
Winzige Lebern im Labor bauen
Die Leber bewältigt im Stillen viele der härtesten Aufgaben des Körpers – sie entgiftet Medikamente, verarbeitet Nährstoffe und reguliert Fette und Zucker. Menschliches Lebergewebe ist jedoch knapp, und reife Leberzellen verlieren im Kultursystem schnell ihre Funktion. Diese Studie beschreibt eine Methode, winzige, traubenartige Cluster menschlicher Leberzellen aus embryonalen Stammzellen zu züchten, die nicht nur wochenlang überleben und sich teilen, sondern auch wesentliche Merkmale echten Lebergewebes nachbilden, einschließlich der Fähigkeit, Galle und andere Substanzen in hochorganisierter Weise zu transportieren.
Warum Hepatozyten-Cluster wichtig sind
Wissenschaftler hoffen seit Langem, dreidimensionale Leber-"Organoide" herzustellen, die sich wie echtes Lebergewebe verhalten. Bestehende Organoide aus Gallengangszellen neigen dazu, hohle Zysten mit einfacher Innen–Außen-Polarität zu bilden, was nicht der komplexen Struktur echter Hepatozyten entspricht. Im Körper besitzt jeder Hepatozyt mehrere „apikale“ Flächen, die sich mit Nachbarzellen verbinden und ein verzweigtes Gallenkanalnetz bilden, während er zugleich auf der gegenüberliegenden Seite Stoffaustausch mit dem Blut betreibt. Traubenähnliche Hepatozyten-Organoide, die aus primären adulten Leberzellen gewonnen werden, können diese multipolare Form und Funktion nachahmen, sind aber auf Spendergewebe angewiesen, das begrenzt und variabel ist. Die neue Arbeit zeigt, dass ähnliche traubenförmige Organoide aus menschlichen embryonalen Stammzellen hergestellt werden können und damit eine potenziell reichlichere und standardisiertere Quelle bieten.
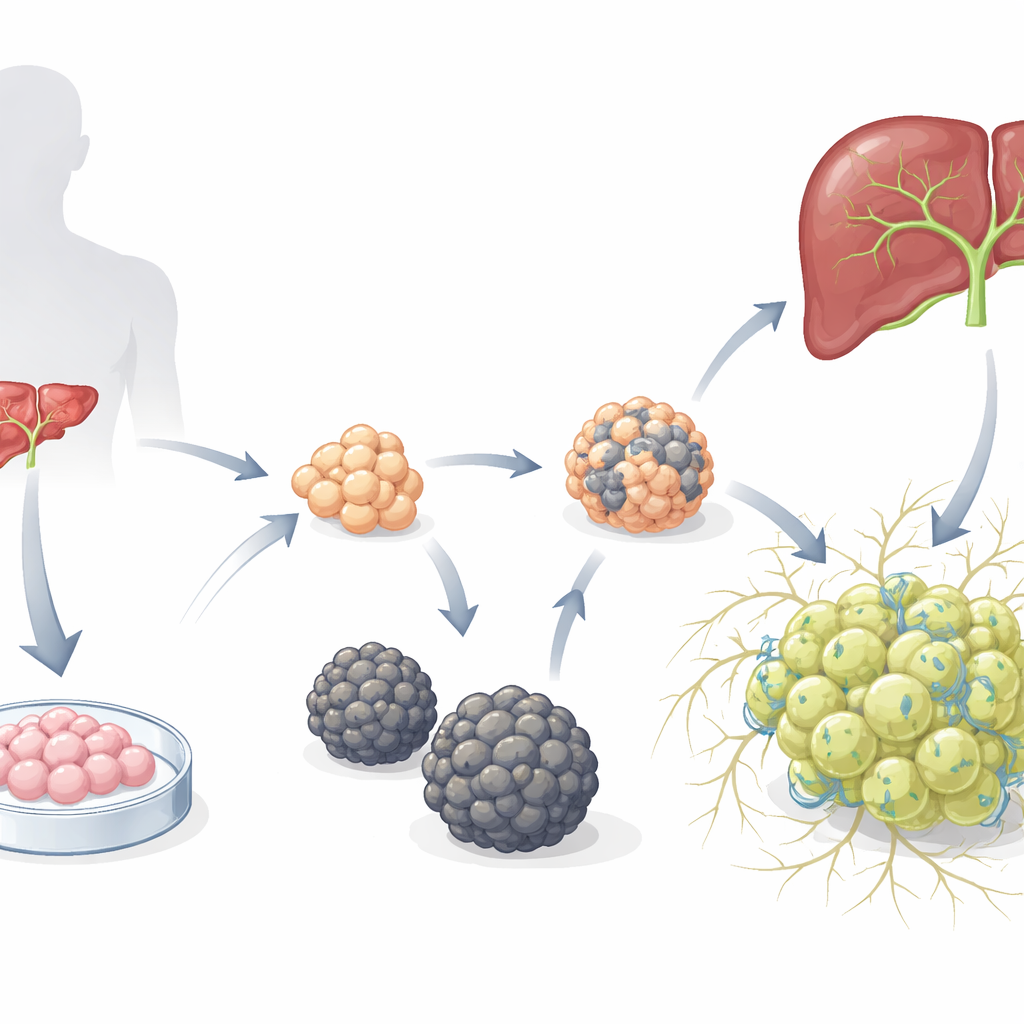
Zwei sehr unterschiedliche Mini-Leber-Gemeinschaften
Die Forschenden begannen mit zuvor etablierten Hepatoblast-Organoiden – unreifen Lebervorläufern, die aus menschlichen embryonalen Stammzellen gezüchtet wurden – und setzten sie in ein Medium, das die Hepatozytenentwicklung begünstigt. Im Laufe der Zeit entstanden zwei deutlich unterscheidbare Organoidtypen. Ein Typ bildete glatte Kugeln (S-heporgs), die schlecht wuchsen, Alters- und Zellsterbezeichen zeigten und kein funktionierendes Gallenkanalnetz organisierten. Der andere Typ bildete unregelmäßige, traubenartige Cluster (G-heporgs), die sich auf mehrere hundert Mikrometer ausdehnten, viele teilende und binukleäre Zellen enthielten, hohe Mengen reifer Leberproteine wie Albumin exprimierten und komplexe, verzweigte Kanalstrukturen zwischen den Zellen aufbauten. Genetische und funktionelle Tests zeigten, dass G-heporgs stoffwechselaktiv und proliferativ waren, während S-heporgs in einem seneszenten, verletzungsähnlichen Zustand verharrten.
Entzündliche Signale, Wachstumsfaktoren und ein Regenerationsschalter
Eine unerwartete Wendung war, dass die versagenden S-heporgs offenbar das Auftreten der erfolgreicheren G-heporgs förderten. Mit zunehmendem Altern setzten S-heporgs entzündliche Moleküle frei und schufen ein Mikroenvironment ähnlich einer geschädigten Leber. In diesem Umfeld aktivierten G-heporgs ein Wachstumsprogramm, das um den Faktor IGF2 und seinen Rezeptor zentriert war, welcher wiederum den PI3K–AKT-Signalweg aktivierte, der für Zellteilung bekannt ist. Zugabe von zusätzlichem IGF2 zur Kultur steigerte sowohl Anzahl als auch Größe der G-heporgs, während Blockade ihres Rezeptors oder der nachgeschalteten Signale sie nahezu eliminierte. Gleichzeitig zeigten die G-heporgs eine starke Aktivierung von YAP, einem Protein, das mechanische und Verletzungssignale erkennt und für das Leberwachstum nach Schädigung entscheidend ist. Als das Team YAP künstlich mit einem kleinen Molekül-Agonisten hochregulierte, konnten die Organoide über mehr als zwei Monate und viele Passagen expandiert werden, ohne ihre traubenartige Architektur zu verlieren; das Abschalten von YAP verringerte das Wachstum deutlich.
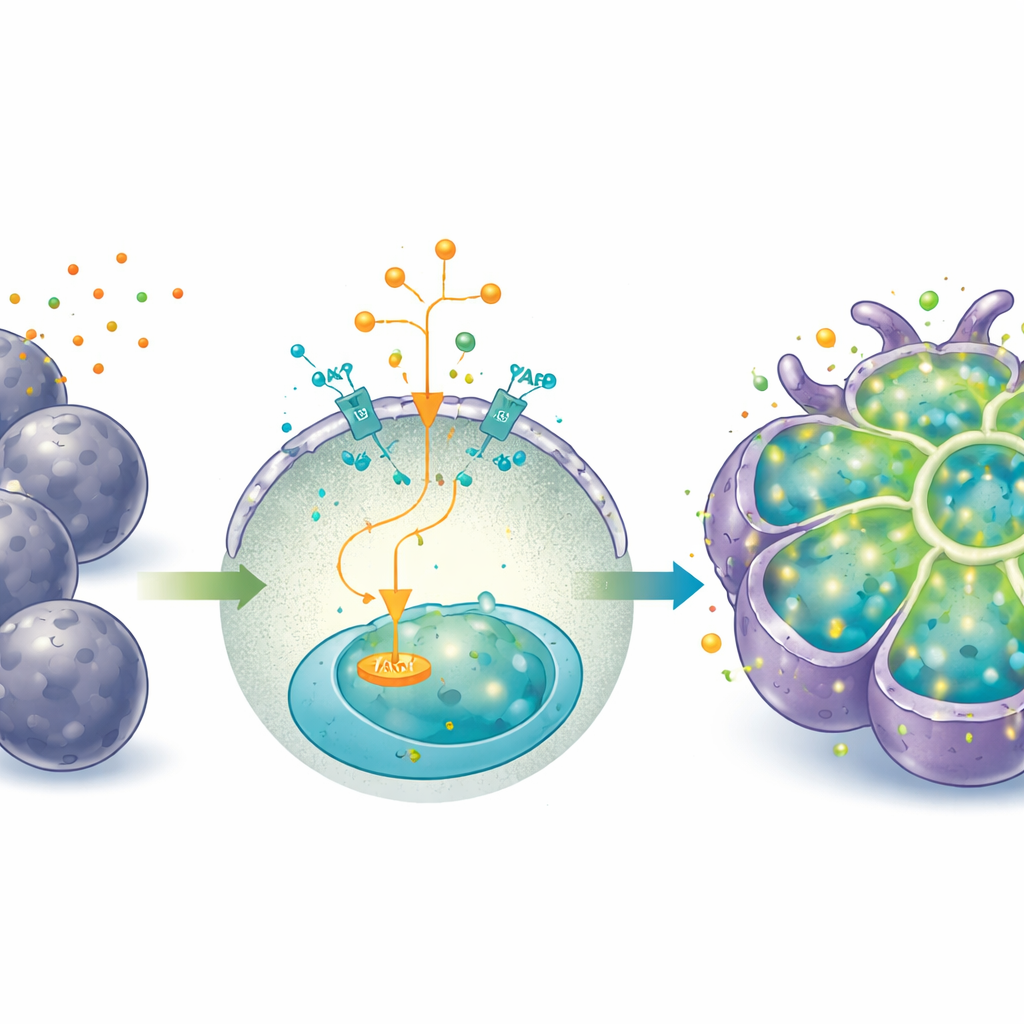
Vom Wachstums- in den Arbeitsmodus
Lang anhaltende YAP-Aktivierung war zwar ideal für die Expansion, hielt die Zellen aber in einem eher fetalen, vorläuferähnlichen Zustand und dämpfte einige ausgereifte Leberfunktionen. Um die Organoide vom „Wachstumsmodus“ in den „Arbeitsmodus“ zu überführen, änderten die Forschenden das Medium – sie entfernten IGF2, den YAP-Agonisten und einen Wnt-Aktivator und fügten das Hormon Dexamethason sowie das Zytokin Oncostatin M hinzu. Unter diesen Bedingungen entwickelten die Organoide größere, polygonale Zellen mit niedrigeren Kern-zu-Zytoplasma-Verhältnissen und mehr binukleären Zellen, alles Kennzeichen mogneder Hepatozyten. Sie produzierten mehr Albumin und Harnstoff, transportierten einen Modellfarbstoff (Indocyaningrün) hinein und wieder heraus und steigerten wichtige medikamentenmetabolisierende Enzyme, insbesondere nach Exposition gegenüber bekannten Enzyminduktoren.
Gallefluss und Metallverarbeitung nachbilden
Eine zentrale Errungenschaft dieser Organoide ist ihre Fähigkeit, polaren Transport nachzubilden – die gerichtete Bewegung von Substanzen zu bestimmten Zellflächen. Die expandierbaren G-heporgs bildeten gallenkanalähnliche Kanäle, markiert durch Proteine, die normalerweise an apikalen Membranen konzentriert sind. Live-Imaging zeigte, wie fluoreszierende Testverbindungen in diese winzigen Lumen gepumpt wurden, und Medikamente, die beim Patienten Cholestase verursachen, störten dieses Kanalnetz und führten zu einer Akkumulation der Farbstoffe in den Zellen, was toxische Nebenwirkungen in der Klinik eng widerspiegelt. Das Team verfolgte zudem ATP7B, einen Kupfertransporter, der bei Morbus Wilson mutiert ist, und stellte fest, dass er als Reaktion auf hohe Kupferwerte von inneren Kompartimenten zu gallenseitigen Oberflächen und lysosomähnlichen Strukturen wanderte, genau wie in nativer Leber. Dies zeigt, dass die Organoide modellieren können, wie Hepatozyten Metalle und andere Moleküle polar dirigieren.
Was das für die zukünftige Leberforschung bedeutet
Durch die Nutzung der kombinierten Wirkung der IGF2- und YAP-Wege schufen die Autoren eine erneuerbare Quelle menschlicher Hepatozyten-Organoide, die sich zu traubenförmigen Clustern zusammenlagern und funktionelle Gallenkanalnetze aufbauen. Obwohl sie noch etwas weniger ausgereift sind als das adulte Lebergewebe und unterstützende Nicht-Hepatozyten fehlen, erfassen diese Strukturen zentrale Aspekte von Leberregeneration, Polarität und Transport. Für Nicht-Spezialisten bedeutet das: Forschende kommen näher an im Labor gezüchtete Mini-Lebern heran, die genutzt werden können, um erbliche Lebererkrankungen zu untersuchen, die Sicherheit von Medikamenten zu testen – insbesondere gallenbezogene Toxizität – und langfristig zellbasierte Therapien zu erforschen, ganz ohne allein auf knappe Spenderorgane angewiesen zu sein.
Zitation: Wu, H., Liu, S., Chen, S. et al. Generation of proliferative hESC-derived grape-clustered hepatocyte organoids with multipolar architecture as regenerative counterpart via synergy of YAP and IGF2 pathways. Cell Death Dis 17, 381 (2026). https://doi.org/10.1038/s41419-026-08635-y
Schlüsselwörter: Leber-Organoide, aus Stammzellen gewonnene Hepatozyten, Gallenkanalikuli, Leberregeneration, medikamenteninduzierte Leberschädigung