Clear Sky Science · nl
Vervaardiging van proliferatieve hESC-afgeleide druifgeclusterde hepatocytenorganoïden met multipolaire architectuur als regeneratief tegenstuk via synergie van YAP- en IGF2-route
Het bouwen van mini-levers in het laboratorium
De lever voert stilletjes veel van de lastigste taken van het lichaam uit: het ontgiften van medicijnen, het verwerken van voedingsstoffen en het reguleren van vetten en suikers. Menselijk leverweefsel is echter schaars en rijpe levercellen verliezen snel hun functie in een kweek. Deze studie beschrijft een manier om kleine, druifachtige clusters van menselijke levercellen uit embryonale stamcellen te kweken die niet alleen wekenlang leven en delen, maar ook belangrijke kenmerken van echt leverweefsel reproduceren, waaronder het vermogen om gal en andere stoffen op een sterk georganiseerde manier te verplaatsen.
Waarom clusters van levercellen ertoe doen
Wetenschappers hopen al lang driedimensionale lever-“organoïden” te bouwen die zich als echt leverweefsel gedragen. Bestaande organoïden gemaakt uit galgangcellen neigen ertoe holle cysten te vormen met eenvoudige binnen–buiten-polariteit, wat niet overeenkomt met de complexe structuur van echte hepatocyten. In het lichaam heeft elke hepatocyt meerdere ‘apicale’ oppervlakken die met buren samenwerken om een vertakt netwerk van galgangetjes te vormen, terwijl ze aan de andere zijde stoffen met het bloed uitwisselen. Druifachtige hepatocytenorganoïden afgeleid van primaire volwassen levertjes kunnen deze multipolaire vorm en functie nabootsen, maar zijn afhankelijk van donorweefsel dat beperkt en variabel is. Het nieuwe werk laat zien dat vergelijkbare druifgeclusterde organoïden uit menselijke embryonale stamcellen kunnen worden geproduceerd, wat een potentieel rijkere en meer gestandaardiseerde bron biedt.
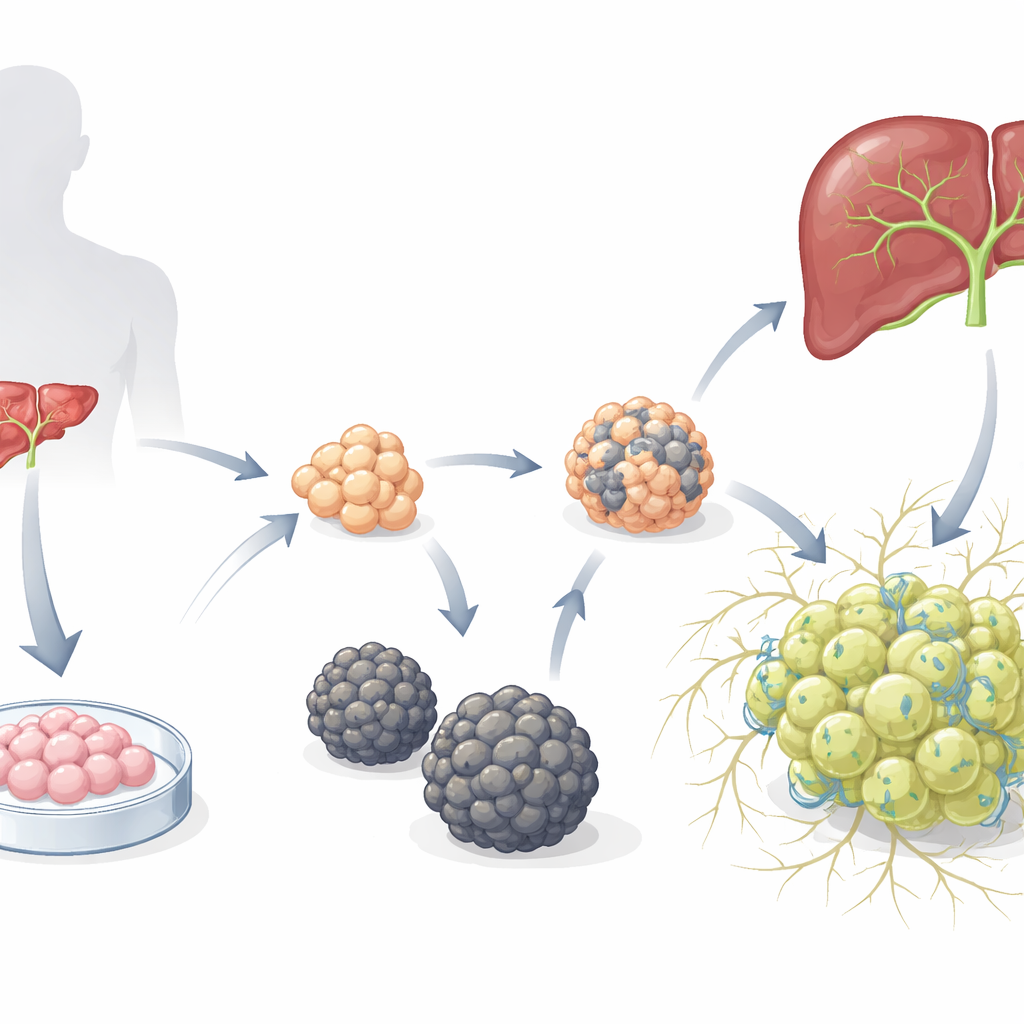
Twee heel verschillende mini-levergemeenschappen
De onderzoekers begonnen met eerder vastgestelde hepatoblastorganoïden—onvolgroeide leverprogenitoren gegroeid uit menselijke embryonale stamcellen—en plaatsten deze in een medium dat hepatocytenontwikkeling bevordert. Na verloop van tijd ontstonden twee duidelijke typen organoïden. Het ene type vormde gladde sferen (S-heporgs) die slecht groeiden, tekenen van veroudering en celdood vertoonden en geen adequaat netwerk van galgangetjes organiseerden. Het andere type vormde onregelmatige, druifachtige clusters (G-heporgs) die uitzetten tot enkele honderden micrometers, veel delende en binucleate cellen bevatten, hoge niveaus van rijpe leverproteïnen zoals albumine tot expressie brachten en ingewikkelde, vertakte kanaalstructuren tussen cellen opbouwden. Genetische en functionele tests toonden aan dat G-heporgs metabolisch actief en proliferatief waren, terwijl S-heporgs vast leken te zitten in een senescent, letselachtig stadium.
Ontstekingssignalen, groeifactoren en een regeneratieschakelaar
Een onverwachte wending was dat de falende S-heporgs de meer succesvolle G-heporgs leken te helpen ontstaan. Naarmate S-heporgs verouderden, gaven ze ontstekingsmoleculen af en creëerden ze een micro-omgeving die leek op een beschadigde lever. In deze setting activeerden G-heporgs een groeiprogramma gecentreerd rond de factor IGF2 en zijn receptor, die op hun beurt het PI3K–AKT-signaleringspad inschakelden dat bekendstaat om celdeling te stimuleren. Het toevoegen van extra IGF2 aan de kweek vergrootte zowel het aantal als de grootte van G-heporgs, terwijl blokkering van zijn receptor of de downstreamsignalen ze bijna volledig deed verdwijnen. Tegelijkertijd toonden G-heporgs sterke activatie van YAP, een eiwit dat mechanische en letselssignalen waarneemt en cruciaal is voor leverherstel na schade. Toen het team YAP-activiteit kunstmatig verhoogde met een kleine moleculaire agonist, konden de organoïden gedurende meer dan twee maanden en vele passages worden uitgebreid zonder hun druifachtige architectuur te verliezen; het uitschakelen van YAP verminderde de groei scherp.
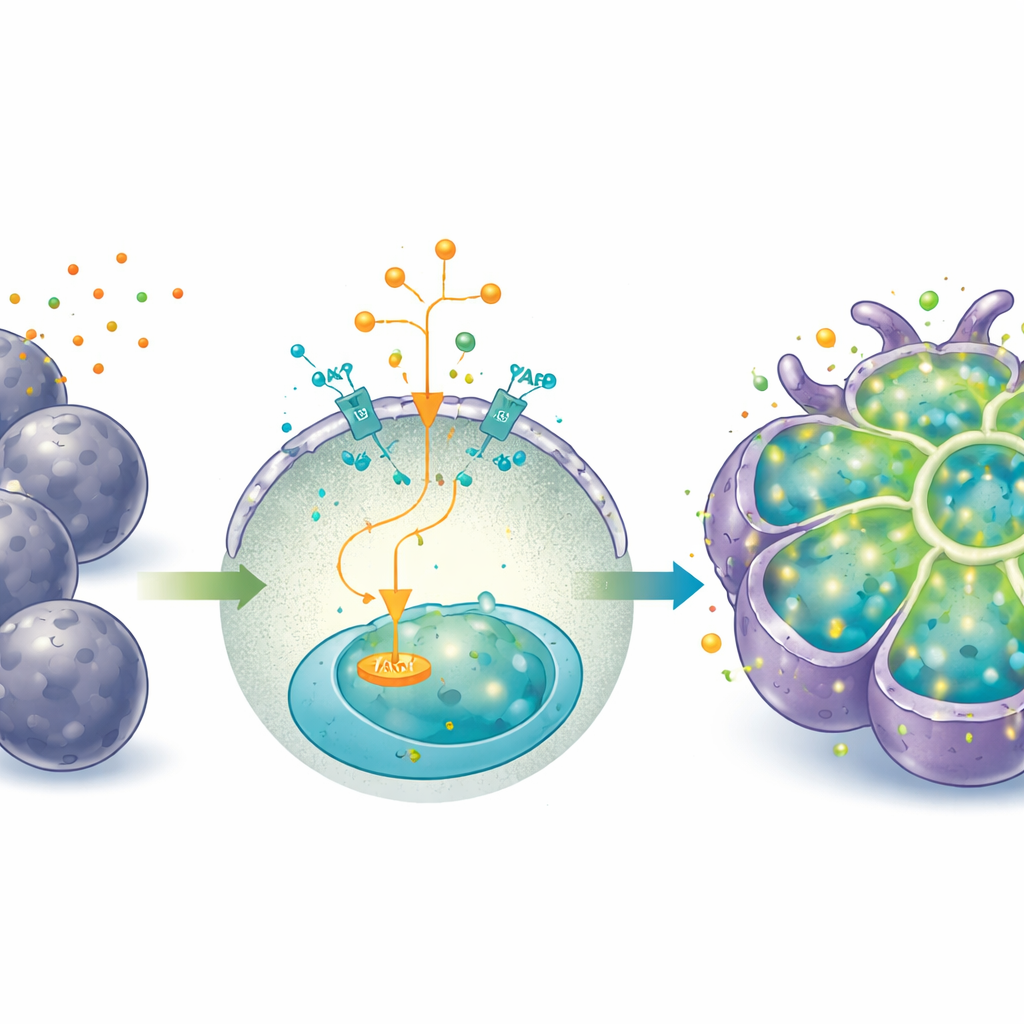
Van groeimodus naar werkmodus
Langdurige YAP-activatie, hoewel uitstekend voor uitbreiding, hield de cellen in een meer foetaal, progenitorachtig stadium en dempte sommige rijpe leverfuncties. Om de organoïden van “groeimodus” naar “werkmodus” te verschuiven, veranderden de onderzoekers het medium—ze verwijderden IGF2, de YAP-agonist en een Wnt-activator, en voegden het hormoon dexamethason en de cytokine oncostatine M toe. Onder deze omstandigheden ontwikkelden de organoïden grotere, veelhoekige cellen met lagere kern‑tot‑cytoplasmaverhoudingen en meer binucleate cellen, allemaal kenmerken van rijpende hepatocyten. Ze produceerden meer albumine en ureum, verwerkten een modelkleurstof (indocyaninegroen) in en uit de cellen, en verhoogden sleutel-enzymen voor geneesmiddelmetabolisme, vooral na blootstelling aan bekende enzyminducers.
Het namaken van galstroom en metaalverwerking
Een centrale prestatie van deze organoïden is hun vermogen gepolariseerd transport na te bootsen—de gerichte verplaatsing van stoffen naar specifieke celoppervlakken. De uitbreidbare G-heporgs vormden galgangachtige kanalen gemarkeerd door eiwitten die normaal op apicale membranen geconcentreerd zijn. Live-imaging toonde fluorescerende testverbindingen die in deze kleine lumen werden gepompt, en geneesmiddelen die bij patiënten cholestase veroorzaken verstoorden dit kanaalnetwerk en leidden tot ophoping van kleurstoffen in de cellen, wat nauwkeurig de toxische bijwerkingen in de kliniek weerspiegelt. Het team volgde ook ATP7B, een koperoverbrenger gemuteerd bij de ziekte van Wilson, en ontdekte dat deze als reactie op hoge koperconcentraties verplaatste van interne compartimenten naar de galgerichte oppervlakken en lysosoomachtige structuren, precies zoals in native lever. Dit toont aan dat de organoïden kunnen modelleren hoe hepatocyten metalen en andere moleculen gepolariseerd dirigeren.
Wat dit betekent voor toekomstig leveronderzoek
Door de gecombineerde werking van IGF2- en YAP-routes te benutten, creëerden de auteurs een hernieuwbare bron van menselijke hepatocytenorganoïden die zich assembleren in druifachtige clusters en functionele netwerken van galgangetjes bouwen. Hoewel ze nog iets minder rijp zijn dan volwassen leverweefsel en ondersteunende niet‑hepatocyten missen, vatten deze structuren belangrijke aspecten van leverregeneratie, polariteit en transport samen. Voor niet‑specialisten betekent dit dat wetenschappers dichterbij komen om in het laboratorium gegroeide mini-levers te gebruiken om erfelijke leverziekten te bestuderen, medicijnen op veiligheid te testen—vooral wat gal-gerelateerde toxiciteit betreft—en uiteindelijk celgebaseerde therapieën te verkennen, allemaal zonder uitsluitend afhankelijk te zijn van schaarse donororganen.
Bronvermelding: Wu, H., Liu, S., Chen, S. et al. Generation of proliferative hESC-derived grape-clustered hepatocyte organoids with multipolar architecture as regenerative counterpart via synergy of YAP and IGF2 pathways. Cell Death Dis 17, 381 (2026). https://doi.org/10.1038/s41419-026-08635-y
Trefwoorden: levernanoïden, hepatocyten afgeleid van stamcellen, galgangetjes, leverregeneratie, geneesmiddelgeïnduceerde leverschade