Clear Sky Science · ar
تكوين عضوويّات كبدية مُستمدة من الخلايا الجذعية الجنينية البشرية على شكل عناقيد عنبية ذات بنية متعددة الأقطاب كنظير تجديدي عبر تآزر مسارات YAP وIGF2
بناء أكباد صغيرة في المختبر
يقوم الكبد بهدوء بالعديد من أصعب وظائف الجسم — تحييد السموم من الأدوية، معالجة المغذيات، وإدارة الدهون والسكريات. ومع ذلك، نسيج الكبد البشري نادر، والخلايا الكبدية الناضجة تفقد وظائفها بسرعة في طبق الزرع. تصف هذه الدراسة طريقة لزراعة عناقيد صغيرة شبيهة بالعنب من خلايا كبدية بشرية مُشتقة من الخلايا الجذعية الجنينية التي لا تبقى فقط على قيد الحياة وتتزايد لأسابيع، بل تُعيد أيضاً ميزات أساسية من نسيج الكبد الحقيقي، بما في ذلك القدرة على نقل الصفراء ومواد أخرى بطريقة منظمة بشكل كبير.
لماذا تهم عناقيد الخلايا الكبدية
لطالما راجت لدى العلماء فكرة بناء "عضويّات" كبد ثلاثية الأبعاد تتصرف كنسيج كبد حقيقي. تميل العضويّات الحالية المصنوعة من خلايا قنوات الصفراء إلى تشكيل أكياس مجوفة ذات قطبية بسيطة داخل/خارج، وهو ما لا يتطابق مع البنية المعقدة للخلايا الكبدية الحقيقية. في الجسم، لكل خلية كبدية عدة أسطح "قميّة" تتصل بالجيران لتكوّن شبكة متفرعة من قنوات الصفراء بينما تتبادل المواد مع الدم على جانبها المقابل. يمكن لعضويّات الخلايا الكبدية الشبيهة بالعنب المشتقة من خلايا كبدية بالغة أولية أن تحاكِي هذا الشكل والوظيفة متعددة الأقطاب، لكنها تعتمد على نسيج متبرع محدود ومتفاوت. يُظهر العمل الجديد أنه يمكن إنتاج عضويّات عناقيد عنبية مماثلة من الخلايا الجذعية الجنينية البشرية، مما يوفر مصدراً أكثر وفرة ومعيارية محتملة.
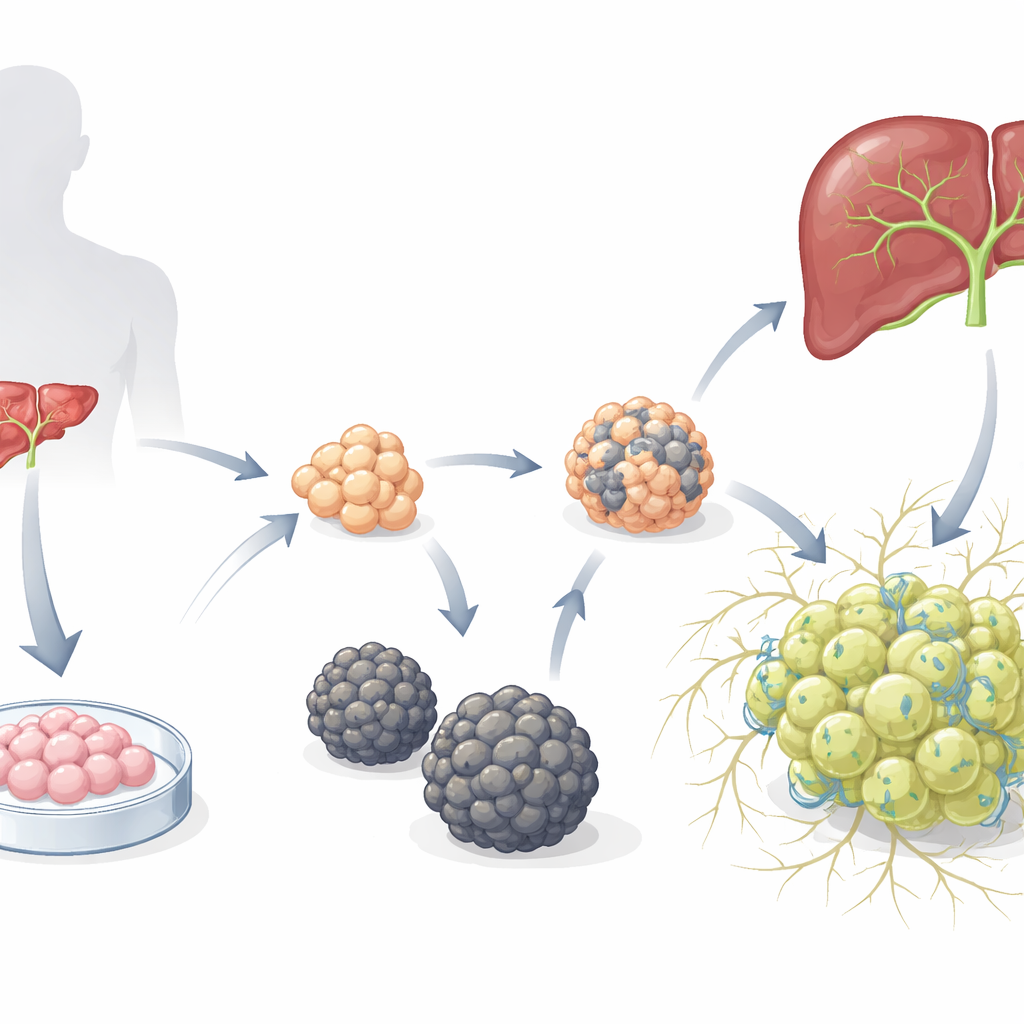
مجتمعان مصغَّران للكبد مختلفان تماماً
بدأ الباحثون بعضويّات بدائية كبدية معروفة سلفاً — سلالات ناضجة من الخلايا الكبدية الجنينية المُستزرعة — ووضعوها في وسط مصمم لتشجيع تطور الخلايا الكبدية. مع مرور الوقت، ظهرت نوعان مميزان من العضويّات. شكل نوع واحد كريات ناعمة (S-heporgs) نمت بشكل ضعيف، أظهرت علامات شيخوخة وموت خلوي، وفشلت في تنظيم شبكة قنوات صفراء صحيحة. بينما شكل النوع الآخر عناقيد غير منتظمة شبيهة بالعنب (G-heporgs) توسعت لتصل إلى مئات الميكرومترات، احتوت على العديد من الخلايا المنقسمة وثنائية النواة، عبرت عن مستويات عالية من بروتينات كبدية ناضجة مثل الألبومين، وبنت هياكل قناة متفرعة ومعقدة بين الخلايا. أظهرت الاختبارات الجينية والوظيفية أن G-heporgs كانت نشطة أيضياً وقابلة للتكاثر، بينما كانت S-heporgs عالقة في حالة شبيه بالشيخوخة أو الإصابة.
الإشارات الالتهابية وعوامل النمو ومفتاح التجدد
من الملاحظ وغير المتوقع أن S-heporgs الفاشلة بدا أنها تُسهِم في ظهور G-heporgs الأكثر نجاحاً. مع تقدم عمر S-heporgs، أطلقت جزيئات التهابية وخلقت بيئة مجهرية تشبه الكبد المتضرر. في هذا السياق، فعّلت G-heporgs برنامج نمو مركزي يعتمد على العامل IGF2 ومستقبله، الذي بدوره شغّل مسار الإشارة PI3K–AKT المعروف بتحفيز انقسام الخلايا. إضافة IGF2 إضافي إلى الوسط زادت عدد وحجم G-heporgs، بينما حجبت مستقبلّه أو الإشارات اللاحقة فتكاد تلغي وجودها. في الوقت نفسه، أظهرت G-heporgs تنشيطاً قوياً لبروتين YAP، وهو مُستشعر للإشارات الميكانيكية والإصابية وحاسم لاستعادة الكبد بعد الضرر. عندما زيَّد الفريق نشاط YAP صناعياً باستخدام منبّه جزيئي صغير، أمكن توسيع العضويّات لأكثر من شهرين وعدة تمريرات دون فقدان بنية العناقيد العنبية؛ وإطفاء YAP حاداً أوقف النمو.
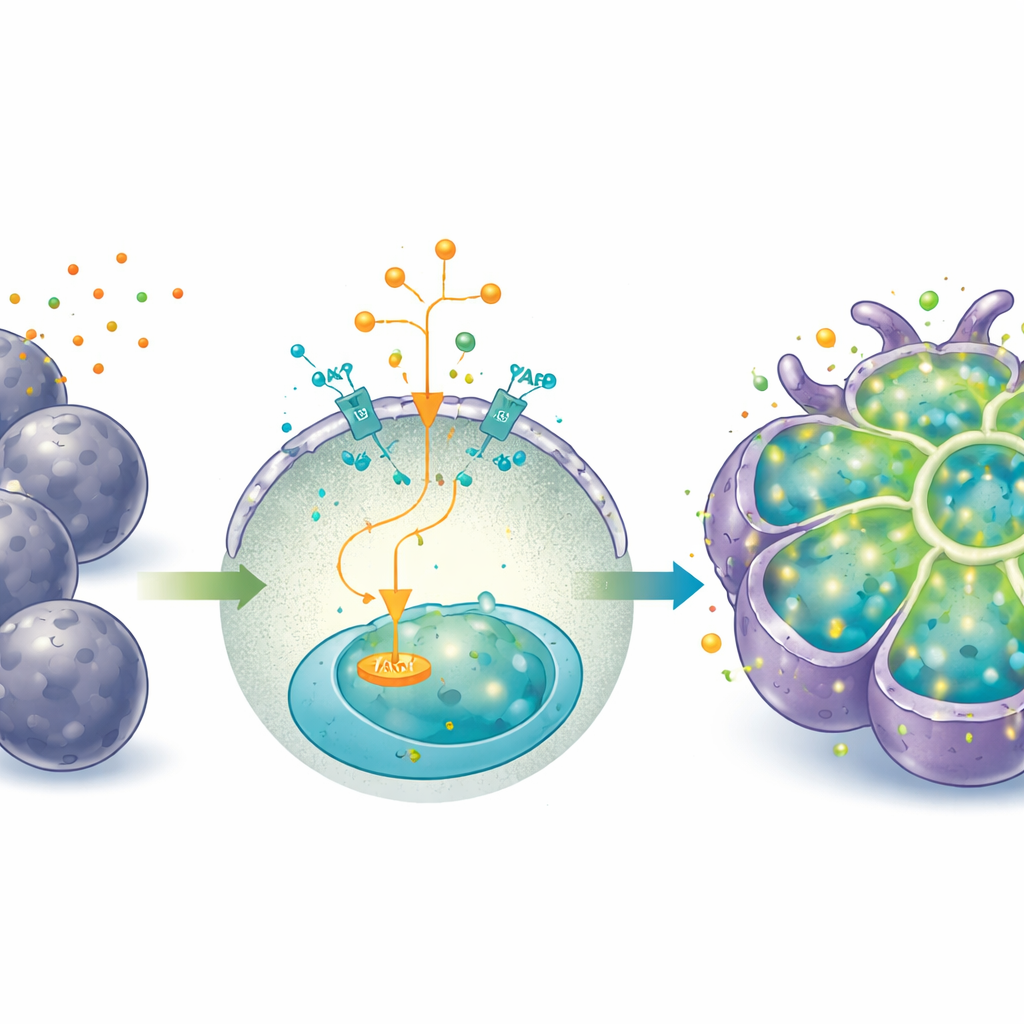
من وضع النمو إلى وضع العمل
بينما كان تنشيط YAP المطوَّل ممتازاً للتوسع، أبقى الخلايا في حالة أكثر جنينية وبدائية وكبت بعض وظائف الكبد الناضجة. لتحويل العضويّات من "وضع النمو" إلى "وضع العمل"، غيّر الباحثون الوسط — أزالوا IGF2 ومنبّه YAP ومنشّط Wnt، وأضافوا هرمون الديكساميثازون والسيتوكين أونكوستاتين M. تحت هذه الظروف، طورت العضويّات خلايا أكبر متعددة الأضلاع ذات نسب نواة/سايتوبلازم أقل والمزيد من الخلايا ثنائية النواة، وهي سمات مميزة لنضج الخلايا الكبدية. أنتجت المزيد من الألبومين واليوريا، وتعاملت مع صبغة نموذجية (الإندوسيانين أخضر) داخل وخارج الخلايا، وزادت مستويات إنزيمات أيض الأدوية الأساسية، وخاصة بعد التعرض لمحفزات هذه الإنزيمات المعروفة.
إعادة خلق تدفّق الصفراء وتعامل المعادن
إنجاز مركزي لهذه العضويّات هو قدرتها على إعادة خلق النقل المستقطب — الحركة الموجهة للمواد إلى أسطح محددة من الخلية. شكّلت G-heporgs القابلة للتوسع قنوات شبيهة بقنوات الصفراء مُعلَّمة ببروتينات تتركز عادة على الأغشية القمية. أظهر تصوير حي ضخ مركبات اختبار فلورية داخل هذه التجاويف الصغيرة، وأدت أدوية معروفة بأنها تسبب ركود الصفراء لدى المرضى إلى تعطيل شبكة القنوات هذه وتراكم الصبغات داخل الخلايا، ما يعكس الآثار السمية الجانبية في العيادة عن كثب. تتبَّع الفريق أيضاً ناقل النحاس ATP7B، الطافر المتحوِّر في مرض ويلسون، ووجدوا أنه استجاب للنحاس العالي بالتحرك من الحويصلات الداخلية إلى الأسطح المواجهة للصفراوات وبنى شبيهة بالجسيمات الحالة، تماماً كما في الكبد الطبيعي. هذا يبرهن أن العضويّات يمكنها نمذجة كيفية توجيه الخلايا الكبدية للمعادن والجزيئات الأخرى بطريقة مستقطبة.
ماذا يعني هذا لأبحاث الكبد المستقبلية
من خلال استغلال العمل المشترك لمسارات IGF2 وYAP، أنشأ المؤلفون مصدرًا متجدداً من العضويّات الكبدية البشرية التي تتجمع في عناقيد شبيهة بالعنب وتبني شبكات قنوات صفراء وظيفية. وعلى الرغم من أنها لا تزال أقل نضجاً بعض الشيء من نسيج الكبد البالغ وتفتقر إلى خلايا داعمة غير كبدية، فإن هذه البنى تلتقط جوانب رئيسية من تجدد الكبد، والقطبية، والنقل. بالنسبة لغير المتخصصين، يعني هذا أن العلماء يقتربون من أكباد مصغرة مزروعة في المختبر يمكن استخدامها لدراسة أمراض الكبد الوراثية، واختبار سلامة الأدوية — لا سيما السمية المتعلقة بالصفراء — واستكشاف العلاجات الخلوية مستقبلاً، كل ذلك دون الاعتماد حصرياً على الأعضاء المتبرع بها النادرة.
الاستشهاد: Wu, H., Liu, S., Chen, S. et al. Generation of proliferative hESC-derived grape-clustered hepatocyte organoids with multipolar architecture as regenerative counterpart via synergy of YAP and IGF2 pathways. Cell Death Dis 17, 381 (2026). https://doi.org/10.1038/s41419-026-08635-y
الكلمات المفتاحية: عضويّات الكبد, خلايا كبدية مشتقة من الخلايا الجذعية, قنوات الصفراء, تجدد الكبد, إصابة الكبد الناجمة عن الأدوية