Clear Sky Science · ru
Получение пролиферирующих печеночных органоидов с гроздевидной архитектурой из hESC с мультиполярной структурой как регенеративный аналог через синергию путей YAP и IGF2
Создание крошечных печеней в лаборатории
Печень тихо выполняет многие из самых сложных функций организма — обезвреживание лекарств, переработку питательных веществ и управление жирами и сахарами. Однако человеческой печёночной ткани мало, а зрелые печёночные клетки быстро теряют функции в культуре. В этом исследовании описан метод выращивания крошечных, гроздевидных скоплений человеческих печёночных клеток из эмбриональных стволовых клеток, которые не только остаются живыми и делятся в течение недель, но и воспроизводят ключевые черты настоящей печёночной ткани, включая способность направленно перемещать желчь и другие вещества.
Почему важны кластерные печёночные структуры
Учёные давно стремятся создать трёхмерные печёночные «органоиды», которые ведут себя как настоящая печень. Существующие органоиды, получаемые из эпителиальных клеток желчных протоков, склонны формировать полые кисты с простой внутренняя–наружная полярностью, что не соответствует сложной структуре истинных гепатоцитов. В организме каждый гепатоцит имеет несколько «апикальных» поверхностей, которые соединяются с соседями, формируя разветвлённую сеть жёлчных канальцев, одновременно обмениваясь веществами с кровью с противоположной стороны. Гроздевидные гепатоцитарные органоиды, полученные из первичных взрослых печёночных клеток, способны имитировать эту мультиполярную форму и функцию, но они зависят от тканевых доноров, которые ограничены и вариабельны. Новая работа показывает, что аналогичные гроздевидные органоиды можно получить из человеческих эмбриональных стволовых клеток, что обеспечивает потенциально более доступный и стандартизированный источник.
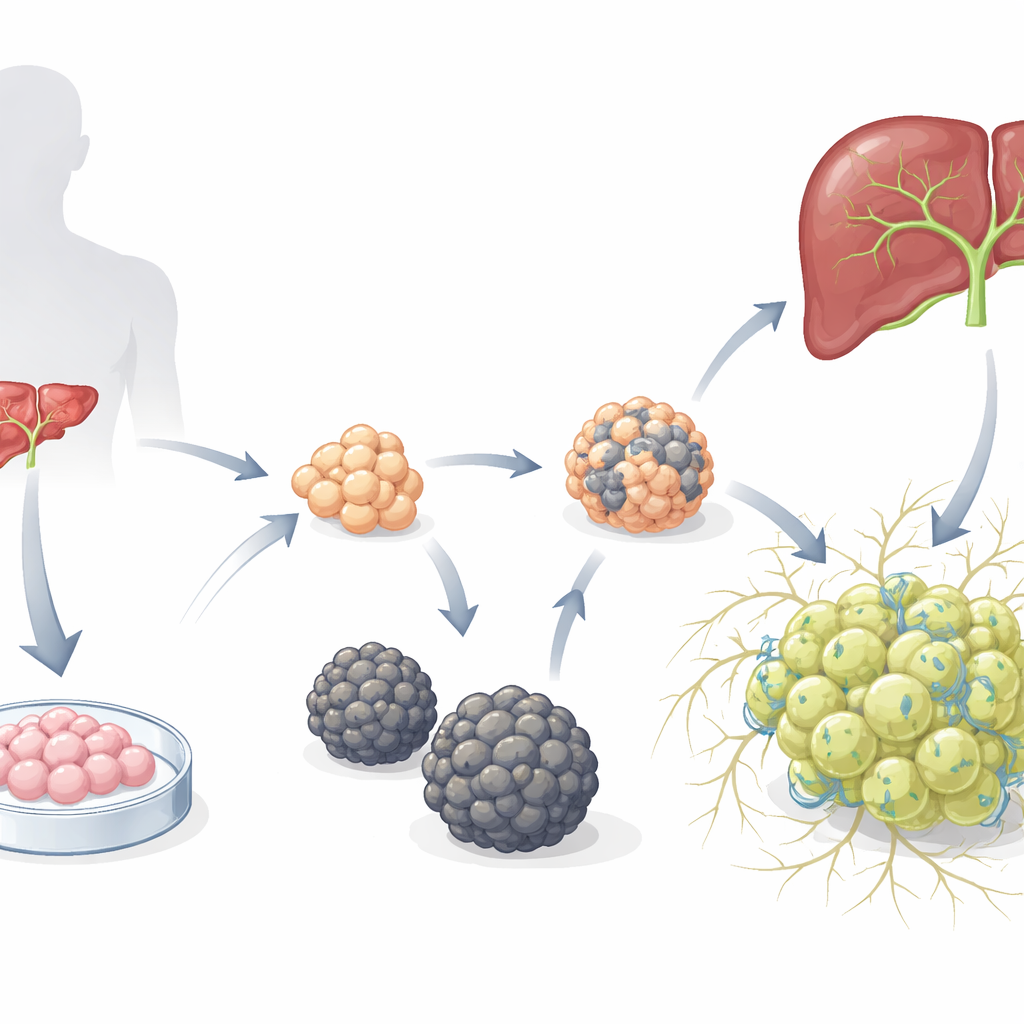
Две принципиально разные мини‑печени
Исследователи начали с ранее полученных органоидов гепатобластов — незрелых печёночных предшественников, выращенных из человеческих эмбриональных стволовых клеток, — и поместили их в среду, благоприятную для развития гепатоцитов. Со временем появились два различных типа органоидов. Один тип сформировал гладкие сферы (S‑heporgs), которые плохо росли, демонстрировали признаки старения и гибели клеток и не организовывали адекватную сеть жёлчных канальцев. Другой тип образовал неправильные, гроздевидные кластеры (G‑heporgs), которые расширялись до нескольких сотен микрометров в поперечнике, содержали много делящихся и биниуклеарных клеток, экспрессировали высокие уровни зрелых печёночных белков, таких как альбумин, и формировали сложные разветвлённые канальцевые структуры между клетками. Генетические и функциональные тесты показали, что G‑heporgs метаболически активны и пролиферируют, тогда как S‑heporgs застряли в состоянии сенесценции, похожем на повреждение.
Воспалительные сигналы, факторы роста и переключатель регенерации
Неожиданным поворотом оказалось то, что терпящие неудачу S‑heporgs, по-видимому, способствовали появлению более успешных G‑heporgs. По мере старения S‑heporgs они выделяли провоспалительные молекулы и создавали микросреду, напоминающую повреждённую печень. В таких условиях G‑heporgs активировали программу роста, сосредоточенную вокруг фактора IGF2 и его рецептора, что, в свою очередь, задействовало путь сигнальной передачи PI3K–AKT, известный как драйвер клеточного деления. Добавление дополнительного IGF2 в культуру увеличивало как количество, так и размер G‑heporgs, тогда как блокирование его рецептора или нижестоящей сигнальной передачи почти полностью их устраняло. Одновременно в G‑heporgs сильно активировался YAP — белок, чувствующий механические и повреждающие сигналы и критически важный для регенерации печени после травмы. Когда команда искусственно усилила активность YAP с помощью маломолекулярного агониста, органоиды можно было расширять более двух месяцев и в многочисленных пассажах без потери гроздевидной архитектуры; выключение YAP резко сокращало рост.
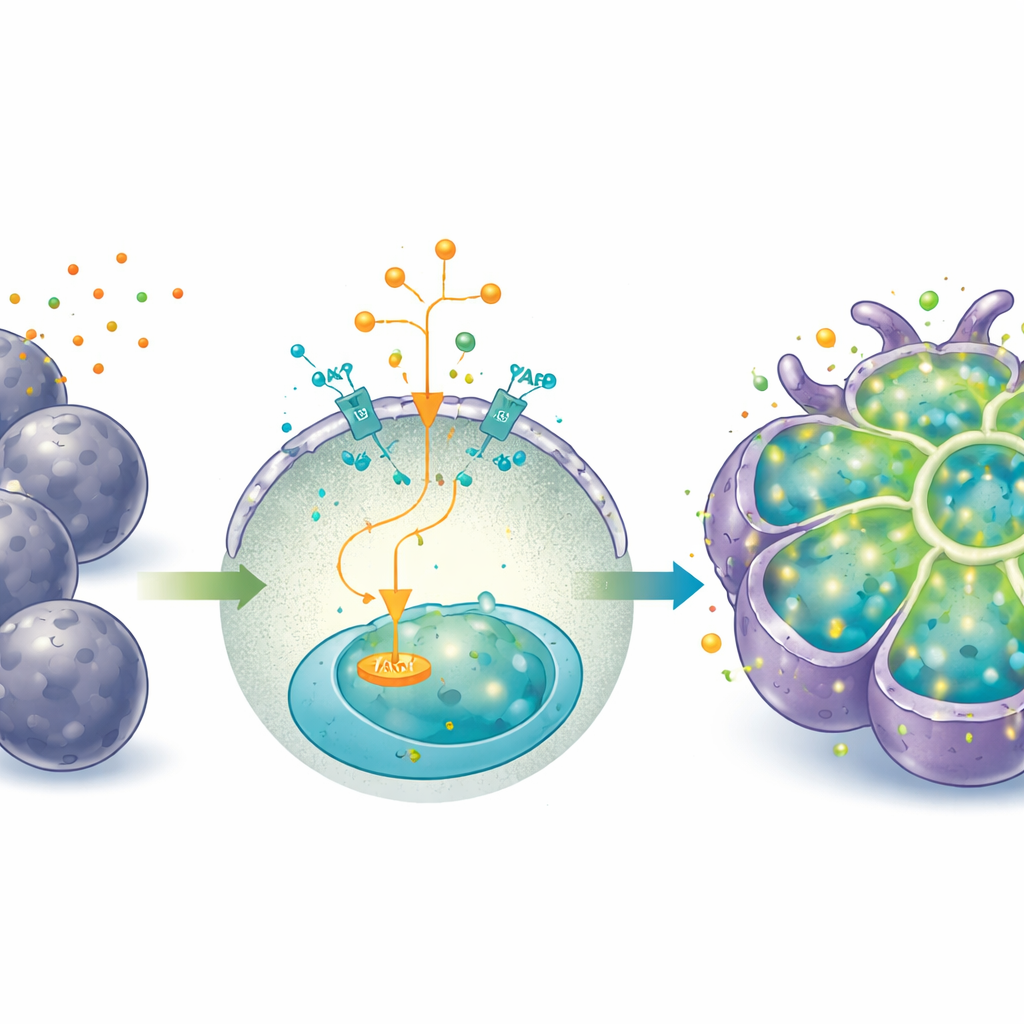
От режима роста к рабочему режиму
Длительная активация YAP, хотя и превосходна для расширения, удерживала клетки в более фетальном, предшественниковом состоянии и ослабляла некоторые зрелые печёночные функции. Чтобы переключить органоиды из «режима роста» в «рабочий режим», исследователи изменили среду — убрали IGF2, агонист YAP и активатор Wnt, добавив гормон дексаметазон и цитокин онкостатин М. При этих условиях органоиды развивали более крупные, многоугольные клетки с меньшим отношением ядро‑к‑цитоплазме и большим количеством биниуклеарных клеток — все признаки созревания гепатоцитов. Они вырабатывали больше альбумина и мочевины, эффективно захватывали и выводили модельный краситель (индоцианиновый зелёный), а также увеличивали уровни ключевых ферментов метаболизма лекарств, особенно после воздействия известных индукторов этих ферментов.
Воссоздание потока желчи и управления металлами
Ключевое достижение этих органоидов — их способность воссоздавать поляризованный транспорт — направленное перемещение веществ на определённые поверхности клетки. Расширяемые G‑heporgs формировали канальцеподобные структуры, помеченные белками, которые обычно концентрируются на апикальных мембранах. Живая визуализация показала, как флуоресцентные тестовые соединения перекачиваются в эти крошечные просветы, а лекарства, известные как вызывающие холестаз у пациентов, нарушали эту канальцевую сеть и приводили к накоплению красителей внутри клеток, что тесно имитирует токсические побочные эффекты в клинике. Команда также отслеживала ATP7B — медиатор транспорта меди, мутировавший при болезни Вилсона, и обнаружила, что в ответ на высокий уровень меди он перемещается из внутренних компартментов на поверхности, обращённые к желчным просветам, и в лизосомоподобные структуры, как и в нативной печени. Это демонстрирует, что органоиды могут моделировать направленную обработку металлов и других молекул гепатоцитами.
Что это значит для будущих исследований печени
Используя совместное действие путей IGF2 и YAP, авторы создали возобновляемый источник человеческих гепатоцитарных органоидов, которые собираются в гроздевидные кластеры и формируют функциональные сети жёлчных канальцев. Хотя они всё ещё несколько менее зрелые, чем ткань взрослой печени, и лишены вспомогательных не‑гепатоцитарных клеток, эти структуры воспроизводят ключевые аспекты регенерации печени, полярности и транспорта. Для неспециалистов это означает, что учёные приблизились к лабораторно выращенным мини‑печеням, которые можно использовать для изучения наследственных заболеваний печени, проверки безопасности лекарств — особенно токсичности, связанной с желчью, — и в перспективе для разработки клеточных терапий, всё это без единственной зависимости от редких донорских органов.
Цитирование: Wu, H., Liu, S., Chen, S. et al. Generation of proliferative hESC-derived grape-clustered hepatocyte organoids with multipolar architecture as regenerative counterpart via synergy of YAP and IGF2 pathways. Cell Death Dis 17, 381 (2026). https://doi.org/10.1038/s41419-026-08635-y
Ключевые слова: печёночные органоиды, гепатоциты, полученные из стволовых клеток, жёлчные канальцы, регенерация печени, лекарственно-индуцированное поражение печени