Clear Sky Science · pl
Generowanie proliferujących organoidów hepatocytów o groniastej architekturze pochodzących z hESC jako regeneracyjny odpowiednik poprzez synergii szlaków YAP i IGF2
Budowanie małych wątrób w laboratorium
Wątroba dyskretnie wykonuje wiele z najtrudniejszych zadań organizmu — detoksykację leków, przetwarzanie składników odżywczych oraz zarządzanie tłuszczami i cukrami. Jednak ludzka tkanka wątroby jest rzadka, a dojrzałe komórki wątrobowe szybko tracą funkcję w hodowli. W tym badaniu opisano sposób hodowli małych, groniastej struktury skupisk ludzkich komórek wątroby pochodzących z embrionalnych komórek macierzystych, które nie tylko pozostają żywe i dzielą się przez tygodnie, ale też odtwarzają kluczowe cechy prawdziwej tkanki wątrobowej, w tym zdolność do ukierunkowanego transportu żółci i innych substancji.
Dlaczego skupiska komórek wątroby mają znaczenie
Naukowcy od dawna dążą do stworzenia trójwymiarowych „organoidów” wątroby, które zachowują się jak prawdziwa tkanka. Istniejące organoidy z komórek przewodów żółciowych mają tendencję do tworzenia pustych cyst z prostą polaryzacją wewnętrzno-zewnętrzną, co nie odzwierciedla złożonej struktury prawdziwych hepatocytów. W organizmie każdy hepatocyt ma kilka powierzchni apikanych, które łączą się z sąsiadami, tworząc rozgałęzioną sieć kanalików żółciowych, jednocześnie wymieniając substancje z krwią po stronie przeciwnej. Groniaste organoidy hepatocytów pochodzące z pierwotnych dorosłych komórek wątroby potrafią naśladować tę multipolarną formę i funkcję, lecz zależą od dawcy, którego materiał jest ograniczony i zmienny. Nowa praca pokazuje, że podobne groniaste organoidy można uzyskać z ludzkich embrionalnych komórek macierzystych, co daje potencjalnie bardziej obfite i ustandaryzowane źródło.
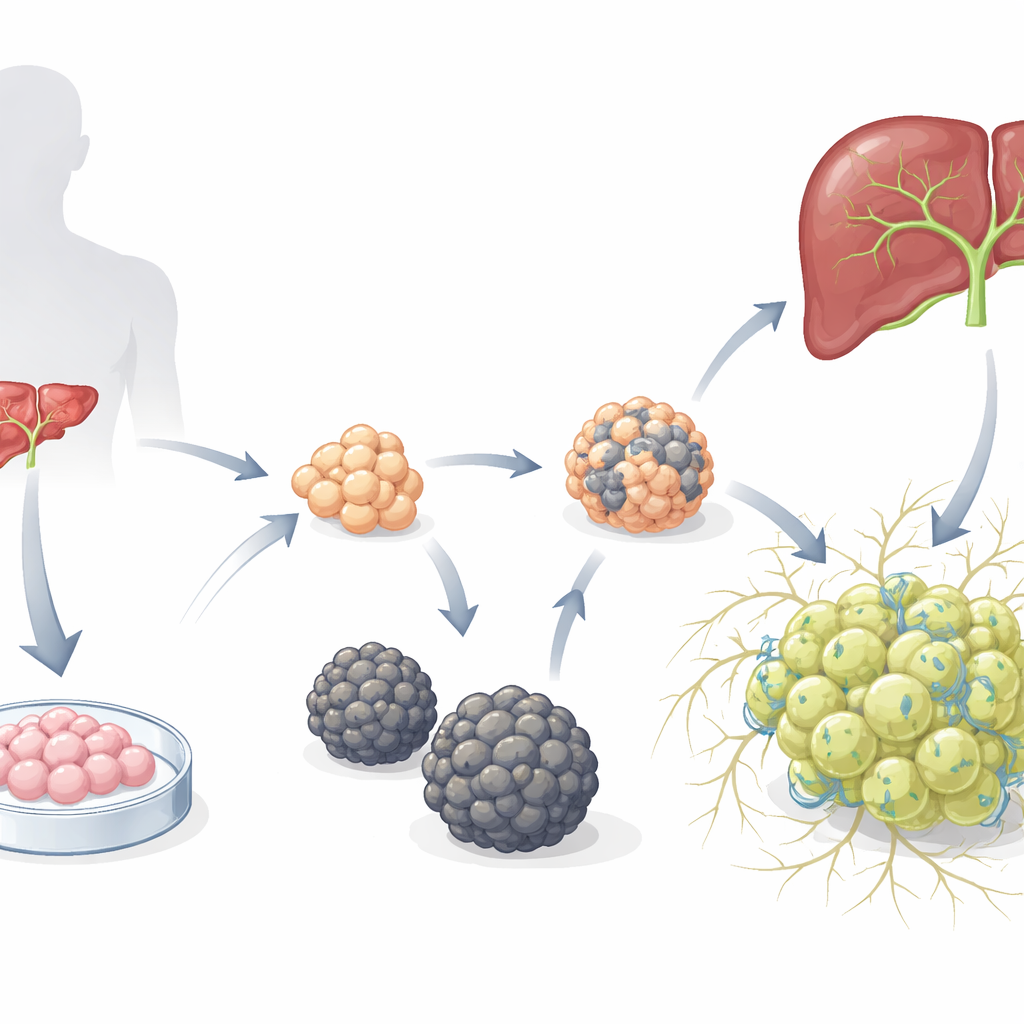
Dwie bardzo różne miniwątrobowe społeczności
Naukowcy rozpoczęli od wcześniej ustanowionych organoidów hepatoblastów — niedojrzałych prekursorów wątroby wyhodowanych z ludzkich embrionalnych komórek macierzystych — i umieścili je w pożywce sprzyjającej rozwojowi hepatocytów. Z upływem czasu pojawiły się dwa odrębne typy organoidów. Jeden typ tworzył gładkie kule (S-heporgs), które słabo rosły, wykazywały oznaki starzenia i śmierci komórkowej oraz nie organizowały prawidłowej sieci kanalików żółciowych. Drugi typ tworzył nieregularne, groniaste skupiska (G-heporgs), które rozrastały się do kilkuset mikrometrów, zawierały wiele dzielących się i dwujądrzastych komórek, wykazywały wysoką ekspresję dojrzałych białek wątroby, takich jak albumina, i budowały złożone, rozgałęzione struktury kanalikowe między komórkami. Testy genetyczne i funkcjonalne wykazały, że G-heporgs były metabolicznie aktywne i proliferujące, podczas gdy S-heporgs utknęły w stanie senesencji przypominającym uraz.
Sygnały zapalne, czynniki wzrostu i przełącznik regeneracji
Niespodziewanym elementem było to, że chybiące S-heporgs wydawały się sprzyjać pojawieniu się bardziej udanych G-heporgs. W miarę starzenia się S-heporgs uwalniały cząsteczki zapalne i tworzyły mikrośrodowisko przypominające uszkodzoną wątrobę. W takim kontekście G-heporgs aktywowały program wzrostu skoncentrowany na czynniku IGF2 i jego receptorze, co z kolei uruchamiało szlak sygnałowy PI3K–AKT znany z napędzania podziałów komórkowych. Dodanie dodatkowego IGF2 do hodowli zwiększało zarówno liczbę, jak i rozmiar G-heporgs, podczas gdy blokada jego receptora lub sygnalizacji poniżej niego niemal je eliminowała. Równocześnie G-heporgs wykazywały silną aktywację YAP, białka wyczuwającego sygnały mechaniczne i uszkodzeniowe, kluczowego dla odrostu wątroby po urazie. Gdy zespół sztucznie zwiększył aktywność YAP za pomocą małocząsteczkowego agonisty, organoidy można było ekspandować przez ponad dwa miesiące i wiele pasaży bez utraty groniastej architektury; wyłączenie YAP gwałtownie ograniczało wzrost.
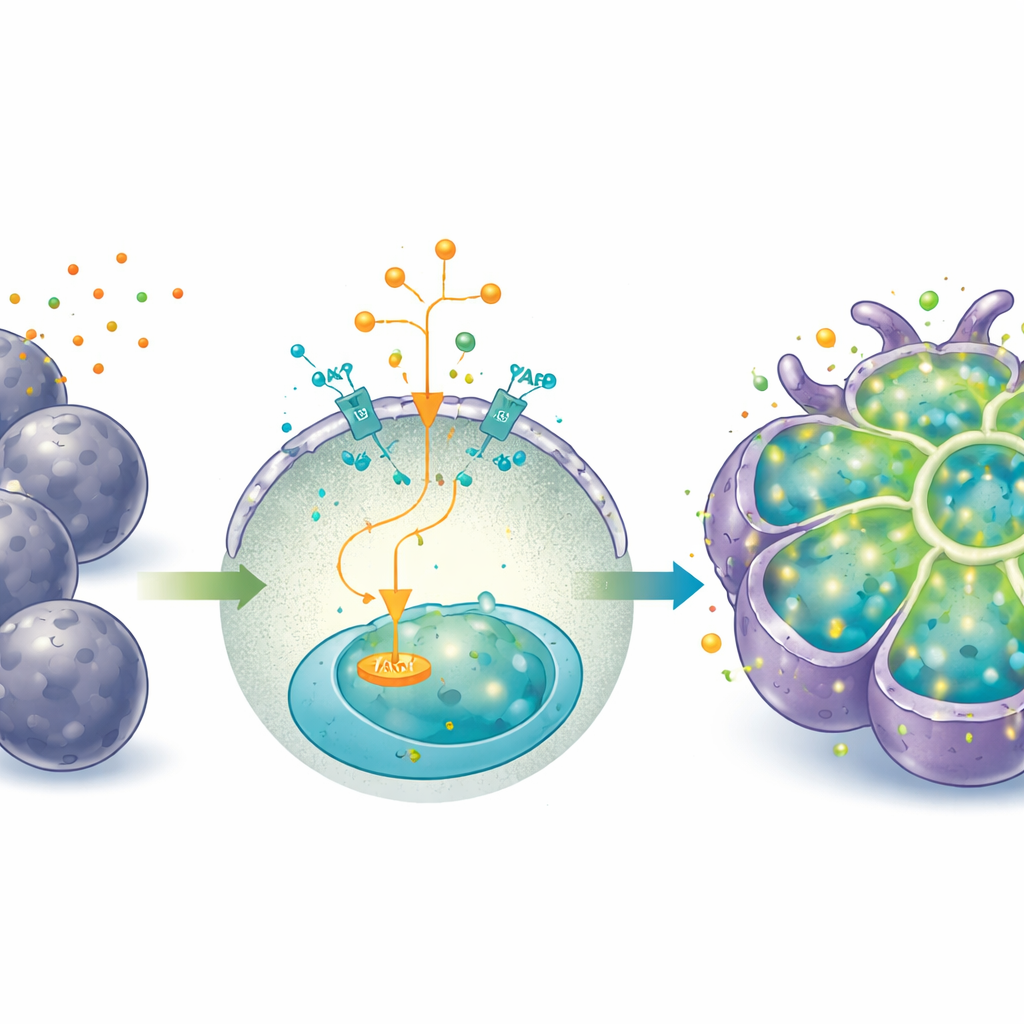
Od trybu wzrostu do trybu pracy
Długotrwała aktywacja YAP, choć doskonała do ekspansji, utrzymywała komórki w bardziej płodowym, prekursorowym stanie i osłabiała niektóre dojrzałe funkcje wątroby. Aby przesunąć organoidy z „trybu wzrostu” do „trybu pracy”, badacze zmienili pożywkę — usunęli IGF2, agonistę YAP i aktywator Wnt, a dodali hormon deksametazon i cytokinę oncostatynę M. W tych warunkach organoidy rozwinęły większe, wielokątne komórki z mniejszym stosunkiem jądro–cytoplazma oraz więcej komórek dwujądrzastych, co są cechy dojrzewających hepatocytów. Produkowały więcej albuminy i mocznika, transportowały modelowy barwnik (indocjaninę zieloną) do wnętrza i na zewnątrz komórek oraz zwiększyły kluczowe enzymy metabolizujące leki, zwłaszcza po ekspozycji na znane induktory enzymatyczne.
Odtwarzanie przepływu żółci i obróbka metali
Centralnym osiągnięciem tych organoidów jest ich zdolność do odtwarzania spolaryzowanego transportu — ukierunkowanego przemieszczania substancji do określonych powierzchni komórki. Ekspandowalne G-heporgs tworzyły kanałopodobne struktury przypominające kanaliki żółciowe, oznakowane białkami zwykle skoncentrowanymi w błonach apikalych. Obrazowanie na żywo pokazało, jak fluorescencyjne związki testowe są pompowane do tych małych lumenów, a leki znane z wywoływania cholestazy u pacjentów zaburzały tę sieć kanalikową i powodowały gromadzenie barwników wewnątrz komórek, ściśle odzwierciedlając toksyczne skutki uboczne obserwowane w klinice. Zespół śledził też ATP7B, transporter miedzi zmutowany w chorobie Wilsona, i zaobserwował, że w odpowiedzi na wysoką zawartość miedzi przemieszcza się z wewnętrznych pęcherzyków na powierzchnie skierowane ku żółci oraz do struktur przypominających lizosomy, podobnie jak w tkance rodzimej wątroby. Pokazuje to, że organoidy mogą modelować sposób, w jaki hepatocyty kierują metalami i innymi cząsteczkami w sposób spolaryzowany.
Co to oznacza dla przyszłych badań nad wątrobą
Dzięki wykorzystaniu skojarzonego działania szlaków IGF2 i YAP autorzy stworzyli odnawialne źródło ludzkich organoidów hepatocytów, które gromadzą się w grona i budują funkcjonalne sieci kanalików żółciowych. Chociaż wciąż są nieco mniej dojrzałe niż tkanka dorosłej wątroby i brakuje im komórek wspierających innych niż hepatocyty, struktury te odzwierciedlają kluczowe aspekty regeneracji wątroby, polaryzacji i transportu. Dla odbiorców niebędących specjalistami oznacza to, że naukowcy zbliżają się do hodowanych w laboratorium miniwątrób, które mogą służyć do badania wrodzonych chorób wątroby, testowania bezpieczeństwa leków — zwłaszcza toksyczności związanej z żółcią — i w końcu eksploracji terapii komórkowych, wszystko bez wyłącznego polegania na rzadkich narządach dawczych.
Cytowanie: Wu, H., Liu, S., Chen, S. et al. Generation of proliferative hESC-derived grape-clustered hepatocyte organoids with multipolar architecture as regenerative counterpart via synergy of YAP and IGF2 pathways. Cell Death Dis 17, 381 (2026). https://doi.org/10.1038/s41419-026-08635-y
Słowa kluczowe: organoidy wątroby, hepatocyty pochodzące z komórek macierzystych, kanalik żółciowy, regeneracja wątroby, uszkodzenie wątroby wywołane lekami