Clear Sky Science · pt
Geração de organoides hepáticos em forma de cachos de uva, derivados de hESC proliferativos, com arquitetura multipolar como contrapartida regenerativa via sinergia das vias YAP e IGF2
Construindo pequenos fígados no laboratório
O fígado realiza discretamente muitas das tarefas mais difíceis do corpo — desintoxicar remédios, processar nutrientes e gerenciar gorduras e açúcares. No entanto, tecido hepático humano é escasso, e células hepáticas maduras perdem rapidamente suas funções em cultura. Este estudo descreve uma maneira de cultivar pequenos aglomerados de células hepáticas humanas em forma de uva a partir de células-tronco embrionárias que não apenas permanecem viáveis e se dividem por semanas, mas também reproduzem características-chave do tecido hepático real, incluindo a capacidade de movimentar bile e outras substâncias de forma altamente organizada.
Por que aglomerados de células hepáticas são importantes
Cientistas há muito tempo buscam construir “organoides” hepáticos tridimensionais que se comportem como tecido hepático real. Organoides existentes derivados de células dos ductos biliares tendem a formar cistos ocos com uma polaridade simples dentro–fora, o que não corresponde à estrutura complexa dos hepatócitos verdadeiros. No organismo, cada hepatócito possui várias superfícies apicais que se juntam às células vizinhas para formar uma rede ramificada de canalículos biliares enquanto, ao mesmo tempo, trocam substâncias com o sangue em seu lado oposto. Organoides em forma de cacho de uva derivados de hepatócitos adultos primários podem imitar essa forma e função multipolar, mas dependem de tecido doador, que é limitado e variável. O trabalho novo mostra que organoides semelhantes em cachos podem ser produzidos a partir de células-tronco embrionárias humanas, oferecendo uma fonte potencialmente mais abundante e padronizada.
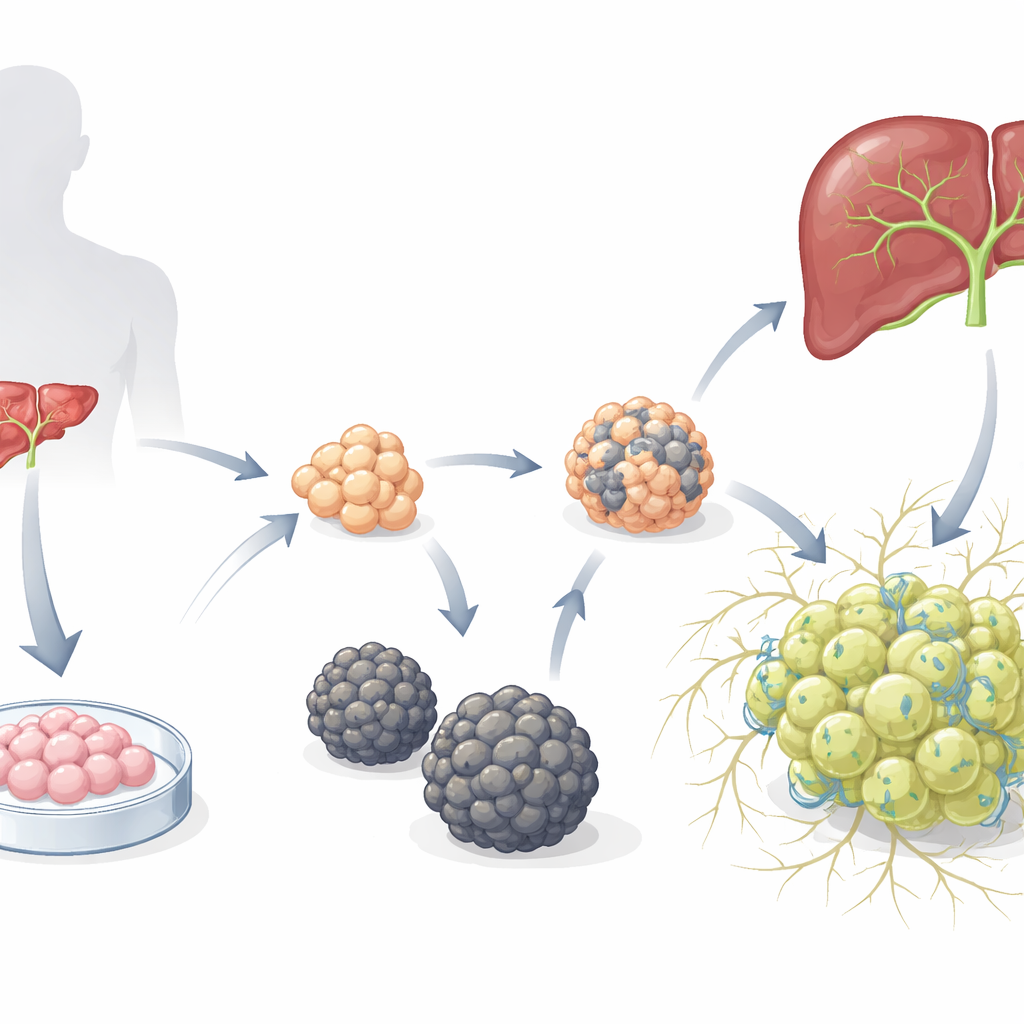
Duas comunidades muito diferentes de mini-fígado
Os pesquisadores partiram de organoides de hepatoblastos já estabelecidos — progenitores hepáticos imaturos cultivados a partir de células-tronco embrionárias humanas — e os colocaram em um meio formulado para favorecer o desenvolvimento de hepatócitos. Com o tempo, emergiram dois tipos distintos de organoides. Um tipo formou esférias lisas (S-heporgs) que cresceram mal, apresentaram sinais de envelhecimento e morte celular e não conseguiram organizar uma rede adequada de canalículos biliares. O outro tipo formou aglomerados irregulares em forma de uva (G-heporgs) que se expandiram até várias centenas de micrômetros, continham muitas células em divisão e binucleadas, expressavam altos níveis de proteínas hepáticas maduras como albumina e construíam estruturas canaliculares intrincadas e ramificadas entre as células. Testes genéticos e funcionais mostraram que os G-heporgs eram metabolicamente ativos e proliferativos, enquanto os S-heporgs estavam presos em um estado senescente, similar a lesão.
Sinais inflamatórios, fatores de crescimento e um interruptor de regeneração
Uma reviravolta inesperada foi que os S-heporgs em falha pareciam ajudar o surgimento dos mais bem-sucedidos G-heporgs. À medida que os S-heporgs envelheciam, liberavam moléculas inflamatórias e criavam um microambiente semelhante ao de um fígado danificado. Nesse contexto, os G-heporgs ativaram um programa de crescimento centrado no fator IGF2 e seu receptor, que por sua vez engajou a via de sinalização PI3K–AKT conhecida por impulsionar a divisão celular. Adicionar IGF2 extra à cultura aumentou tanto o número quanto o tamanho dos G-heporgs, enquanto bloquear seu receptor ou a sinalização a jusante praticamente os eliminou. Ao mesmo tempo, os G-heporgs exibiram forte ativação de YAP, uma proteína que detecta sinais mecânicos e de lesão e é crucial para o crescimento hepático após dano. Quando a equipe aumentou artificialmente a atividade de YAP com um agonista de pequena molécula, os organoides puderam ser expandidos por mais de dois meses e muitas passagens sem perder sua arquitetura em forma de uva; desativar YAP reduziu fortemente o crescimento.
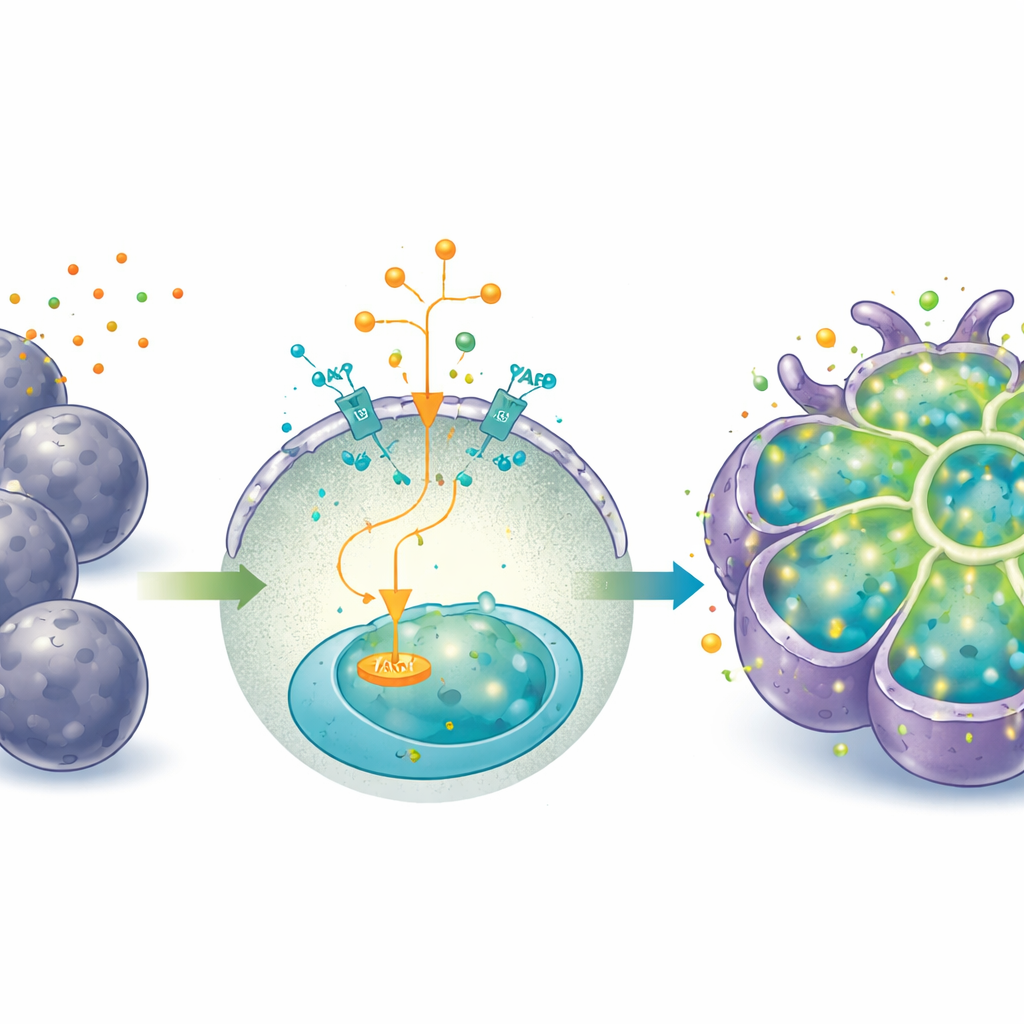
Do modo crescimento ao modo trabalho
A ativação prolongada de YAP, embora excelente para expansão, manteve as células em um estado mais fetal, semelhante a progenitores, e suprimiu algumas funções hepáticas maduras. Para deslocar os organoides do “modo crescimento” para o “modo trabalho”, os pesquisadores mudaram o meio — removendo IGF2, o agonista de YAP e um ativador de Wnt, e adicionando o hormônio dexametasona e a citocina oncostatina M. Nessas condições, os organoides desenvolveram células maiores e poligonais com menor razão núcleo/citoplasma e mais células binucleadas, todos marcos da maturação hepatocitária. Produziram mais albumina e ureia, manejaram um corante modelo (indocianina verde) entrando e saindo das células, e aumentaram enzimas-chave de metabolização de fármacos, especialmente após exposição a indutores conhecidos dessas enzimas.
Recriando o fluxo biliar e o manejo de metais
Uma conquista central desses organoides é sua capacidade de recriar transporte polarizado — o movimento direcionado de substâncias para superfícies específicas da célula. Os G-heporgs expansíveis formaram canais semelhantes a canalículos biliares marcados por proteínas que normalmente se concentram em membranas apicais. Imagens em tempo real mostraram compostos fluorescentes de teste sendo bombeados para esses pequenos lúmens, e fármacos conhecidos por causar colestase em pacientes perturbavam essa rede canalicular e fizeram os corantes se acumularem dentro das células, espelhando de perto os efeitos tóxicos observados na clínica. A equipe também rastreou ATP7B, um transportador de cobre mutado na doença de Wilson, e constatou que em resposta ao cobre alto ele se movia de compartimentos internos para as superfícies voltadas para a bile e para estruturas semelhantes a lisossomos, exatamente como no fígado nativo. Isso demonstra que os organoides podem modelar como os hepatócitos direcionam metais e outras moléculas de forma polarizada.
O que isso significa para futuras pesquisas hepáticas
Ao aproveitar a ação combinada das vias IGF2 e YAP, os autores criaram uma fonte renovável de organoides de hepatócitos humanos que se organizam em cachos de uva e constroem redes funcionais de canalículos biliares. Embora ainda um tanto menos maduros que o tecido hepático adulto e sem células de apoio não-hepatocíticas, essas estruturas capturam aspectos-chave da regeneração hepática, polaridade e transporte. Para não especialistas, isso significa que os cientistas estão mais próximos de mini-fígados cultivados em laboratório que podem ser usados para estudar doenças hepáticas hereditárias, testar a segurança de medicamentos — especialmente quanto à toxicidade relacionada à bile — e, eventualmente, explorar terapias baseadas em células, tudo sem depender exclusivamente de órgãos doadores escassos.
Citação: Wu, H., Liu, S., Chen, S. et al. Generation of proliferative hESC-derived grape-clustered hepatocyte organoids with multipolar architecture as regenerative counterpart via synergy of YAP and IGF2 pathways. Cell Death Dis 17, 381 (2026). https://doi.org/10.1038/s41419-026-08635-y
Palavras-chave: organoides hepáticos, hepatócitos derivados de células-tronco, canais biliares, regeneração do fígado, lesão hepática induzida por fármacos