Clear Sky Science · zh
骨膜线粒体DNA结构驱动与衰老相关的骨骼修复不良
为什么老年人的骨折难以愈合
随着年龄增长,一次简单的跌倒可能导致骨折,而这些骨折往往不能完全正常愈合。医生每天都能见到这种情况,但细胞内部的根本原因一直不清楚。这项研究揭示了一个出人意料的罪魁祸首:存在于骨修复细胞微小能量工厂中的异常DNA结,以缓慢累积的方式破坏愈合过程。
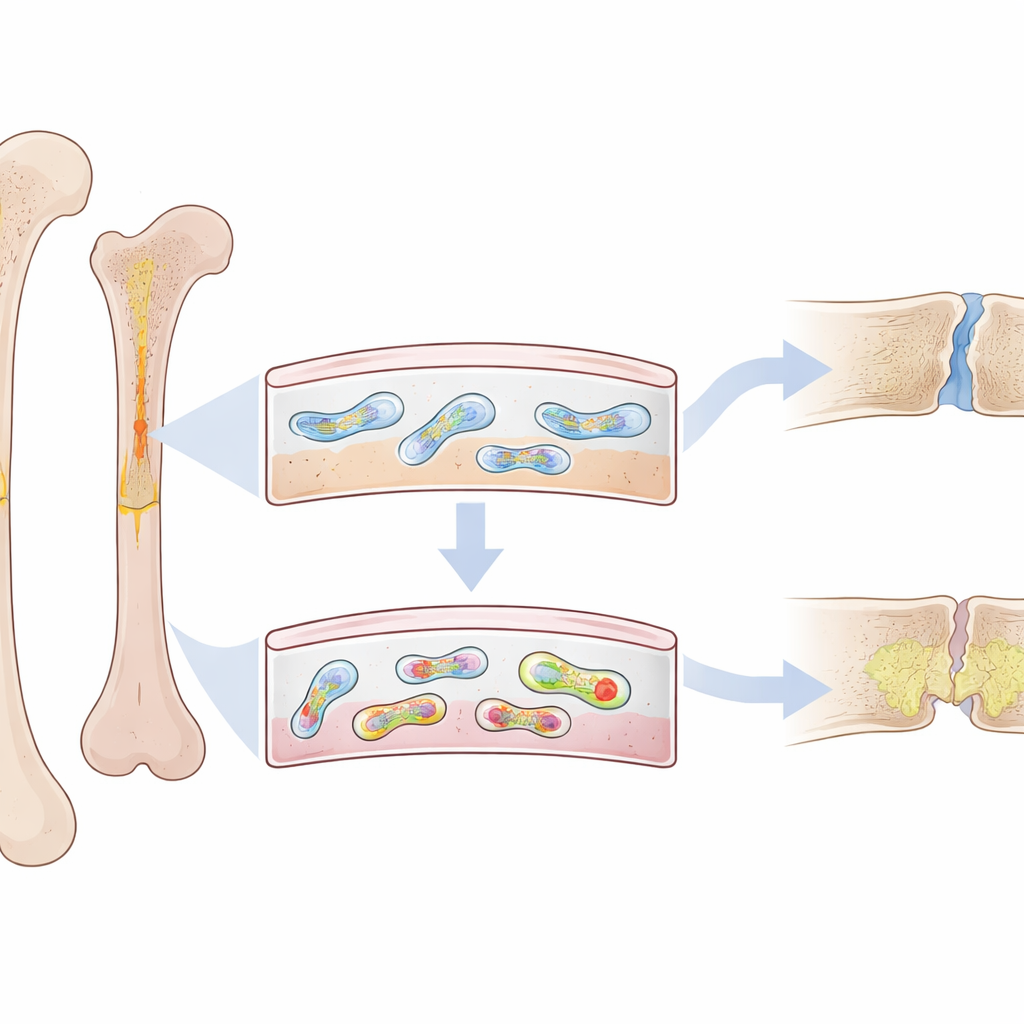
一层薄膜却承担重大职责
在每块骨头外侧都有一层纤维状的薄皮,称为骨膜。它远非仅是包覆物,而是包含一类特殊的类干细胞,这些细胞在骨折后迅速介入重建骨组织。在年轻成人中,这些骨膜细胞高度活跃,能迅速形成坚固的新骨。但在年长者——以及早衰动物模型中——修复更慢、更脆弱,更容易留下被柔软易损组织填充的空隙。研究者怀疑,骨膜细胞内部随着年龄变化的某些因素,使它们偏离了健康的重建路径。
细胞能量工厂中的微小DNA结
研究团队将注意力放在线粒体上——细胞内的能量工厂,它们携带着自身的小环状DNA。线粒体DNA中的某些序列可以折叠成紧密的四股结构,称为G-四链体。借助一种高专一性的荧光探针,科学家在小鼠骨组织中绘制了这些结构的分布图。他们发现,这些称为mtG4的DNA结随年龄在骨膜中选择性累积——无论是正常老龄小鼠,还是早衰基因模型。值得注意的是,这种累积在通常负责骨折修复的骨膜干细胞中最为明显。
从能量危机到“衰老”细胞
为了弄清mtG4的实际作用,研究人员分离出骨膜干细胞并将其培养成微小的三维类器官——模仿早期骨折修复的小型组织。通过短暂暴露于钾离子(可稳定G-四链体结构),他们在不直接损伤细胞的情况下促进了mtG4的形成。结果惊人:关键的线粒体基因表达下降,能量产出(ATP)减少,线粒体呈肿胀和损伤状态,且常被回收结构吞噬,进入称为线粒体自噬的过程。这些受压细胞表现出细胞衰老的特征——停止分裂,表达典型的“衰老”标志,并释放大量可伤害周围组织的炎性分子。
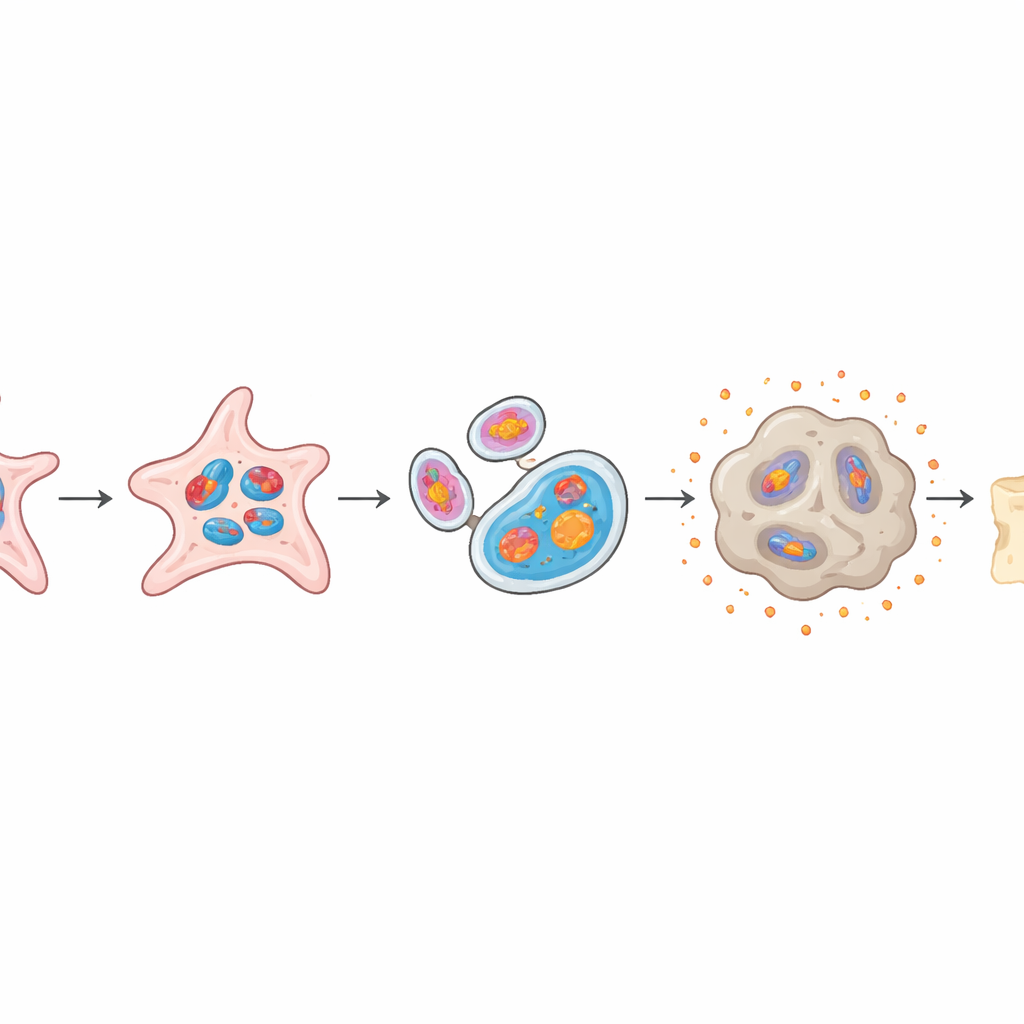
当修复细胞走上错误路径
健康的骨膜干细胞可以选择分化为坚硬、矿化的骨组织或具有弹性的软骨,这种平衡对正确愈合至关重要。在类器官模型中,富含mtG4的细胞丧失了大量成骨能力,表现为矿化减少和骨相关基因表达下降。与此同时,它们更易形成类软骨组织,出现更大、更成熟的软骨簇。当这些富含mtG4的类器官移植到小鼠体内时,产生的新骨远少于正常类器官,忠实再现了老龄动物所见的修复不良现象。
将DNA结构与脆弱骨联系起来
最后,研究团队检验了该机制是否真正驱动活体动物中类似年龄的骨问题。在携带一种使线粒体DNA不稳定并促进mtG4形成的突变小鼠中,骨折愈合不良:新生骨薄且多孔、力学强度差,而本应形成坚固骨组织的部位却滞留软骨。在这些实验中,一个模式反复出现——凡是骨膜干细胞中累积mtG4的地方,线粒体功能受损、细胞变为衰老样状态,骨修复就受到了影响。
这对健康衰老意味着什么
这项研究表明,线粒体DNA内的特殊DNA结可以像分子刹车一样抑制骨修复,尤其是在骨膜中。随着mtG4结构随年龄累积,它们耗尽干细胞的能量,使其过早进入“衰老”状态,并将愈合偏向于形成柔软的软骨而非坚固的骨。通过将mtG4精确定位为一种组织特异性标志物和有害衰老细胞的驱动因子,这项工作指出了未来治疗的新方向:开发能阻止或逆转这些线粒体DNA结的药物,或选择性清除富含mtG4的衰老细胞,或许有朝一日能帮助老年患者更快、更稳固地愈合骨折。
引用: Wu, Y., Han, C., Yang, X. et al. Periosteal mitochondria DNA structures drive aging-associated poor skeletal repair. Bone Res 14, 40 (2026). https://doi.org/10.1038/s41413-026-00524-6
关键词: 骨修复, 衰老, 线粒体, 干细胞, 细胞衰老