Clear Sky Science · ja
骨膜のミトコンドリアDNA構造が加齢に伴う骨の修復不全を駆動する
なぜ高齢になると骨折が治りにくくなるのか
年をとると、ちょっとした転倒で生じた骨折が完全には治らないことがよくあります。臨床では頻繁に見られる現象ですが、その細胞内における根本的原因ははっきりしていませんでした。本研究は、骨の修復を担う細胞の小さな発電所の内部にひそむ意外な犯人――時間とともに静かに蓄積し治癒を妨げる異常なDNAの結び目――を明らかにしました。
薄い層に秘められた大きな役割
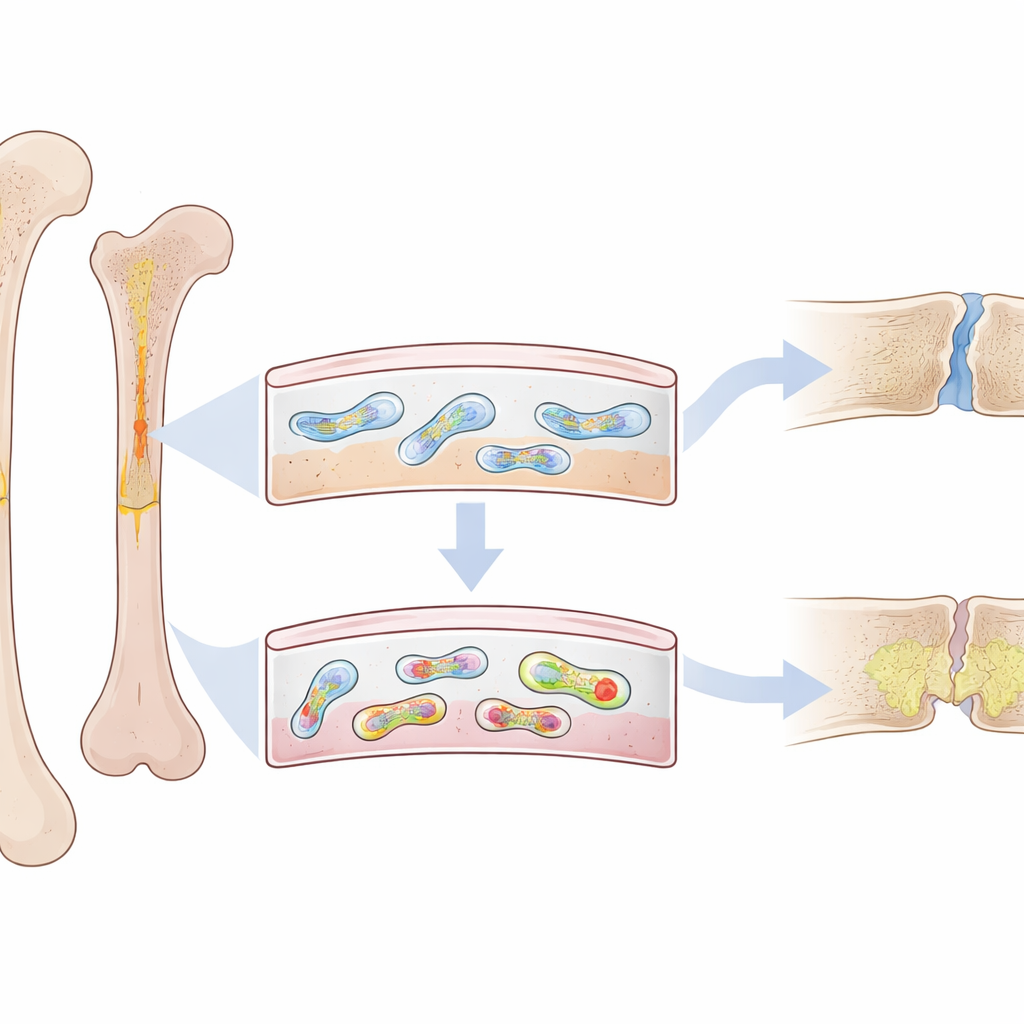
骨の表面には骨膜と呼ばれる薄く繊維状の膜があります。単なる包みではなく、骨折後に骨を再生するために駆け付ける幹様細胞群を抱えています。若年成人ではこれらの骨膜細胞は高い活性を示し、迅速に新しい硬い骨を形成します。しかし高齢者や早期老化モデルの動物では、修復は遅く弱くなり、柔らかく脆い組織で隙間が残りやすくなります。研究者らは、骨膜細胞内部で加齢とともに何かが変化し、健康な再生から逸れてしまうのではないかと疑いました。
細胞の発電所にできる小さなDNAの結び目
研究チームはミトコンドリアに注目しました。ミトコンドリアは細胞内のエネルギー工場であり、独自の小さな環状DNAを持っています。ミトコンドリアDNAの特定の配列はG-四重鎖(G-quadruplex)として知られる緊密な四本鎖構造に折りたたまれることがあります。高選択性の蛍光プローブを用いてマウスの骨でこれらの構造を可視化したところ、このDNA結び目(mtG4と呼ばれる)が加齢に伴い骨膜に選択的に蓄積することが明らかになりました――通常の老齢マウスでも、早期老化の遺伝子モデルでも同様でした。重要なのは、この蓄積が骨折修復を担う骨膜幹細胞で最も顕著だった点です。
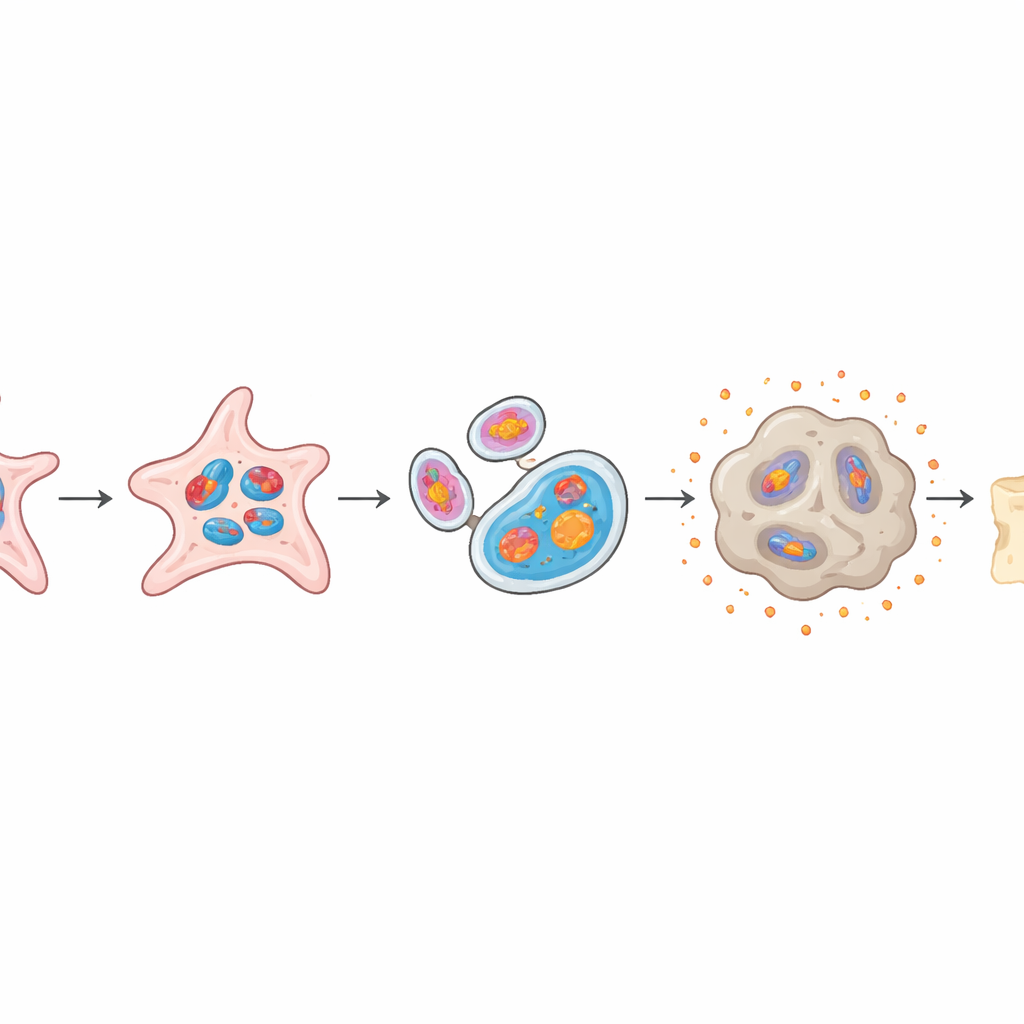
エネルギー危機から「老化」した細胞へ
mtG4が実際にどのような影響を与えるかを検証するため、研究者らは骨膜幹細胞を単離し、小さな3次元オルガノイド(初期の骨折修復を模したミニ組織)に成長させました。カリウムで一時的に処理するとG-四重鎖が安定化し、細胞を傷つけることなくmtG4の形成が促進されました。その結果は顕著でした:重要なミトコンドリア遺伝子の発現が低下し、エネルギー産生(ATP)が減少し、ミトコンドリア自体は膨張・損傷し、しばしばミトファジーと呼ばれるリサイクル機構によって取り込まれていました。こうしたストレスを受けた細胞は細胞老化の特徴を示すようになり――増殖を停止し、古典的な「老化」マーカーを発現し、周囲の組織に損傷を与え得る高レベルの炎症性分子を放出しました。
修復細胞が誤った選択をする時
健全な骨膜幹細胞は硬い石灰化した骨になる道と、柔軟な軟骨になる道を選べますが、そのバランスが適切な治癒には不可欠です。オルガノイドモデルでは、mtG4が過剰な細胞は骨形成能力を大きく失い、石灰化の蓄積が減り、骨関連遺伝子の発現も低下しました。同時に軟骨様組織を形成しやすくなり、より大きく成熟した軟骨クラスターを作りました。これらのmtG4多量のオルガノイドをマウスに移植すると、新しい骨の形成は通常のオルガノイドに比べてはるかに少なく、加齢動物で見られる修復不全を忠実に再現しました。
DNA構造と脆弱な骨との関連
最後に、このメカニズムが生体内で加齢様の骨問題を実際に引き起こすかを検証しました。ミトコンドリアDNAを不安定化させmtG4形成を促進する変異を持つマウスでは、骨折はうまく治りませんでした:新生骨は薄く多孔性で機械的に弱く、本来硬い骨ができるべき部位に軟骨が残存しました。これらの実験を通じて一つのパターンが浮かび上がりました――骨膜幹細胞にmtG4が蓄積するところでは常にミトコンドリアが機能不全に陥り、細胞は老化し、骨修復が損なわれるのです。
健康的な加齢に向けての示唆
本研究は、ミトコンドリアDNA内の特別なDNA結び目が、特に骨膜において骨修復に対する分子的なブレーキのように働き得ることを示しています。mtG4構造が加齢とともに蓄積すると、幹細胞のエネルギーを奪い、これらを早期に「老いた」状態へと押し込み、強い骨ではなく柔らかい軟骨へと治癒を偏らせます。組織特異的な有害な老化細胞のマーカーかつ駆動因子としてmtG4を特定したことで、将来的な治療の新たな道が示されました:ミトコンドリアDNAのこれらの結び目を防いだり解消したりする薬や、mtG4を多く含む老化細胞を選択的に除去する方法が開発されれば、高齢患者の骨折治癒をより速く、より確実にする助けになる可能性があります。
引用: Wu, Y., Han, C., Yang, X. et al. Periosteal mitochondria DNA structures drive aging-associated poor skeletal repair. Bone Res 14, 40 (2026). https://doi.org/10.1038/s41413-026-00524-6
キーワード: 骨修復, 加齢, ミトコンドリア, 幹細胞, 細胞性老化