Clear Sky Science · ru
Структуры митохондриальной ДНК периоста приводят к ухудшению заживления костей при старении
Почему переломы хуже заживают в пожилом возрасте
По мере старения даже простое падение может привести к перелому, который никогда не заживает полностью. Врачи сталкиваются с этим ежедневно, но коренная причина на уровне клеток долгое время оставалась неясной. В этом исследовании обнаружен неожиданный виновник, скрывающийся глубоко в крошечных «электростанциях» клеток, отвечающих за восстановление кости — необычные узлы ДНК, которые постепенно накапливаются и подрывают процессы заживления.
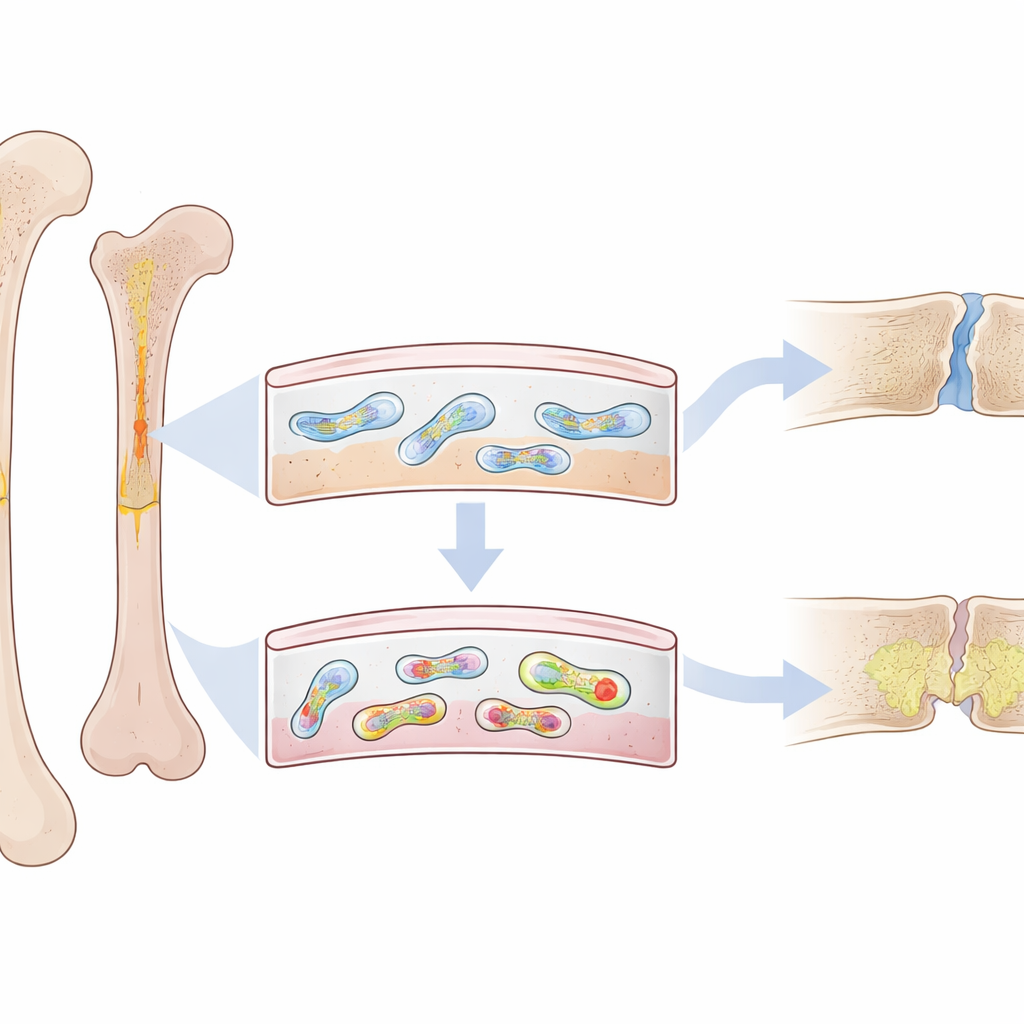
Тонкий слой с большой задачей
Снаружи каждая кость покрыта тонкой волокнистой оболочкой — периостом. Это не просто обёртка: в ней находится особая группа стволоподобных клеток, которые устремляются к месту перелома и восстанавливают кость. У молодых взрослых периостальные клетки очень активны и быстро формируют новую плотную кость. Но у пожилых людей — и у животных с преждевременным старением — восстановление идет медленнее, слабее и чаще оставляет пробелы, заполненные мягкой и хрупкой тканью. Исследователи предположили, что с возрастом в этих периостальных клетках происходят внутренние изменения, смещающие их от здорового восстановления.
Маленькие узлы ДНК в энергетических станциях клетки
Команда сосредоточилась на митохондриях — энергетических фабриках клетки, которые содержат собственные небольшие кольца ДНК. Некоторые участки митохондриальной ДНК способны сворачиваться в плотные четырехцепочечные структуры, известные как G-квадруплексы. С помощью высокоспецифичного флуоресцентного зонда учёные картировали эти структуры в костях мышей. Они обнаружили, что эти «узлы» ДНК, названные mtG4, избирательно накапливаются в периосте по мере старения — как у нормально старых мышей, так и в генетической модели преждевременного старения. Важно, что накопление было наиболее выражено в периостальных стволовых клетках, которые обычно ведут восстановление при переломе.
От энергетического кризиса к «старым» клеткам
Чтобы установить, что именно делает mtG4, исследователи выделили периостальные стволовые клетки и вырастили их в небольших 3D-органоидах — мини-тканях, имитирующих ранние этапы восстановления при переломе. Кратковременное воздействие калием, стабилизирующим G-квадруплексы, усилило образование mtG4, не причиняя иначе заметного вреда клеткам. Последствия были впечатляющими: активность ключевых митохондриальных генов снижалась, выработка энергии (АТФ) падала, а сами митохондрии набухали и повреждались, часто утилизируясь через митофагию. Эти напряжённые клетки приобретали признаки клеточного старения — прекращение деления, экспрессию классических маркеров сенесценции и выброс высоких уровней провоспалительных молекул, вредящих окружающим тканям.
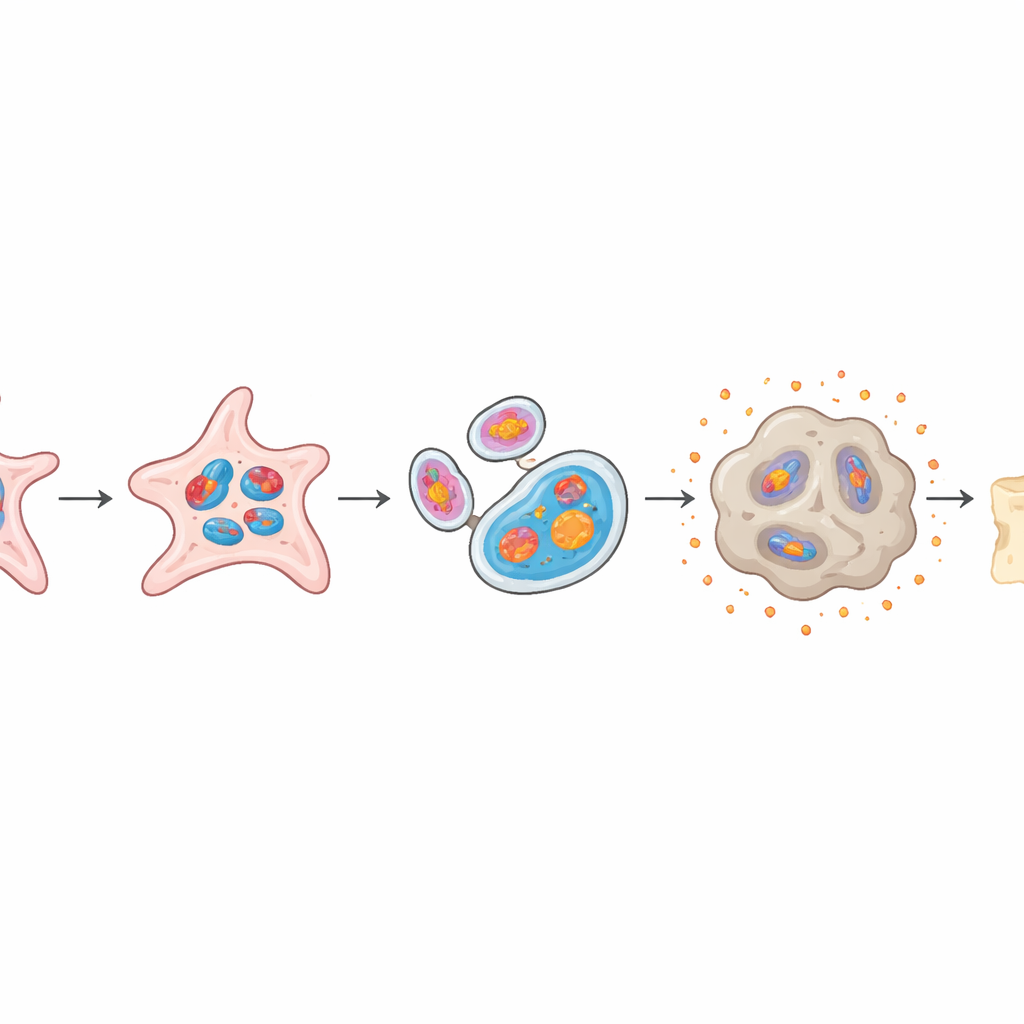
Когда клетки восстановления выбирают неправильный путь
Здоровые периостальные стволовые клетки могут дифференцироваться в твёрдую, минерализованную кость или в гибкий хрящ; равновесие между этими путями критично для правильного заживления. В модели органоидов клетки, перегруженные mtG4, потеряли большую часть способности формировать кость: наблюдалось меньше минерализации и пониженная активность костно-ассоциированных генов. Одновременно они стали более склонны к образованию хрящевой ткани, формируя более крупные и зрелые хрящевые скопления. Когда такие mtG4-насыщенные органоиды пересаживали мышам, они давали значительно меньше новой кости по сравнению с нормальными органоидами, верно воспроизводя плохое заживление, наблюдаемое у стареющих животных.
Связь структур ДНК с хрупкими костями
В завершение команда проверила, действительно ли этот механизм вызывает возрастоподобные проблемы с костями в живом организме. У мышей с мутацией, стабилизирующей образование mtG4 в митохондриальной ДНК, переломы заживали плохо: новая кость была тонкой, пористой и механически слабой, в то время как хрящ сохранялся там, где должна была образоваться твёрдая кость. Во всех экспериментах проявлялась одна закономерность — где бы ни накапливались mtG4 в периостальных стволовых клетках, там митохондрии отказывали, клетки становились сенесцентными, и восстановление кости страдало.
Что это означает для здорового старения
Исследование показывает, что специфические «узлы» ДНК внутри митохондрий могут действовать как молекулярные тормоза для восстановления кости, особенно в периосте. По мере накопления mtG4 с возрастом они истощают энергию стволовых клеток, переводят их в преждевременно «старое» состояние и смещают исцеление в сторону мягкого хряща вместо прочной кости. Выделив mtG4 как тканеспецифический маркер и драйвер вредоносных сенесцентных клеток, работа открывает новый возможный путь для терапии: препараты, предотвращающие образование или расщепляющие эти узлы митохондриальной ДНК, либо селективно удаляющие mtG4-нагруженные сенесцентные клетки, в перспективе могут помочь пожилым пациентам быстрее и надежнее заживать после переломов.
Цитирование: Wu, Y., Han, C., Yang, X. et al. Periosteal mitochondria DNA structures drive aging-associated poor skeletal repair. Bone Res 14, 40 (2026). https://doi.org/10.1038/s41413-026-00524-6
Ключевые слова: репарация кости, старение, митохондрии, стволовые клетки, клеточное старение