Clear Sky Science · es
Las estructuras del ADN mitocondrial en el periostio impulsan la mala reparación ósea asociada al envejecimiento
Por qué los huesos rotos tienen dificultades para curarse en la vejez
A medida que las personas envejecen, una simple caída puede provocar una fractura que nunca termina de curarse correctamente. Los médicos lo observan a diario, pero la causa raíz dentro de nuestras células ha sido poco clara. Este estudio descubre a un culpable sorprendente, escondido en las diminutas centrales energéticas de las células reparadoras del hueso: nudos inusuales de ADN que se acumulan silenciosamente con el tiempo y sabotean la curación.
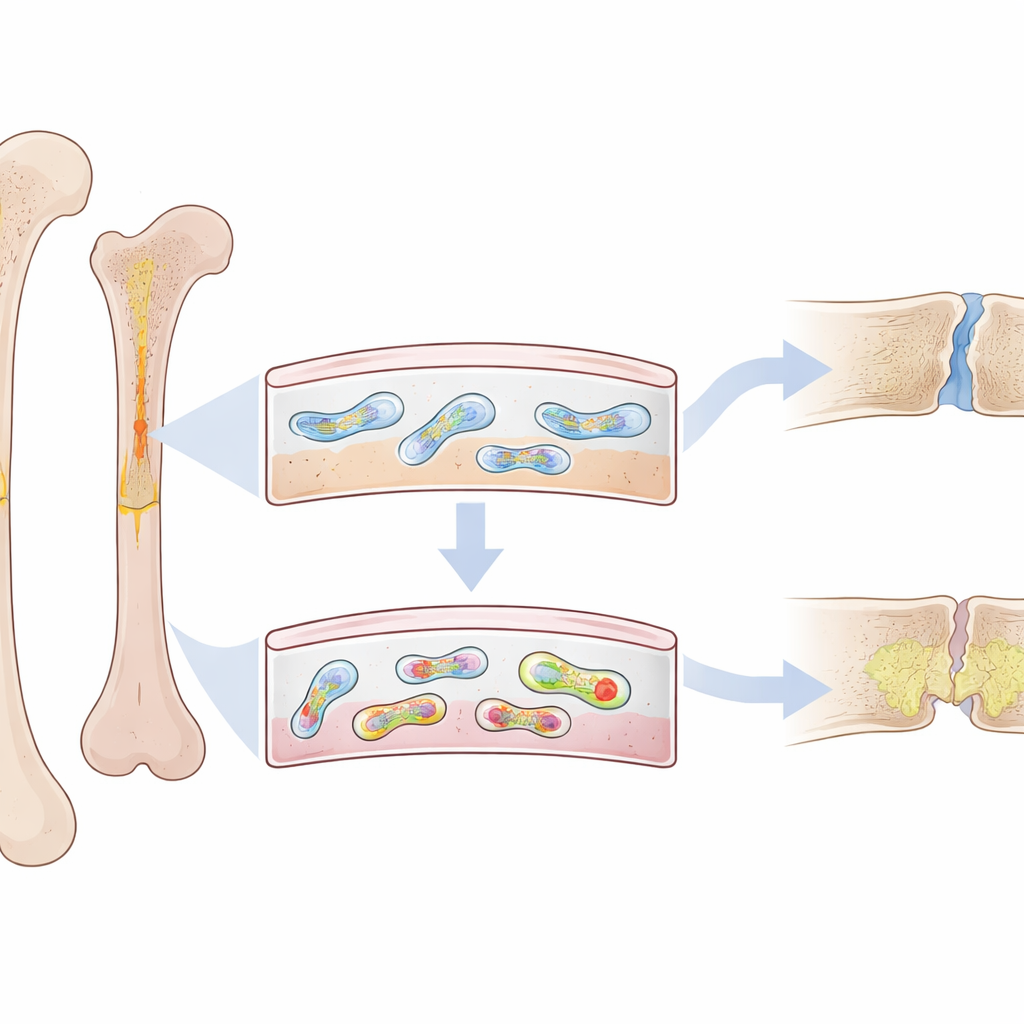
Una capa delgada con una gran función
En el exterior de cada hueso hay una delgada piel fibrosa llamada periostio. Lejos de ser solo un envoltorio, contiene un grupo especial de células con rasgos de células madre que acuden rápidamente a reconstruir el hueso tras una fractura. En adultos jóvenes, estas células periosteales son muy activas y pueden formar hueso nuevo y sólido con rapidez. Pero en personas mayores —y en animales con envejecimiento prematuro— las reparaciones son más lentas, más débiles y con más probabilidad de dejar huecos llenos de tejido blando y frágil. Los investigadores sospecharon que algo dentro de estas células periosteales cambia con la edad, inclinándolas fuera de la vía de una reconstrucción saludable.
Pequeños nudos de ADN en las centrales energéticas celulares
El equipo se centró en las mitocondrias, las fábricas de energía dentro de las células que llevan su propio pequeño anillo de ADN. Ciertos tramos de este ADN mitocondrial pueden plegarse en nudos ajustados de cuatro hebras conocidos como G-cuádruplex. Usando una sonda fluorescente altamente específica, los científicos cartografiaron estas estructuras en huesos de ratón. Descubrieron que estos nudos de ADN, denominados mtG4, se acumulan selectivamente en el periostio a medida que los animales envejecen —tanto en ratones viejos normales como en un modelo genético de envejecimiento prematuro. Importa que esta acumulación fue más intensa en las células madre periosteales que normalmente impulsan la reparación de fracturas.
De la crisis energética a las células “envejecidas”
Para ver qué hacen realmente las mtG4, los investigadores aislaron células madre periosteales y las cultivaron en pequeños organoides 3D —mini tejidos que imitan la reparación temprana de una fractura. Exponiendo brevemente las células al potasio, que estabiliza las estructuras G-cuádruplex, aumentaron la formación de mtG4 sin dañar las células por otros medios. Las consecuencias fueron llamativas: genes mitocondriales clave se volvieron menos activos, la producción de energía (ATP) cayó y las propias mitocondrias se hincharon y dañaron, con frecuencia siendo engullidas por estructuras de reciclaje en un proceso llamado mitofagia. Estas células estresadas adquirieron características del envejecimiento celular: dejaron de dividirse, expresaron marcadores clásicos de senescencia y liberaron altos niveles de moléculas inflamatorias que pueden dañar el tejido cercano.
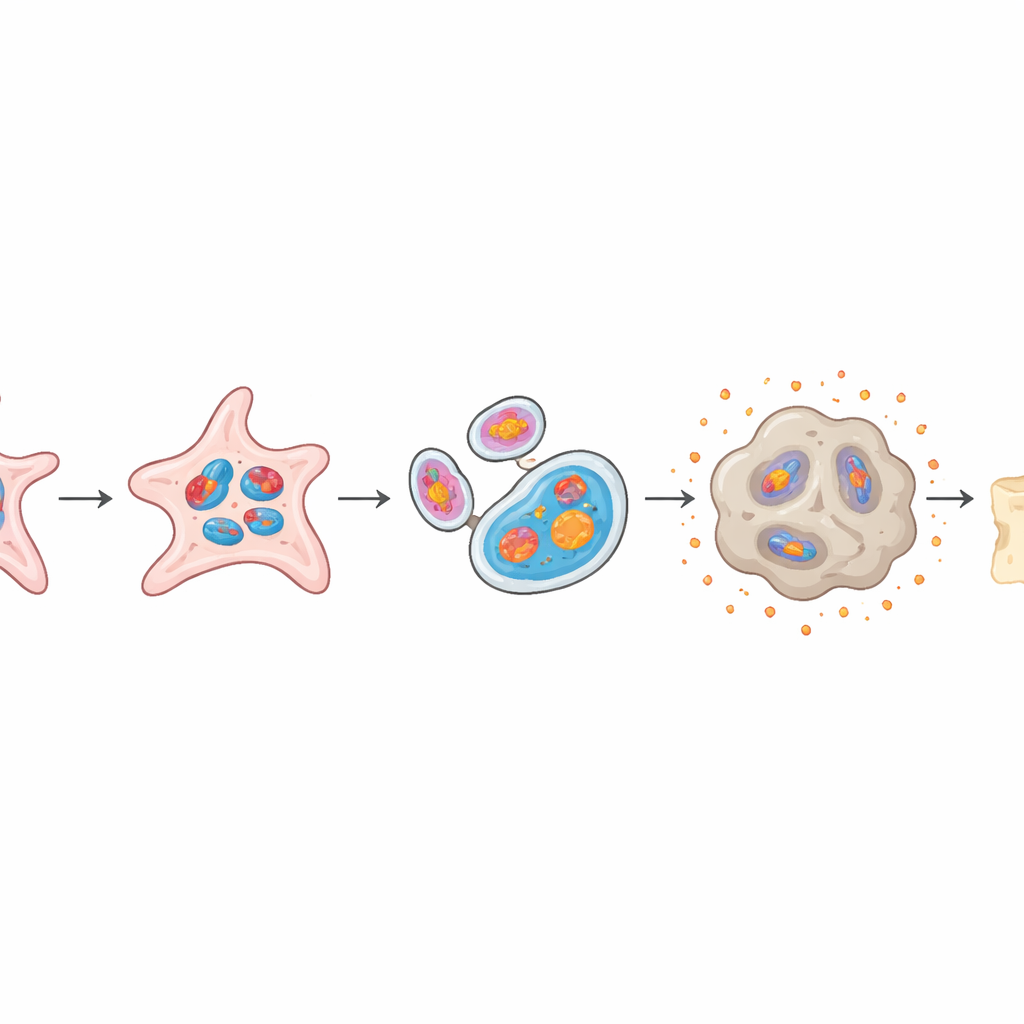
Cuando las células reparadoras eligen el camino equivocado
Las células madre periosteales sanas pueden diferenciarse en hueso duro y mineralizado o en cartílago flexible, y ese equilibrio es crucial para una curación adecuada. En el modelo de organoides, las células sobrecargadas de mtG4 perdieron gran parte de su capacidad para formar hueso, mostrando menos acumulación mineral y niveles más bajos de genes relacionados con el hueso. Al mismo tiempo, se mostraron más proclives a formar tejido similar al cartílago, con cúmulos cartilaginosos más grandes y más maduros. Cuando estos organoides ricos en mtG4 se trasplantaron a ratones, generaron mucho menos hueso nuevo que los organoides normales, reproduciendo fielmente la mala reparación observada en animales envejecidos.
Vinculando estructuras de ADN con huesos frágiles
Por último, el equipo probó si este mecanismo impulsa realmente problemas óseos similares a los del envejecimiento en animales vivos. En ratones portadores de una mutación que desestabiliza el ADN mitocondrial y promueve la formación de mtG4, las fracturas curaron mal: el hueso nuevo era fino, poroso y mecánicamente débil, mientras que el cartílago persistía donde debería haberse formado hueso sólido. A lo largo de estos experimentos surgió un patrón: allí donde mtG4 se acumulaba en las células madre periosteales, las mitocondrias fallaban, las células entraban en senescencia y la reparación ósea se veía comprometida.
Qué significa esto para un envejecimiento saludable
El estudio revela que nudos especiales de ADN dentro del ADN mitocondrial pueden actuar como frenos moleculares sobre la reparación ósea, especialmente en el periostio. A medida que las estructuras mtG4 se acumulan con la edad, drenan la energía de las células madre, las empujan a un estado prematuramente “envejecido” y desvían la curación hacia cartílago blando en lugar de hueso fuerte. Al identificar mtG4 como un marcador y un impulsor específico de tejido de células senescentes dañinas, este trabajo sugiere una nueva vía para futuros tratamientos: fármacos que prevengan o deshagan estos nudos del ADN mitocondrial, o que eliminen selectivamente las células senescentes cargadas de mtG4, podrían algún día ayudar a pacientes mayores a curar fracturas de forma más rápida y segura.
Cita: Wu, Y., Han, C., Yang, X. et al. Periosteal mitochondria DNA structures drive aging-associated poor skeletal repair. Bone Res 14, 40 (2026). https://doi.org/10.1038/s41413-026-00524-6
Palabras clave: reparación ósea, envejecimiento, mitocondrias, células madre, senescencia celular