Clear Sky Science · fr
Structures d’ADN mitochondrial périostées entraînent une mauvaise réparation squelettique liée au vieillissement
Pourquoi les os cassés peinent à se réparer avec l’âge
Avec l’âge, une simple chute peut provoquer une fracture qui ne se consolide jamais correctement. Les médecins l’observent quotidiennement, mais la cause profonde au niveau cellulaire restait floue. Cette étude met en lumière un coupable inattendu niché au cœur des petites centrales énergétiques des cellules réparatrices de l’os : des nœuds d’ADN inhabituels qui s’accumulent progressivement et sabordent la réparation.
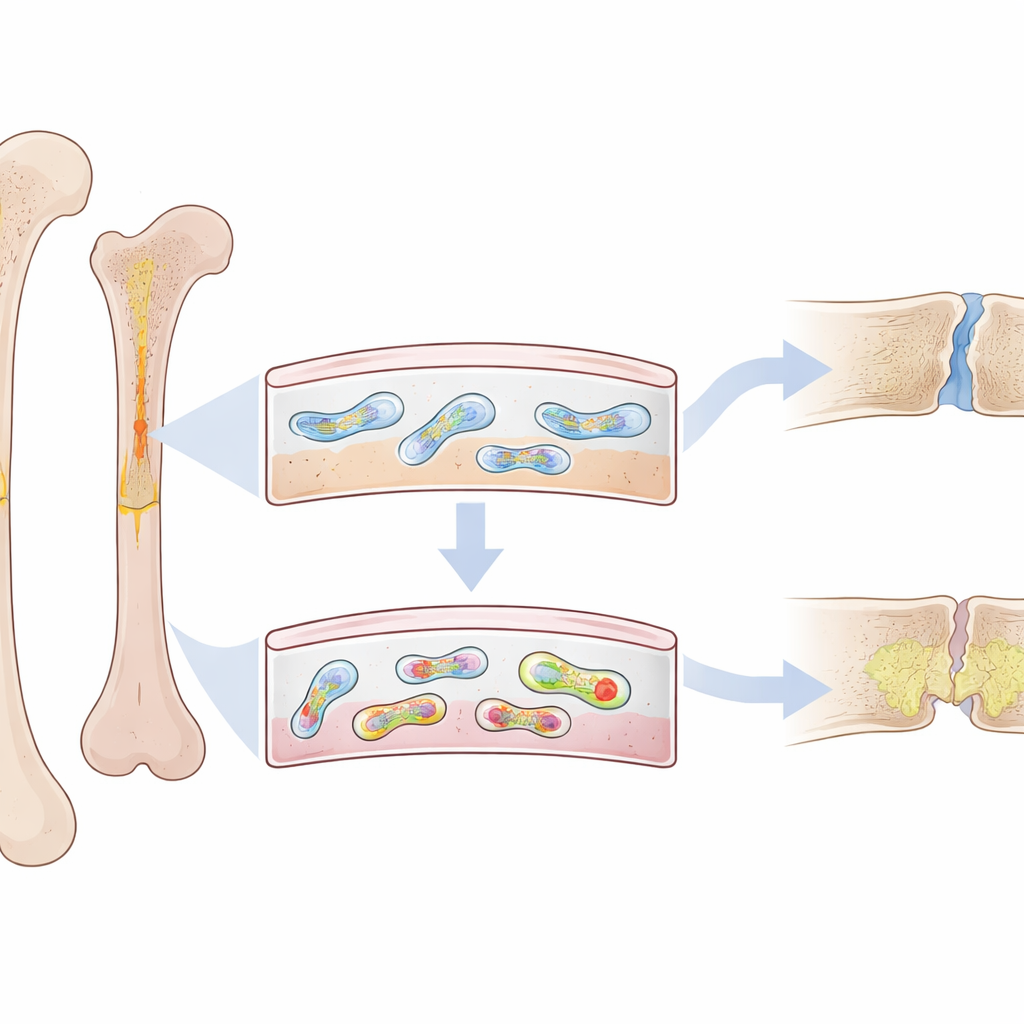
Une fine couche qui a une grande mission
À l’extérieur de chaque os se trouve une fine peau fibreuse appelée périoste. Bien plus qu’un simple enveloppe, elle contient un groupe particulier de cellules à caractère souches qui accourent pour reconstruire l’os après une fracture. Chez les adultes jeunes, ces cellules périostées sont très actives et forment rapidement un os solide. Mais chez les personnes âgées — et chez des animaux présentant un vieillissement prématuré — les réparations sont plus lentes, plus faibles et laissent souvent des zones comblées par un tissu mou et fragile. Les chercheurs ont émis l’hypothèse que quelque chose à l’intérieur de ces cellules périostées change avec l’âge, les détournant d’une reconstruction saine.
De minuscules nœuds d’ADN dans les centrales cellulaires
L’équipe s’est concentrée sur les mitochondries, les usines énergétiques des cellules qui possèdent leur propre petit ADN circulaire. Certains segments de cet ADN mitochondrial peuvent se replier en nœuds serrés à quatre brins appelés G-quadruplexes. À l’aide d’une sonde fluorescente très spécifique, les scientifiques ont cartographié ces structures dans les os de souris. Ils ont découvert que ces nœuds d’ADN, appelés mtG4, s’accumulent de façon sélective dans le périoste avec l’âge — à la fois chez des souris âgées normales et dans un modèle génétique de vieillissement prématuré. De manière importante, cet entassement était le plus prononcé dans les cellules souches périostées qui pilotent normalement la réparation des fractures.
D’une crise énergétique à des cellules « vieillies »
Pour évaluer l’effet réel des mtG4, les chercheurs ont isolé des cellules souches périostées et les ont cultivées sous forme de petits organoïdes tridimensionnels — des mini-tissus qui reproduisent la réparation initiale d’une fracture. En exposant brièvement les cellules au potassium, qui stabilise les structures G-quadruplex, ils ont favorisé la formation de mtG4 sans nuire autrement aux cellules. Les conséquences furent nettes : des gènes mitochondriaux clés voyaient leur expression diminuer, la production d’énergie (ATP) chutait, et les mitochondries elles‑mêmes apparaissaient gonflées et endommagées, souvent englobées par des structures de recyclage dans un processus appelé mitophagie. Ces cellules stressées présentaient des signes caractéristiques du vieillissement cellulaire : arrêt de la division, expression de marqueurs classiques de sénescence et libération élevée de molécules inflammatoires susceptibles d’endommager les tissus voisins.
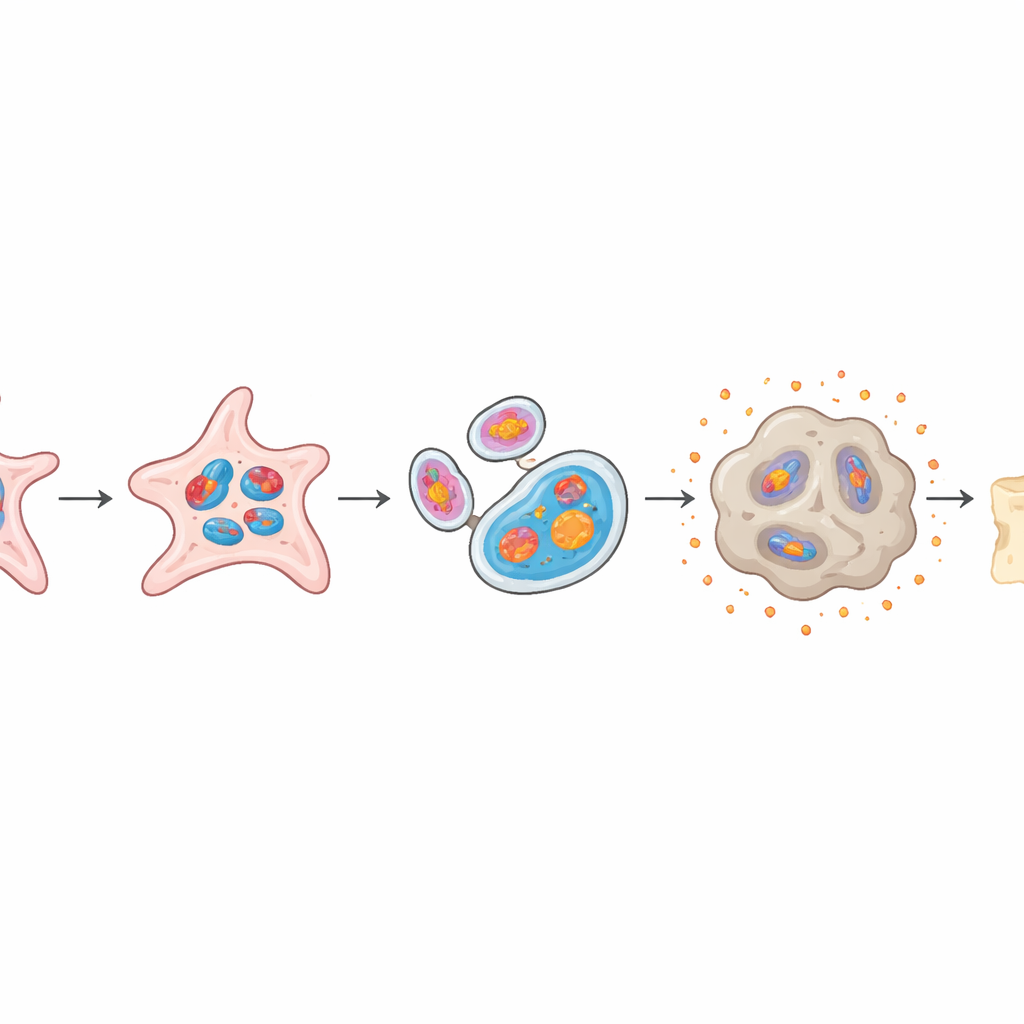
Quand les cellules réparatrices choisissent la mauvaise voie
Les cellules souches périostées saines peuvent différencier soit en tissu osseux minéralisé et rigide, soit en cartilage plus souple, et cet équilibre est crucial pour une bonne guérison. Dans le modèle d’organoïde, les cellules surchargées en mtG4 perdaient une grande partie de leur capacité à former de l’os, montrant moins de dépôt minéral et des niveaux réduits de gènes liés à l’os. Simultanément, elles étaient plus enclines à générer un tissu de type cartilagineux, avec des amas cartilagineux plus volumineux et plus matures. Lorsque ces organoïdes riches en mtG4 furent transplantés chez des souris, ils produisirent beaucoup moins d’os neuf que les organoïdes normaux, reproduisant fidèlement la mauvaise réparation observée chez les animaux âgés.
Relier les structures d’ADN aux os fragiles
Enfin, l’équipe a vérifié si ce mécanisme était bien responsable des problèmes osseux liés à l’âge chez des animaux vivants. Chez des souris porteuses d’une mutation qui déstabilise l’ADN mitochondrial et favorise la formation de mtG4, les fractures consolidaient mal : l’os néoformé était mince, poreux et mécaniquement faible, tandis que le cartilage persistait là où de l’os solide aurait dû se former. À travers ces expériences, un schéma a émergé : partout où mtG4 s’accumulait dans les cellules souches périostées, les mitochondries défaillaient, les cellules devenaient sénescentes et la réparation osseuse était compromise.
Ce que cela signifie pour un vieillissement en bonne santé
L’étude révèle que de véritables nœuds d’ADN au sein de l’ADN mitochondrial peuvent agir comme des freins moléculaires à la réparation osseuse, en particulier dans le périoste. À mesure que les structures mtG4 s’accumulent avec l’âge, elles appauvrissent l’énergie des cellules souches, les poussent vers un état prématurément « vieux » et orientent la réparation vers du cartilage mou plutôt que vers un os solide. En identifiant mtG4 comme un marqueur et un moteur tissulaire de cellules sénescentes néfastes, ce travail ouvre une voie possible pour de futurs traitements : des médicaments qui empêchent ou dénouent ces nœuds d’ADN mitochondrial, ou qui éliminent sélectivement les cellules sénescentes chargées de mtG4, pourraient un jour aider les patients âgés à consolider plus rapidement et plus sûrement leurs fractures.
Citation: Wu, Y., Han, C., Yang, X. et al. Periosteal mitochondria DNA structures drive aging-associated poor skeletal repair. Bone Res 14, 40 (2026). https://doi.org/10.1038/s41413-026-00524-6
Mots-clés: réparation osseuse, vieillissement, mitochondries, cellules souches, sénescence cellulaire