Clear Sky Science · de
Periostale mitochondriale DNA-Strukturen treiben altersbedingte schlechte Knochenheilung voran
Warum gebrochene Knochen im Alter schwerer heilen
Mit zunehmendem Alter kann schon ein einfacher Sturz zu einem Knochenbruch führen, der nie ganz richtig verheilt. Ärztinnen und Ärzte sehen das täglich, doch die zugrunde liegende Ursache in unseren Zellen war lange unklar. Diese Studie deckt einen überraschenden Übeltäter in den winzigen Kraftwerken der knochenbildenden Zellen auf — ungewöhnliche DNA-Knötchen, die sich über die Zeit still ansammeln und die Heilung sabotieren.
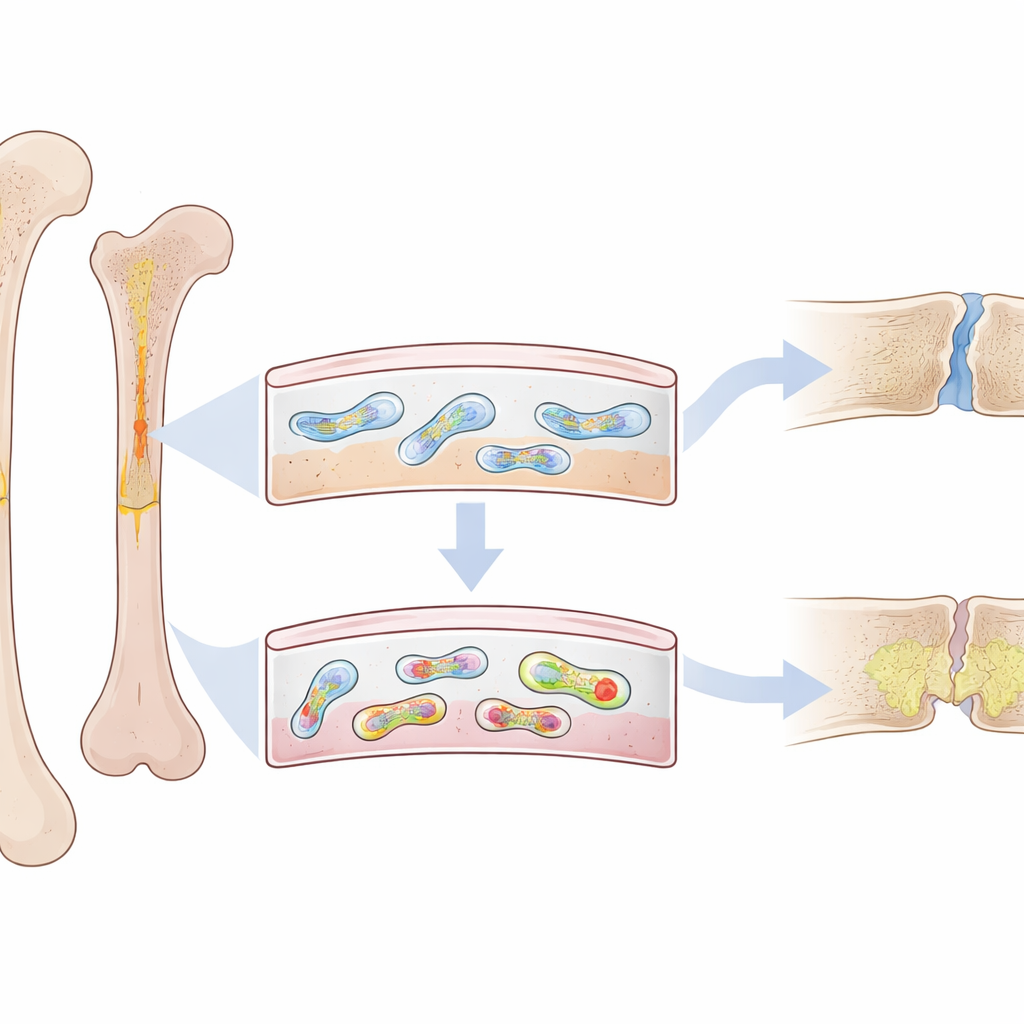
Eine dünne Schicht mit großer Aufgabe
Äußerlich um jeden Knochen liegt eine dünne, faserige Haut, das Periost. Weit davon entfernt, nur eine Hülle zu sein, enthält es eine spezielle Gruppe stammzellähnlicher Zellen, die nach einem Bruch rasch zur Neubildung von Knochen herbeieilen. Bei jungen Erwachsenen sind diese periostalen Zellen sehr aktiv und können schnell neuen, festen Knochen bilden. Bei älteren Menschen — und bei Tieren mit vorzeitigem Altern — verlaufen die Reparaturen langsamer, schwächer und hinterlassen häufiger Lücken mit weichem, fragilen Gewebe. Die Forschenden vermuteten, dass sich in diesen periostalen Zellen mit dem Alter etwas verändert, das sie vom gesunden Wiederaufbau abdrängt.
Winzige DNA-Knötchen in den Zellkraftwerken
Das Team konzentrierte sich auf Mitochondrien, die Energiemanufakturen in den Zellen, die eigene kleine DNA-Ringe tragen. Bestimmte Abschnitte dieser mitochondrialen DNA können sich zu dichten, viersträngigen Knäueln falten, die als G-Quartette bekannt sind. Mithilfe einer hochspezifischen fluoreszierenden Sonde kartierten die Wissenschaftler diese Strukturen in Maus-Knochen. Sie entdeckten, dass diese DNA-Knötchen, genannt mtG4, selektiv im Periost anreichern, wenn Tiere altern — sowohl in normal alten Mäusen als auch in einem genetischen Modell vorzeitigen Alterns. Wichtig war, dass sich dieser Aufbau besonders stark in den periostalen Stammzellen zeigte, die normalerweise die Bruchheilung antreiben.
Vom Energieengpass zur „alten“ Zelle
Um herauszufinden, was mtG4 tatsächlich bewirkt, isolierten die Forschenden periostale Stammzellen und züchteten sie zu winzigen 3D-Organoiden — Mini-Geweben, die die frühe Bruchheilung nachahmen. Durch eine kurze Behandlung mit Kalium, das G-Quartett-Strukturen stabilisiert, verstärkten sie die Bildung von mtG4, ohne die Zellen sonst zu schädigen. Die Folgen waren deutlich: Wichtige mitochondriale Gene gingen in ihrer Aktivität zurück, die Energieproduktion (ATP) fiel, und die Mitochondrien selbst wurden geschwollen und beschädigt, häufig in Recyclingstrukturen aufgenommen in einem Prozess namens Mitophagie. Diese gestressten Zellen zeigten typische Kennzeichen zellulären Alterns — sie stellten die Teilung ein, exprimierten klassische Seneszenzmarker und setzten hohe Mengen entzündungsfördernder Moleküle frei, die umliegendes Gewebe schädigen können.
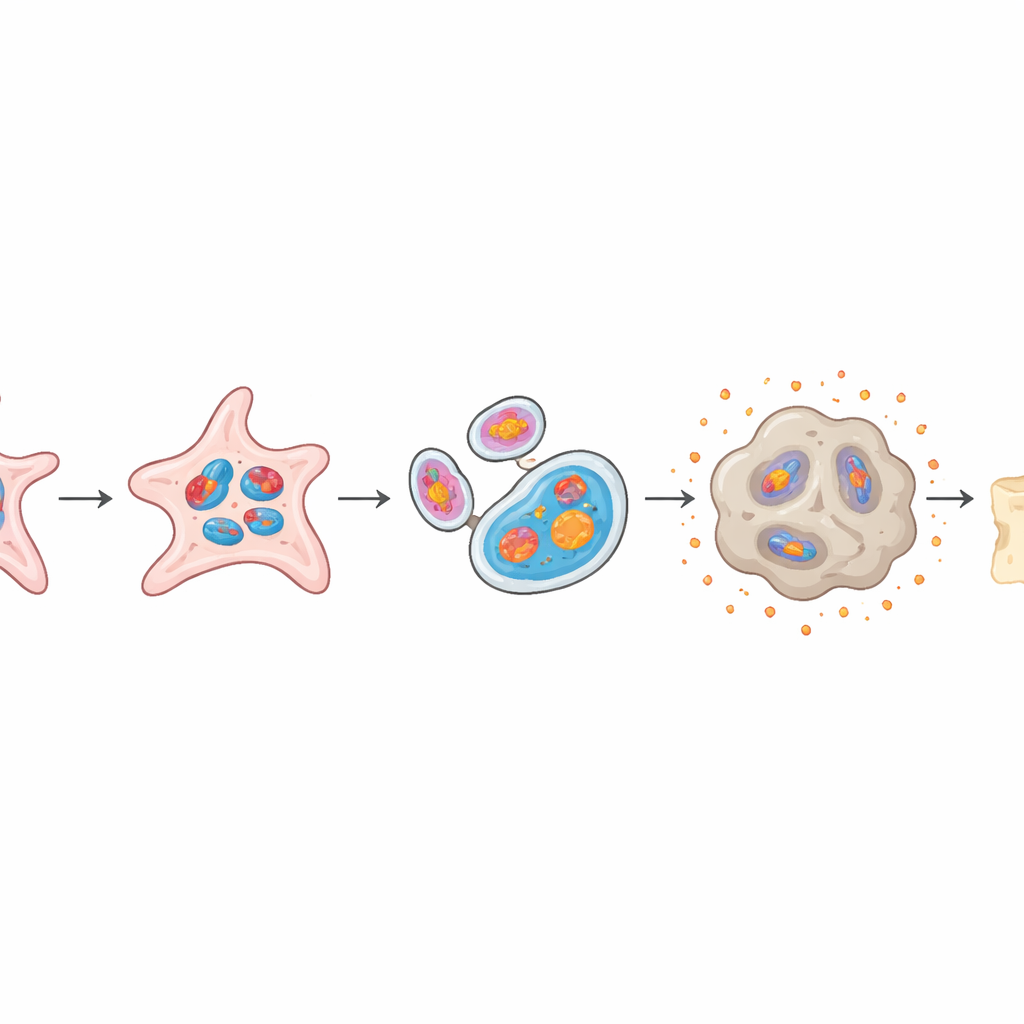
Wenn Reparaturzellen den falschen Weg wählen
Gesunde periostale Stammzellen können sich zu hartem, mineralisiertem Knochen oder zu flexiblem Knorpel differenzieren; dieses Gleichgewicht ist entscheidend für eine ordnungsgemäße Heilung. Im Organoid-Modell verloren Zellen mit mtG4-Überladung einen Großteil ihrer Fähigkeit, Knochen zu bilden: Es zeigte sich weniger Mineralanlagerung und niedrigere Werte knochenbezogener Gene. Gleichzeitig neigten sie stärker zur Knorpelbildung, mit größeren, reiferen Knorpelclustern. Wurden diese mtG4-reichen Organoide in Mäuse transplantiert, bildeten sie deutlich weniger neuen Knochen als normale Organoide und imitierten damit die schlechte Heilung, die bei alten Tieren beobachtet wird.
Verknüpfung von DNA-Strukturen mit fragilen Knochen
Schließlich prüfte das Team, ob dieser Mechanismus tatsächlich altersähnliche Knochenprobleme in lebenden Tieren verursacht. In Mäusen mit einer Mutation, die die mitochondriale DNA destabilisiert und die mtG4-Bildung fördert, heilten Brüche schlecht: Der neue Knochen war dünn, porös und mechanisch schwach, während Knorpel dort verweilte, wo fester Knochen entstehen sollte. Überall dort, wo sich mtG4 in periostalen Stammzellen anhäufte, zeigten die Mitochondrien Versagen, die Zellen wurden seneszent und die Knochenheilung litt.
Was das für gesundes Altern bedeutet
Die Studie zeigt, dass spezielle DNA-Knötchen in der mitochondrialen DNA wie molekulare Handbremsen auf der Knochenheilung wirken können, besonders im Periost. Wenn mtG4-Strukturen mit dem Alter zunehmen, entziehen sie Stammzellen Energie, drücken sie in einen vorzeitigen „alten“ Zustand und verschieben die Heilung zugunsten weichen Knorpels statt starken Knochens. Indem mtG4 als gewebespezifischer Marker und Treiber schädlicher seneszenter Zellen identifiziert wurde, eröffnet diese Arbeit einen neuen Ansatz für künftige Therapien: Wirkstoffe, die diese mitochondrialen DNA-Knötchen verhindern oder auflösen, oder die gezielt mtG4-beladene seneszente Zellen entfernen, könnten eines Tages älteren Patientinnen und Patienten helfen, Knochenbrüche schneller und sicherer zu heilen.
Zitation: Wu, Y., Han, C., Yang, X. et al. Periosteal mitochondria DNA structures drive aging-associated poor skeletal repair. Bone Res 14, 40 (2026). https://doi.org/10.1038/s41413-026-00524-6
Schlüsselwörter: Knochenheilung, Altern, Mitochondrien, Stammzellen, zelluläre Seneszenz