Clear Sky Science · pt
Estruturas do DNA mitocondrial no periósteo impulsionam a má regeneração óssea associada ao envelhecimento
Por que ossos quebrados têm dificuldade para cicatrizar na velhice
À medida que as pessoas envelhecem, uma queda simples pode provocar uma fratura que nunca se cura corretamente. Médicos observam isso diariamente, mas a causa dentro de nossas células permaneceu obscura. Este estudo revela um culpado surpreendente enterrado nas minúsculas usinas de energia das células reparadoras do osso — nós incomuns no DNA que se acumulam gradualmente e sabotam a cicatrização.
Uma camada fina com um grande papel
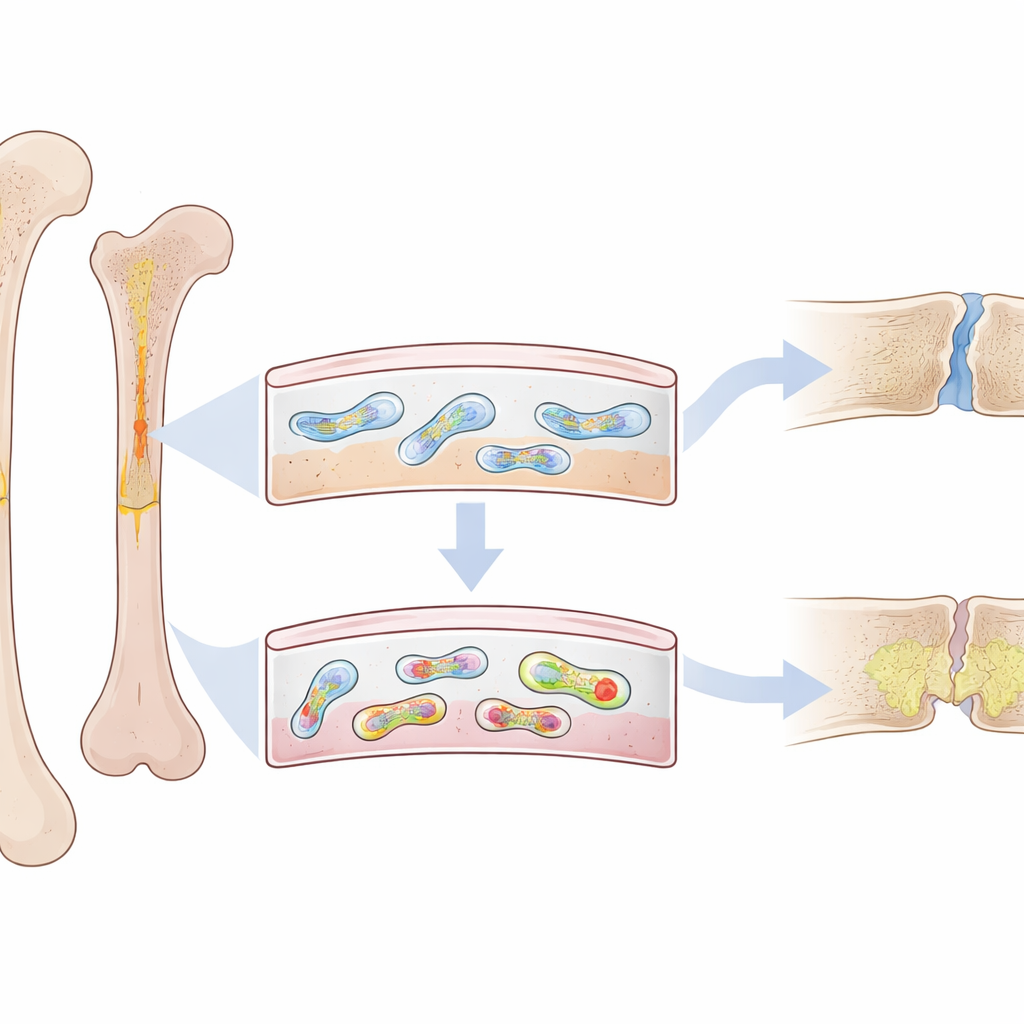
Na superfície de todo osso existe uma camada delgada e fibrosa chamada periósteo. Longe de ser apenas um invólucro, ela abriga um grupo especial de células com características de célula-tronco que correm para reconstruir o osso após uma fratura. Em adultos jovens, essas células do periósteo são altamente ativas e conseguem formar rapidamente osso novo e sólido. Mas em pessoas mais velhas — e em animais com envelhecimento prematuro — as reparações são mais lentas, mais fracas e têm maior probabilidade de deixar lacunas preenchidas por tecido mole e frágil. Os pesquisadores suspeitaram que algo dentro dessas células do periósteo muda com a idade, deslocando-as da reconstrução saudável.
Pequenos nós de DNA nas usinas de energia celular
A equipe concentrou-se nas mitocôndrias, as fábricas de energia dentro das células que carregam seus próprios pequenos anéis de DNA. Certos trechos desse DNA mitocondrial podem se dobrar em nós apertados de quatro fitas conhecidos como G-quadruplexos. Usando uma sonda fluorescente altamente específica, os cientistas mapearam essas estruturas em ossos de camundongos. Eles descobriram que esses nós de DNA, chamados mtG4, se acumulam seletivamente no periósteo à medida que os animais envelhecem — tanto em camundongos idosos normais quanto em um modelo genético de envelhecimento prematuro. Importante, esse acúmulo foi mais forte nas células-tronco periosteais que normalmente impulsionam o reparo de fraturas.
Da crise de energia às células “velhas”
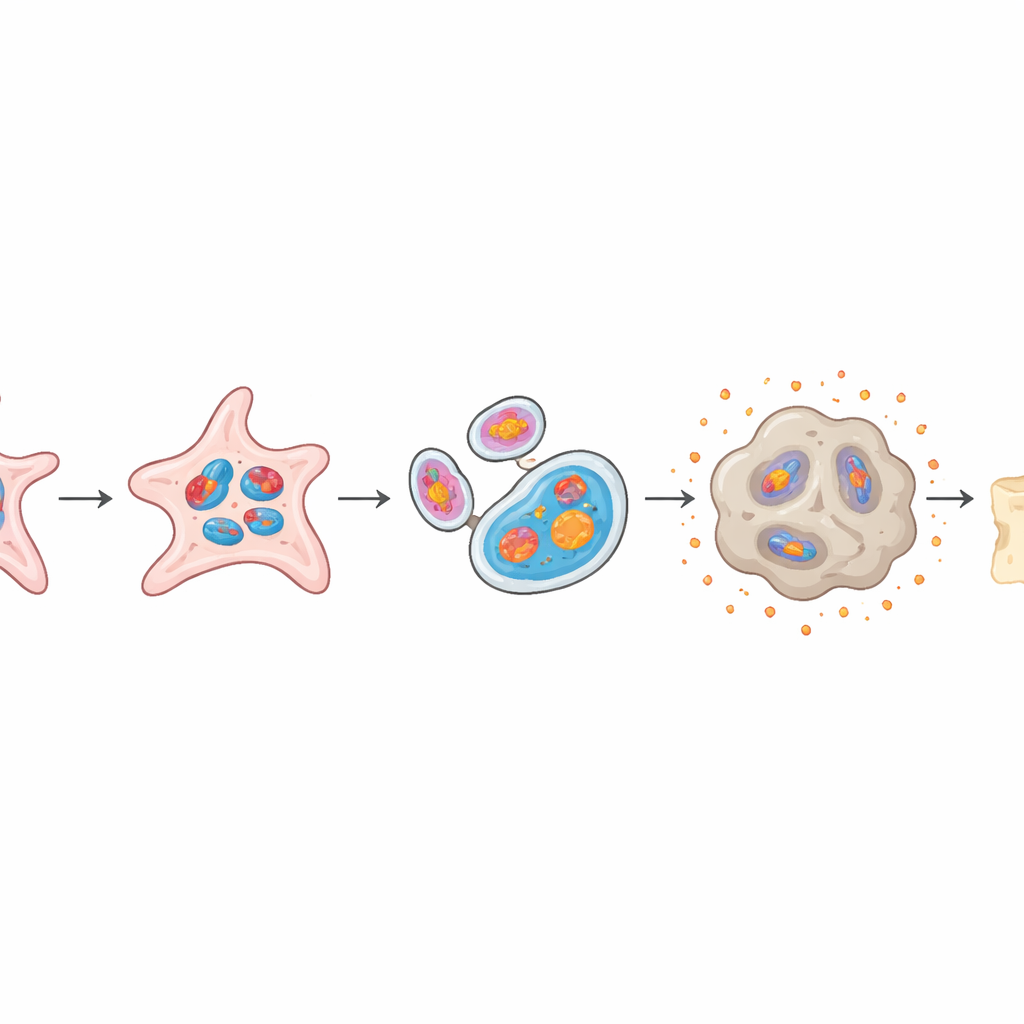
Para entender o efeito dos mtG4, os pesquisadores isolaram células-tronco periosteais e as cultivaram em organoides 3D — mini-tecidos que imitam o reparo inicial de fraturas. Ao expor brevemente as células ao potássio, que estabiliza estruturas G-quadruplex, eles aumentaram a formação de mtG4 sem danificar as células de outra forma. As consequências foram marcantes: genes mitocondriais-chave ficaram menos ativos, a produção de energia (ATP) diminuiu, e as próprias mitocôndrias ficaram inchadas e danificadas, frequentemente sendo engolfadas por estruturas de reciclagem em um processo chamado mitofagia. Essas células estressadas passaram a exibir sinais de envelhecimento celular — pararam de se dividir, expressaram marcadores clássicos de senescência e liberaram altos níveis de moléculas inflamatórias que podem prejudicar o tecido vizinho.
Quando as células reparadoras escolhem o caminho errado
Células-tronco periosteais saudáveis podem optar por se tornar osso duro e mineralizado ou cartilagem flexível, e esse equilíbrio é crucial para a cicatrização adequada. No modelo de organoide, células sobrecarregadas de mtG4 perderam grande parte da capacidade de formar osso, apresentando menor deposição mineral e níveis reduzidos de genes relacionados ao osso. Ao mesmo tempo, tornaram-se mais propensas a formar tecido semelhante à cartilagem, com agrupamentos cartilaginosos maiores e mais maduros. Quando esses organoides ricos em mtG4 foram transplantados em camundongos, geraram muito menos osso novo do que organoides normais, reproduzindo fielmente a má cicatrização observada em animais envelhecidos.
Vinculando estruturas de DNA a ossos frágeis
Finalmente, a equipe testou se esse mecanismo realmente causa problemas ósseos semelhantes aos do envelhecimento em animais vivos. Em camundongos que carregam uma mutação que desestabiliza o DNA mitocondrial e promove a formação de mtG4, as fraturas cicatrizaram mal: o osso novo era fino, poroso e mecanicamente fraco, enquanto cartilagem persistia onde deveria ter se formado osso sólido. Ao longo desses experimentos, um padrão emergiu — onde quer que mtG4 se acumulasse nas células-tronco periosteais, as mitocôndrias falhavam, as células tornavam-se senescentes e o reparo ósseo sofria.
O que isso significa para um envelhecimento saudável
O estudo revela que nós especiais no DNA mitocondrial podem agir como freios moleculares ao reparo ósseo, especialmente no periósteo. À medida que as estruturas mtG4 se acumulam com a idade, elas drenam a energia das células-tronco, empurram-nas para um estado prematuramente “velho” e deslocam a cicatrização em direção à cartilagem mole em vez de osso resistente. Ao identificar os mtG4 como um marcador e motor específico de tecido para células senescentes prejudiciais, este trabalho sugere uma nova via para tratamentos futuros: fármacos que impeçam ou desfaçam esses nós do DNA mitocondrial, ou que removam seletivamente as células senescentes carregadas de mtG4, poderiam um dia ajudar pacientes idosos a curar ossos quebrados mais rápida e seguramente.
Citação: Wu, Y., Han, C., Yang, X. et al. Periosteal mitochondria DNA structures drive aging-associated poor skeletal repair. Bone Res 14, 40 (2026). https://doi.org/10.1038/s41413-026-00524-6
Palavras-chave: reparo ósseo, envelhecimento, mitocôndrias, células-tronco, senescência celular