Clear Sky Science · it
Strutture del DNA mitocondriale periosteo guidano la cattiva riparazione scheletrica legata all’invecchiamento
Perché le ossa rotte faticano a rimarginare con l’età
Con l’avanzare dell’età, una semplice caduta può causare una frattura che non si rimargina correttamente. I medici lo vedono quotidianamente, ma la causa profonda a livello cellulare è stata poco chiara. Questo studio individua un colpevole sorprendente nascosto al cuore delle centrali energetiche delle cellule che riparano l’osso: nodi anomali di DNA che si accumulano silenziosamente nel tempo e compromettono la guarigione.
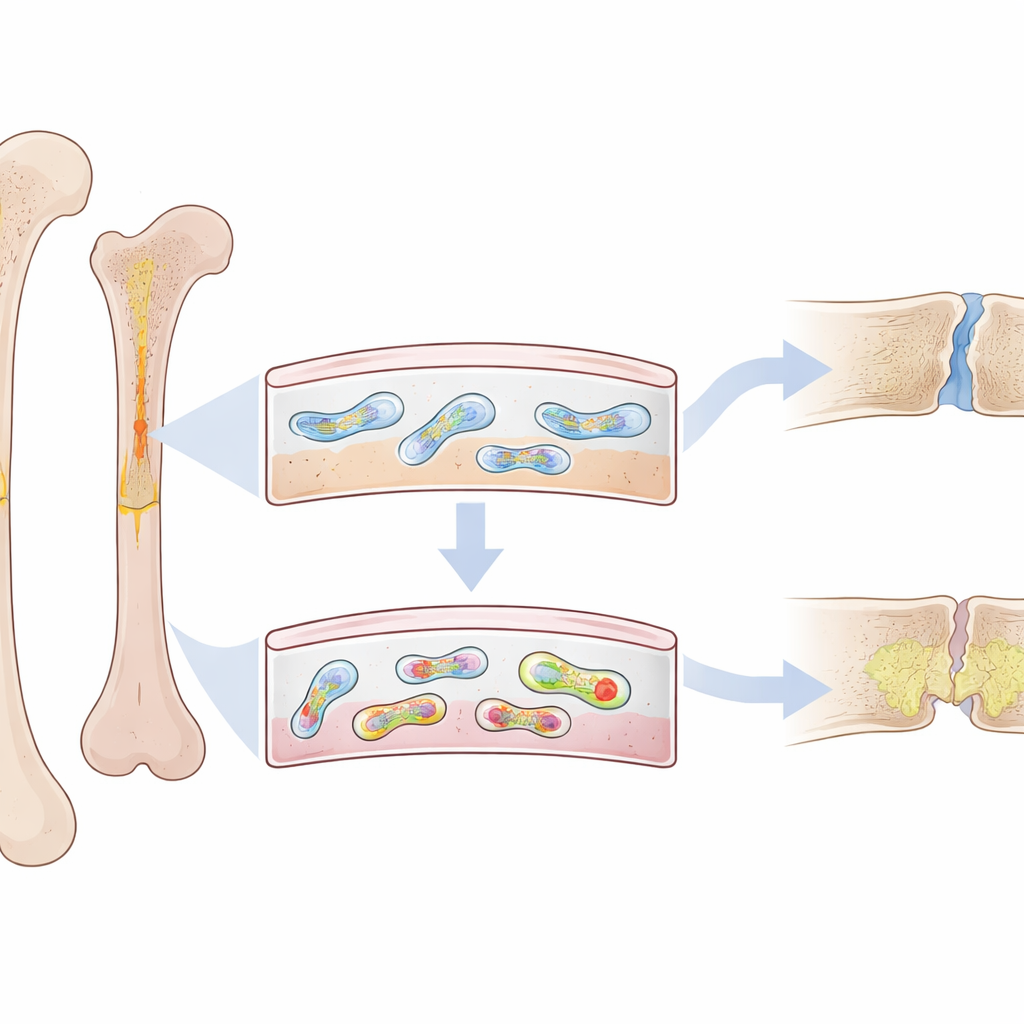
Uno strato sottile con un compito importante
Sulla superficie esterna di ogni osso si trova un sottile rivestimento fibroso chiamato periostio. Lontano dall’essere solo un involucro, contiene un gruppo speciale di cellule simili a staminali che intervengono per ricostruire l’osso dopo una frattura. Nei giovani adulti queste cellule periostali sono molto attive e possono formare rapidamente nuovo osso solido. Ma nelle persone anziane — e negli animali con invecchiamento prematuro — le riparazioni sono più lente, più deboli e più propense a lasciare spazi riempiti da tessuto molle e fragile. I ricercatori hanno ipotizzato che qualcosa all’interno di queste cellule periostali cambi con l’età, facendole deviare dalla ricostruzione sana.
Piccoli nodi di DNA nelle centrali energetiche cellulari
Il gruppo si è concentrato sui mitocondri, le fabbriche energetiche delle cellule che possiedono piccoli anelli di DNA propri. Alcuni tratti di questo DNA mitocondriale possono ripiegarsi in nodi stretti a quattro fili noti come G-quadruplex. Utilizzando una sonda fluorescente altamente specifica, gli scienziati hanno mappato queste strutture nelle ossa dei topi. Hanno scoperto che questi nodi di DNA, chiamati mtG4, si accumulano selettivamente nel periostio con l’età — sia nei topi anziani normali sia in un modello genetico di invecchiamento precoce. È importante che questo accumulo fosse massimo nelle cellule staminali periostali che normalmente guidano la riparazione delle fratture.
Dalla crisi energetica alle cellule “vecchie”
Per capire cosa fanno realmente gli mtG4, i ricercatori hanno isolato le cellule staminali periostali e le hanno coltivate in piccoli organoidi 3D — mini tessuti che imitano la riparazione iniziale della frattura. Esponendo brevemente le cellule al potassio, che stabilizza le strutture a G-quadruplex, hanno aumentato la formazione di mtG4 senza danneggiare le cellule in altro modo. Le conseguenze sono state evidenti: geni mitocondriali chiave risultarono meno attivi, la produzione di energia (ATP) diminuì e i mitocondri stessi divennero gonfi e danneggiati, spesso eliminati da strutture di riciclo in un processo chiamato mitofagia. Queste cellule sotto stress assunsero caratteristiche tipiche dell’invecchiamento cellulare — cessando di dividersi, esprimendo marcatori classici di senescenza e rilasciando alti livelli di molecole infiammatorie che possono danneggiare il tessuto circostante.
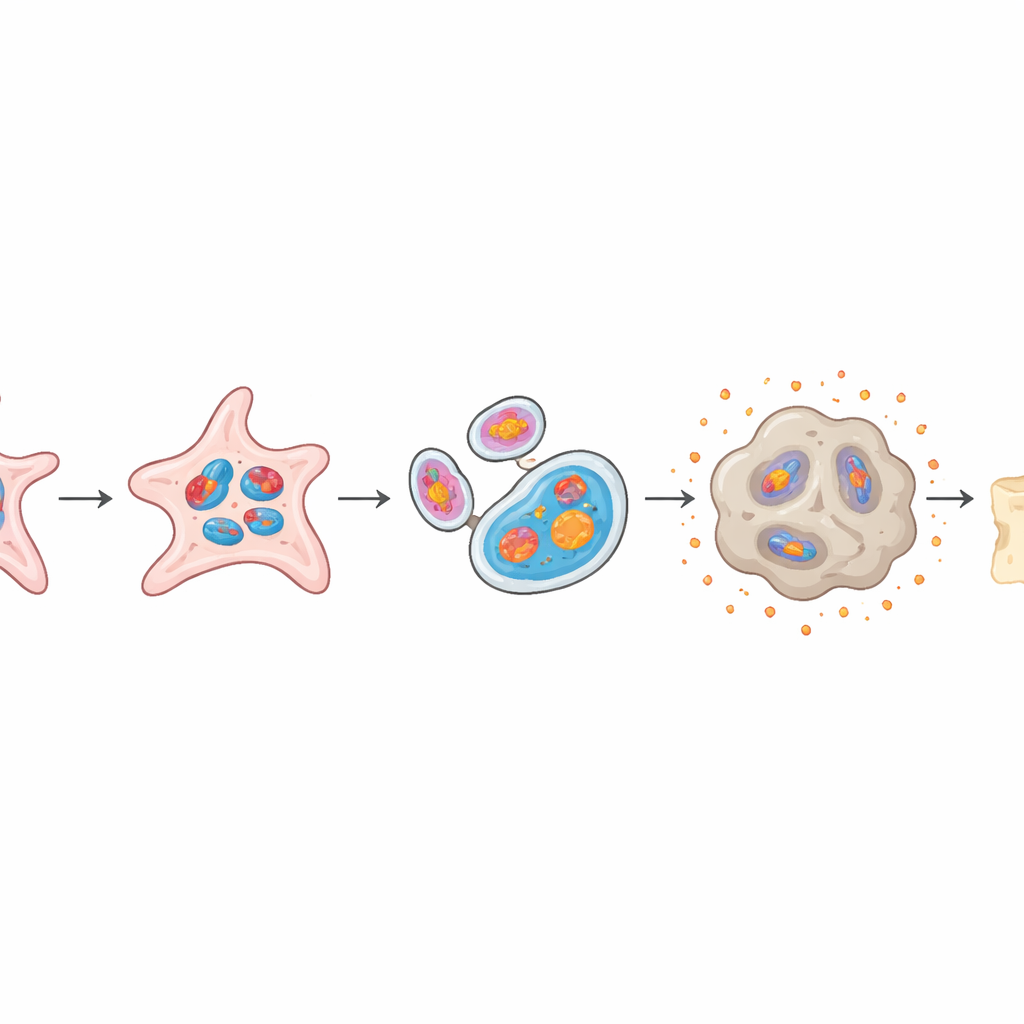
Quando le cellule riparatrici scelgono il percorso sbagliato
Le cellule staminali periostali sane possono differenziarsi in osso duro e mineralizzato o in cartilagine flessibile, e questo equilibrio è cruciale per una guarigione corretta. Nel modello di organoidi, le cellule sovraccariche di mtG4 persero gran parte della loro capacità di formare osso, mostrando minore accumulo di minerali e livelli ridotti di geni legati all’osso. Allo stesso tempo, divennero più inclini a formare tessuto simile alla cartilagine, con ammassi cartilaginei più grandi e maturi. Quando questi organoidi ricchi di mtG4 furono trapiantati nei topi, generarono molto meno osso nuovo rispetto agli organoidi normali, riproducendo fedelmente la scarsa riparazione osservata negli animali invecchiati.
Collegare le strutture del DNA a ossa fragili
Infine, il team ha testato se questo meccanismo guidasse davvero problemi ossei simili all’età negli animali vivi. Nei topi portatori di una mutazione che destabilizza il DNA mitocondriale e favorisce la formazione di mtG4, le fratture guarirono male: il nuovo osso era sottile, poroso e meccanicamente debole, mentre la cartilagine persisteva dove sarebbe dovuto formarsi osso solido. Attraverso questi esperimenti emerse un quadro coerente — dove gli mtG4 si accumulavano nelle cellule staminali periostali, i mitocondri fallivano, le cellule diventavano senescenti e la riparazione ossea ne risentiva.
Cosa significa per un invecchiamento sano
Lo studio rivela che particolari nodi di DNA all’interno del DNA mitocondriale possono agire come freni molecolari sulla riparazione ossea, specialmente nel periostio. Man mano che le strutture mtG4 si accumulano con l’età, drenano l’energia delle cellule staminali, le spingono in uno stato di “invecchiamento” prematuro e indirizzano la guarigione verso cartilagine molle invece che verso osso resistente. Identificando gli mtG4 come un marcatore specifico tissutale e come un agente che promuove cellule senescenti dannose, questo lavoro suggerisce una nuova strada per futuri trattamenti: farmaci che prevengano o sciolgano questi nodi di DNA mitocondriale, o che rimuovano selettivamente le cellule senescenti ricche di mtG4, potrebbero un giorno aiutare i pazienti anziani a guarire le ossa rotte più rapidamente e in modo più sicuro.
Citazione: Wu, Y., Han, C., Yang, X. et al. Periosteal mitochondria DNA structures drive aging-associated poor skeletal repair. Bone Res 14, 40 (2026). https://doi.org/10.1038/s41413-026-00524-6
Parole chiave: riparazione ossea, invecchiamento, mitocondri, cellule staminali, senescenza cellulare