Clear Sky Science · ar
هياكل DNA الميتوكوندريا في الغشاء المحيط بالعظم تدفع إلى ضعف إصلاح الهيكل العظمي المرتبط بالشيخوخة
لماذا تكافح العظام المكسورة للالتئام في سن متقدم
مع تقدم الناس في العمر، قد يؤدي سقوط بسيط إلى كسر عظم لا يلتئم بشكل صحيح. يواجه الأطباء هذا يوميًا، لكن السبب الجذري داخل خلايانا ظل غير واضح. تكشف هذه الدراسة عن سبب مفاجئ مدفون داخل محطات الطاقة الصغيرة لخلايا إصلاح العظم — عقد DNA غير معتادة تتراكم بهدوء مع مرور الزمن وتخرب عملية الشفاء.
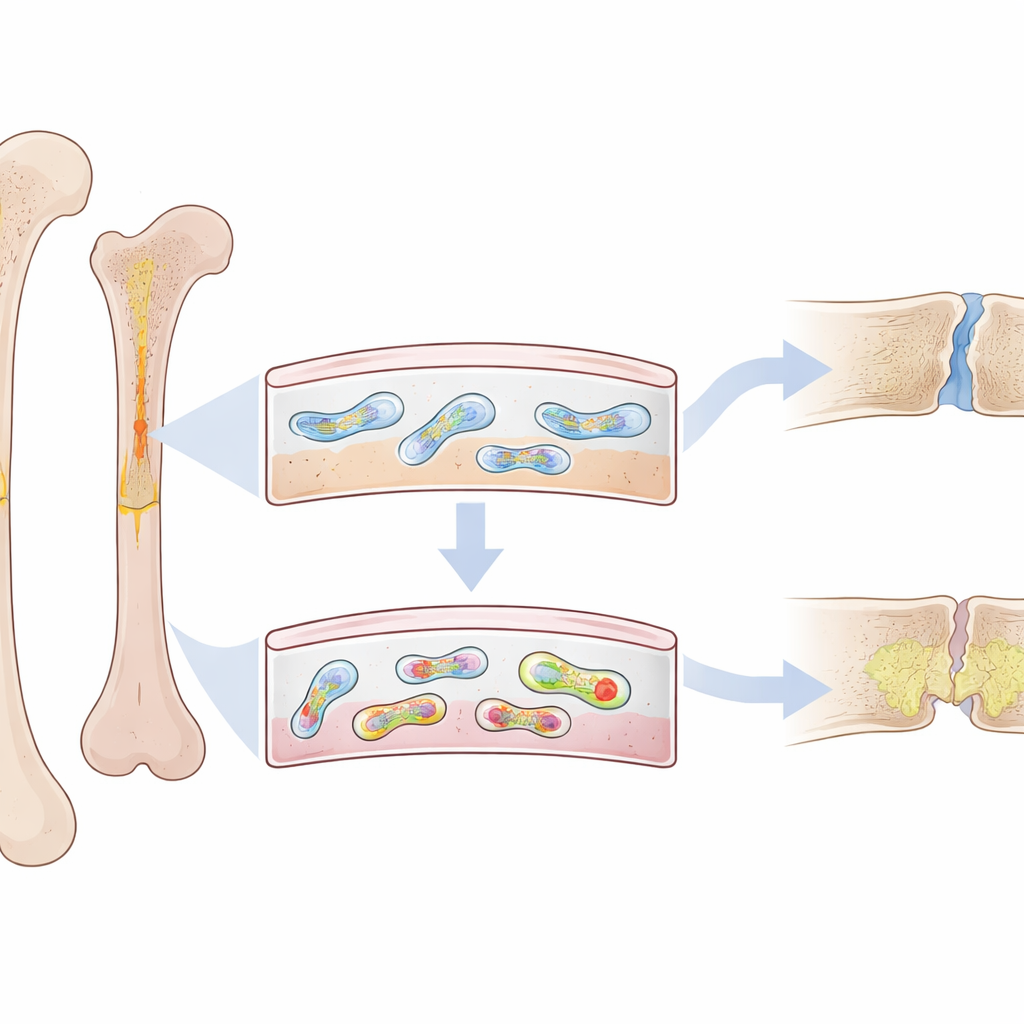
طبقة رقيقة ذات وظيفة كبيرة
على سطح كل عظم تقع طبقة رقيقة ليفية تُسمى الغشاء المحيطي (periosteum). وبعيدة عن كونها مجرد غلاف، فهي تحوي مجموعة مميزة من الخلايا الشبيهة بالجذع التي تتدخل لإعادة بناء العظم بعد الكسر. في البالغين الشباب، تكون هذه الخلايا المحيطية نشطة جدًا ويمكنها تشكيل عظم صلب جديد بسرعة. لكن في المسنين — وفي الحيوانات التي تعاني شيخوخة مبكرة — تكون عمليات الإصلاح أبطأ وأضعف وأكثر عرضة لترك فراغات مملوءة بنسيج طري وهش. اشتبه الباحثون أن شيئًا ما داخل هذه الخلايا المحيطية يتغير مع العمر، مما يبعدها عن إعادة البناء الصحي.
عقد DNA صغيرة في مصانع طاقة الخلايا
ركز الفريق على الميتوكوندريا، مصانع الطاقة داخل الخلايا التي تحمل حلقات صغيرة من DNA خاص بها. يمكن لبعض مقاطع هذا DNA الميتوكوندري أن تطوي نفسها إلى عُقد ضيقة ذات أربعة خيوط تُعرف باسم رباعيات الجوانين (G-quadruplexes). باستخدام مسبار فلوري شديد التخصص، رسم العلماء خارطة لهذه البنى في عظام الفئران. اكتشفوا أن هذه العُقد من الـDNA، المسماة mtG4، تتراكم انتقائيًا في الغشاء المحيطي مع تقدم الحيوانات في العمر — سواء في الفئران المسنة الطبيعية أو في نموذج جيني للشيخوخة المبكرة. والأهم من ذلك، أن هذا التراكم كان أقوى في خلايا الجذع المحيطية التي تقود عادة إصلاح الكسور.
من أزمة طاقة إلى خلايا «عجوز»
لمعرفة ما تفعله mtG4 بالفعل، عزل الباحثون خلايا الجذع المحيطية ونمّوها إلى أعضاء مصغرة ثلاثية الأبعاد — أنسجة صغيرة تحاكي إصلاح الكسور المبكر. عن طريق تعريض الخلايا لفترة وجيزة للبوتاسيوم، الذي يثبت بنى رباعيات الجوانين، عززوا تكوّن mtG4 دون أن يلحقوا أذى آخر بالخلايا. وكانت العواقب لافتة: انخفضت نشاطات جينات ميتوكوندرية رئيسية، وتناقص إنتاج الطاقة (ATP)، وتحولت الميتوكوندريا نفسها إلى هياكل منتفخة ومتضررة، وغالبًا ما ابتلعها نظام إعادة التدوير داخل الخلية في عملية تُسمى البلعمة الميتوكوندرية (mitophagy). اتخذت هذه الخلايا المتوترة سمات الشيخوخة الخلوية — توقفت عن الانقسام، عبرت عن علامات «الشيخوخة» الكلاسيكية، وأفرجت عن مستويات عالية من الجزيئات الالتهابية التي يمكن أن تضر الأنسجة المجاورة.
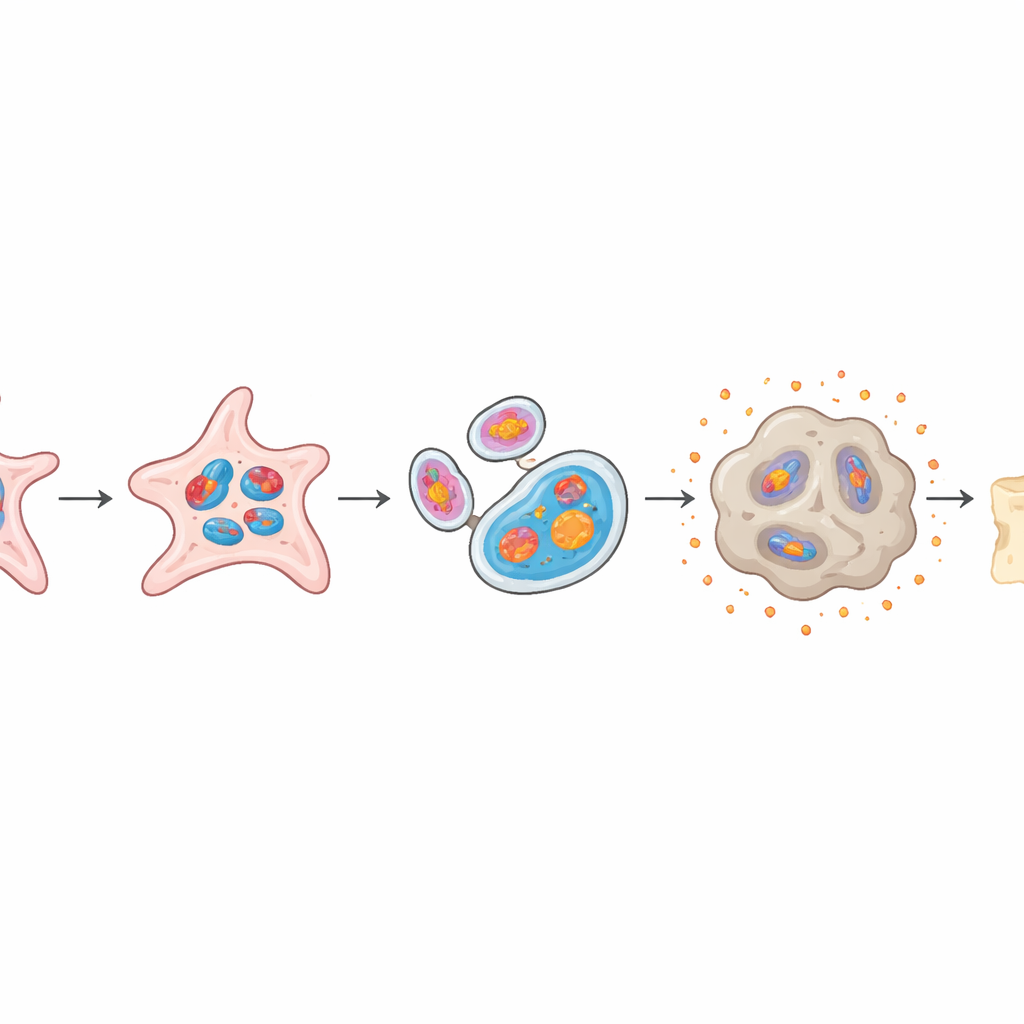
عندما تختار خلايا الإصلاح المسار الخاطئ
يمكن لخلايا الجذع المحيطية الصحية أن تختار أن تتحول إلى عظم صلب ومُمَعدن أو إلى غضروف مرن، وهذا التوازن حاسم للشفاء السليم. في نموذج الأعضاء المصغرة، فقدت الخلايا المشبعة بـmtG4 الكثير من قدرتها على تكوين العظم، حيث أظهرت تراكمًا أقل للمعادن ومستويات أدنى من جينات مرتبطة بالعظم. وفي الوقت نفسه، أصبحت أكثر ميلاً لتكوين نسيج شبيه بالغضروف، مع تجمعات غضروف أكبر وأكثر نضجًا. وعندما زرع الباحثون هذه الأعضاء الغنية بـmtG4 في فئران، أنتجت عظمًا جديدًا أقل بكثير من الأعضاء الطبيعية، محاكاةً بدقة ضعف الإصلاح المرصود في الحيوانات المسنة.
ربط بنى DNA بالعظام الهشة
أخيرًا، اختبر الفريق ما إذا كانت هذه الآلية تقود فعلاً مشاكل العظام المشابهة للشيخوخة في الحيوانات الحية. في الفئران التي تحمل طفرة تزعزع استقرار DNA الميتوكوندري وتعزز تكوّن mtG4، شفيت الكسور بشكل ضعيف: كان العظم الجديد رقيقًا ومسامياً وضعيفًا ميكانيكيًا، بينما ظل الغضروف متواجدًا حيث كان يجب أن يتكون عظم صلب. عبر هذه التجارب، برز نمط واحد — أينما تراكمت mtG4 في خلايا الجذع المحيطية، فشلت الميتوكوندريا، وأصبحت الخلايا مسنة، وتعرض إصلاح العظم للخطر.
ماذا يعني هذا للشيخوخة الصحية
تكشف الدراسة أن عُقد DNA الخاصة داخل الـDNA الميتوكوندري يمكنها أن تعمل كمكابح جزيئية على إصلاح العظام، خصوصًا في الغشاء المحيطي. مع تراكم بنى mtG4 مع العمر، تستنزف طاقة الخلايا الجذعية، وتدفعها إلى حالة «عجوز» مبكرة، وتُميّل عملية الشفاء نحو غضروف طري بدلاً من عظم قوي. وبذلك، يحدد هذا العمل mtG4 كعلامة نسيجية ومحرك للخلايا المسنة الضارة، مما يقترح مسارًا جديدًا للعلاجات المستقبلية: أدوية تمنع أو تفك هذه العُقد في DNA الميتوكوندريا، أو تزيل انتقائيًا الخلايا المسنة المشبعة بـmtG4، قد تساعد يومًا ما المرضى المسنين على شفاء الكسور بسرعة وأمان أكبر.
الاستشهاد: Wu, Y., Han, C., Yang, X. et al. Periosteal mitochondria DNA structures drive aging-associated poor skeletal repair. Bone Res 14, 40 (2026). https://doi.org/10.1038/s41413-026-00524-6
الكلمات المفتاحية: إصلاح العظم, الشيخوخة, الميتوكوندريا, الخلايا الجذعية, شيخوخة خلوية