Clear Sky Science · pl
Struktury DNA mitochondriów w okostnej napędzają związane z wiekiem zaburzenia gojenia kości
Dlaczego złamane kości trudno się goją w podeszłym wieku
W miarę starzenia się ludzi prosty upadek może prowadzić do złamania, które nigdy nie zagoi się prawidłowo. Lekarze obserwują to na co dzień, ale przyczyna leżąca we wnętrzu naszych komórek pozostawała niejasna. To badanie odkrywa zaskakującego winowajcę ukrytego głęboko w małych elektrowniach komórek naprawiających kości — niezwykłe supły DNA, które stopniowo się gromadzą i sabotują proces gojenia.
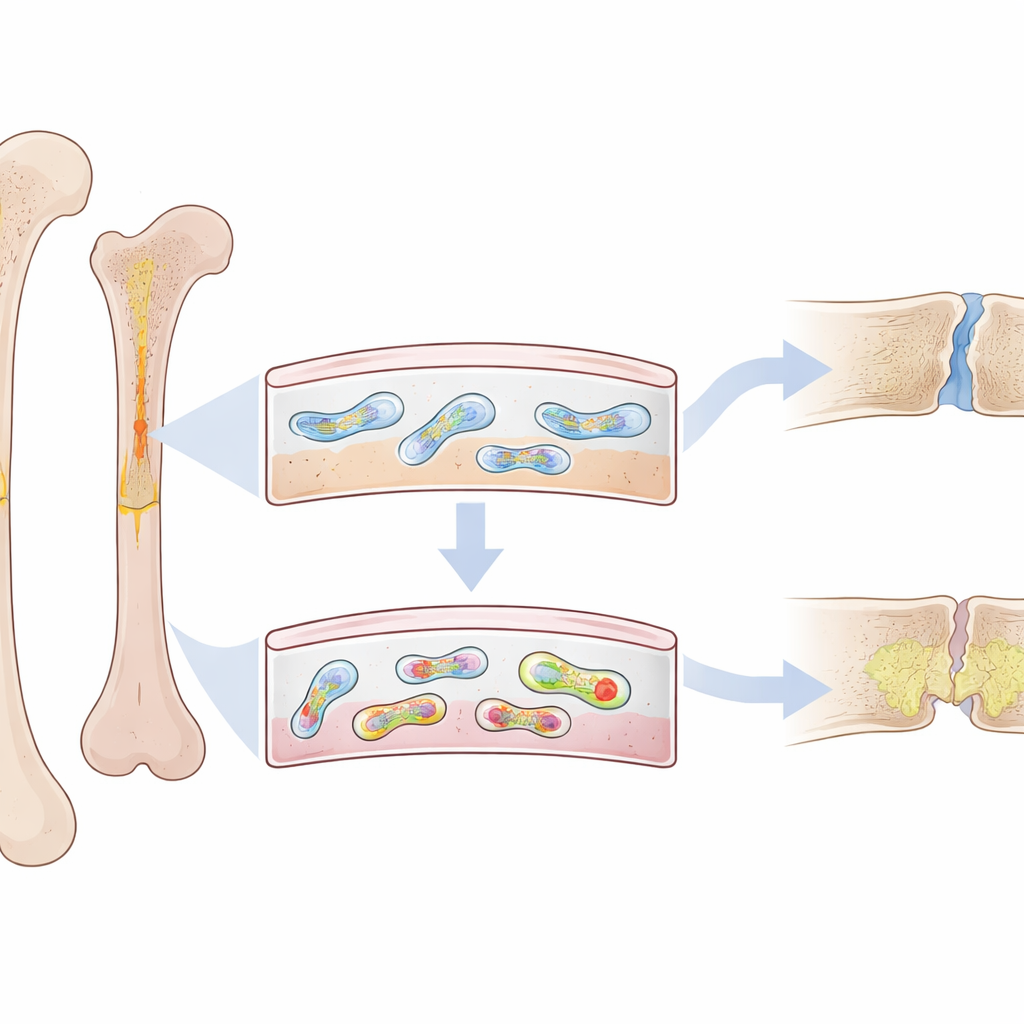
Cienka warstwa o wielkiej roli
Na zewnętrznej powierzchni każdej kości znajduje się cienka, włóknista powłoka zwana okostną. To nie tylko osłona — zawiera specjalną grupę komórek przypominających komórki macierzyste, które szybko wkraczają, by odbudować kość po złamaniu. U młodych dorosłych komórki okostnej są bardzo aktywne i potrafią szybko tworzyć nową, zwartą tkankę kostną. Jednak u starszych osób — i u zwierząt z przedwczesnym starzeniem — naprawy przebiegają wolniej, są słabsze i częściej pozostawiają luki wypełnione miękką, kruchą tkanką. Badacze przypuszczali, że coś wewnątrz tych komórek okostnej zmienia się z wiekiem, odchylając je od zdrowej odbudowy.
Malutkie supły DNA w elektrowniach komórkowych
Zespół skupił się na mitochondriach, fabrykach energetycznych komórek, które mają własne małe pętle DNA. Niektóre odcinki tego DNA mitochondrialnego mogą fałdować się w ciasne, czteroniciowe supły znane jako G-kwadrupleksy. Używając wysoce specyficznej fluorescencyjnej sondy, naukowcy zmapowali te struktury w kościach myszy. Odkryli, że te supły DNA, nazwane mtG4, gromadzą się selektywnie w okostnej wraz z wiekiem — zarówno u normalnie starych myszy, jak i w genetycznym modelu przedwczesnego starzenia. Co ważne, nagromadzenie było najsilniejsze w komórkach macierzystych okostnej, które zwykle napędzają naprawę złamań.
Od kryzysu energetycznego do „starych” komórek
Aby sprawdzić, co mtG4 robi w praktyce, badacze wyizolowali komórki macierzyste okostnej i hodowali je jako maleńkie organoidy 3D — mini tkanki naśladujące wczesną naprawę złamania. Krótka ekspozycja komórek na potas, który stabilizuje struktury G-kwadrupleksowe, zwiększyła formowanie mtG4 bez bezpośredniego uszkadzania komórek. Konsekwencje były uderzające: aktywność kluczowych genów mitochondrialnych zmalała, produkcja energii (ATP) spadła, a mitochondria zrobiły się obrzmiałe i uszkodzone, często usuwane przez struktury recyklingujące w procesie zwanym mitofagią. Stresowane komórki przyjęły cechy starzenia komórkowego — przestały się dzielić, zaczęły wyrażać klasyczne markery „senescencji” i wydzielać wysokie poziomy zapalnych molekuł, które mogą uszkadzać pobliską tkankę.
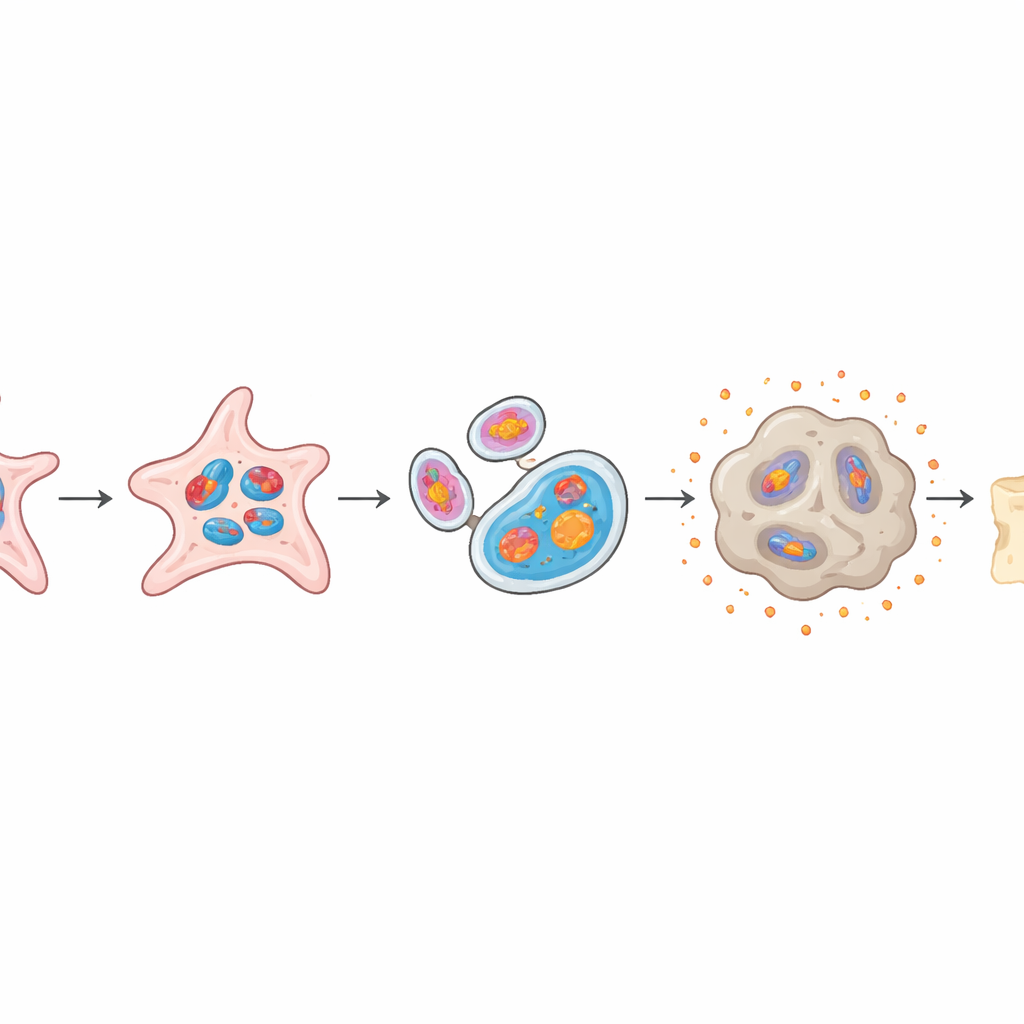
Gdy komórki naprawcze wybierają złą ścieżkę
Zdrowe komórki macierzyste okostnej mogą różnicować się w twardą, zmineralizowaną kość lub w elastyczną chrząstkę, a równowaga między tymi drogowymi jest kluczowa dla poprawnego gojenia. W modelu organoidów komórki przeciążone mtG4 straciły dużą część zdolności do tworzenia kości — wykazywały mniejsze odkładanie minerałów i niższe poziomy genów związanych z kością. Jednocześnie stały się bardziej skłonne do tworzenia tkanki przypominającej chrząstkę, tworząc większe, bardziej dojrzałe skupiska chrzęstne. Gdy te organoidy bogate w mtG4 przeszczepiono do myszy, wytworzyły znacznie mniej nowej tkanki kostnej niż normalne organoidy, wiernie naśladując słabe gojenie obserwowane u starych zwierząt.
Łączenie struktur DNA ze słabymi kośćmi
Wreszcie zespół sprawdził, czy ten mechanizm rzeczywiście powoduje problemy z kośćmi przypominające wiekowe u żywych zwierząt. U myszy noszących mutację destabilizującą DNA mitochondrialne i sprzyjającą formowaniu mtG4, złamania goiły się źle: nowa kość była cienka, porowata i mechanicznie słaba, podczas gdy chrząstka utrzymywała się tam, gdzie powinna powstać zwarta tkanka kostna. W całych eksperymentach wyłonił się jeden wzorzec — tam, gdzie mtG4 gromadziło się w komórkach macierzystych okostnej, mitochondria zawodziły, komórki przechodziły w stan senescencji, a naprawa kości była zaburzona.
Co to oznacza dla zdrowego starzenia
Badanie pokazuje, że specjalne supły DNA wewnątrz DNA mitochondrialnego mogą działać jak molekularne hamulce na proces gojenia kości, szczególnie w okostnej. W miarę narastania struktur mtG4 z wiekiem wyczerpują one energię komórek macierzystych, przedwcześnie wpychają je w „stary” stan i odchylają proces gojenia w stronę miękkiej chrząstki zamiast mocnej kości. Wskazanie mtG4 jako markeru specyficznego dla tkanki i czynnika napędzającego szkodliwe komórki senescentne sugeruje nowy kierunek dla przyszłych terapii: leki zapobiegające tworzeniu się tych supłów DNA mitochondrialnego lub odwracające je, albo selektywne usuwanie komórek senescentnych obciążonych mtG4, mogłyby kiedyś pomóc starszym pacjentom szybciej i bezpieczniej goić złamane kości.
Cytowanie: Wu, Y., Han, C., Yang, X. et al. Periosteal mitochondria DNA structures drive aging-associated poor skeletal repair. Bone Res 14, 40 (2026). https://doi.org/10.1038/s41413-026-00524-6
Słowa kluczowe: naprawa kości, starzenie się, mitochondria, komórki macierzyste, starzenie komórkowe