Clear Sky Science · zh
空间分辨的成骨细胞追踪转录组学揭示TGF-β可与硬化素联合作为治疗骨质疏松的靶点
这项骨骼研究为何重要
骨质疏松会使骨骼变脆、易断,尤以老年人常见。现有许多药物要么减缓骨吸收,要么短期内促进成骨,但它们可出现副作用且疗效可能会减退。本研究探讨了如何重新激活沉默的成骨细胞,并提出了一种新的联合治疗策略,可能更有力且更持久地增强骨强度。
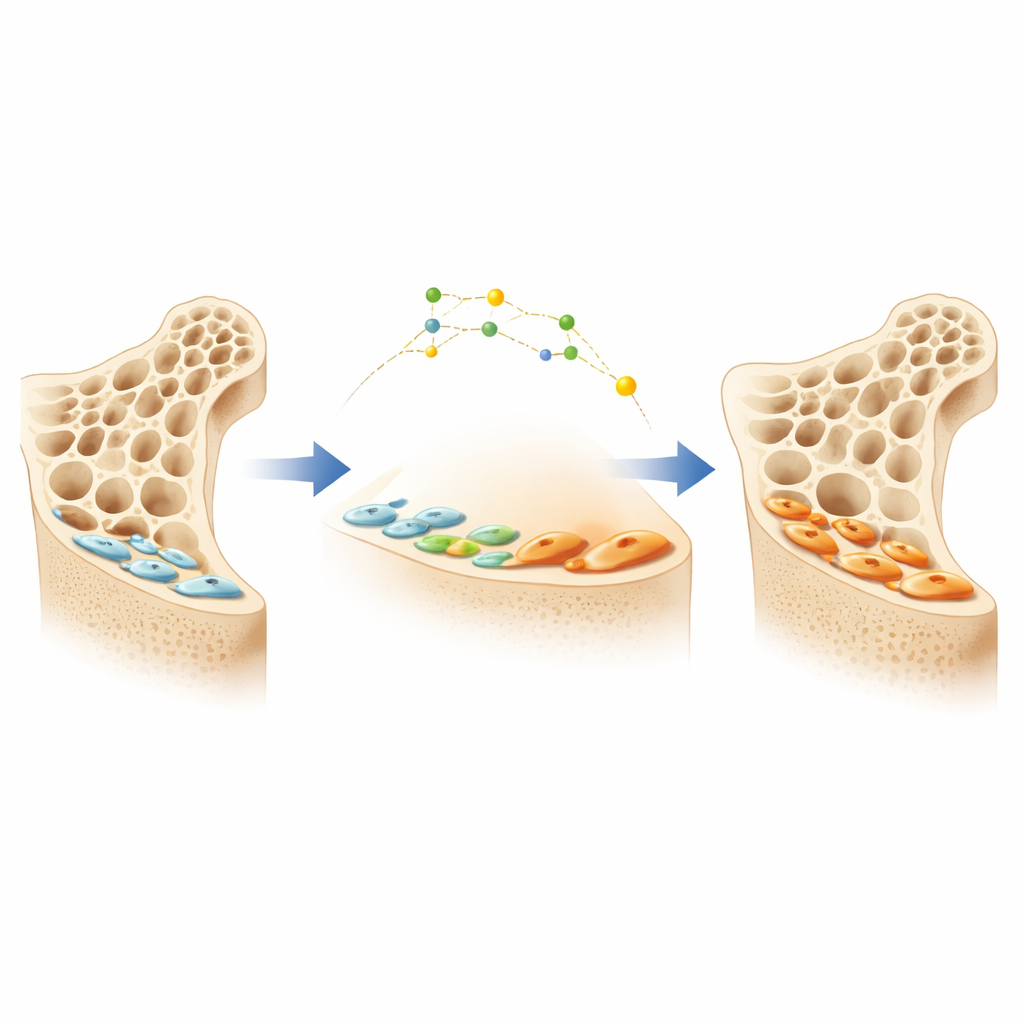
骨表面的沉默“工人”
骨骼由两类主要细胞不断重塑:破骨细胞负责去除老旧骨组织,成骨细胞负责沉积新骨。当成骨细胞完成一轮工作后,许多细胞并不死亡;相反,它们变得扁平,形成薄薄的“骨衬里细胞”,静静地附着在骨表面。这些沉默的细胞构成了大量隐藏的潜在造骨储备。一种较新的抗骨质疏松药通过阻断名为硬化素的蛋白可以唤醒这些衬里细胞,使其重新成为活跃的成骨细胞,从而迅速增加骨量。然而,衬里细胞在静息与活跃状态之间如何切换的细节一直不清楚,这使得设计更聪明、更持久的疗法变得困难。
在原位追踪骨细胞
研究者开发了一种他们称之为“空间分辨的成骨细胞追踪转录组学”的方法,以便在小鼠骨内直接观察这些转变。首先,他们使用了遗传标记系统,使成熟成骨细胞及其后代发出绿色荧光,从而能在这些细胞成为衬里细胞或被抗硬化素抗体重新激活时跟踪它们。随后,他们将此标记与一种基于激光的取样方法结合,该方法可以在保持每个细胞RNA完整性的情况下,轻柔地切取骨片上极小且精确选定的区域。通过对这些区域的RNA测序,研究团队能够看到活跃成骨细胞、静默衬里细胞以及被重新唤醒细胞中哪些基因被开启或关闭,同时保留这些细胞在骨面上的空间位置。
抑制造骨的关键刹车
当团队比较活跃、非活跃和被重新激活的成骨细胞的基因活动模式时,有一条信号通路表现为强有力的“刹车”:由转化生长因子β(TGF-β)控制的通路。静默的衬里细胞显示出更强的TGF-β活性,而不论是自然活跃的成骨细胞还是被硬化素阻断重新激活的细胞,其TGF-β信号都较弱。对成千上万个单细胞进行的单细胞测序证实,最活跃的成骨细胞始终呈现低TGF-β信号。在体外培养的骨类器官中,加入TGF-β会促使成骨细胞变得更扁、更少增殖并更像衬里细胞。这些发现指出,TGF-β是促进静止并抑制造骨活性的一个开关。
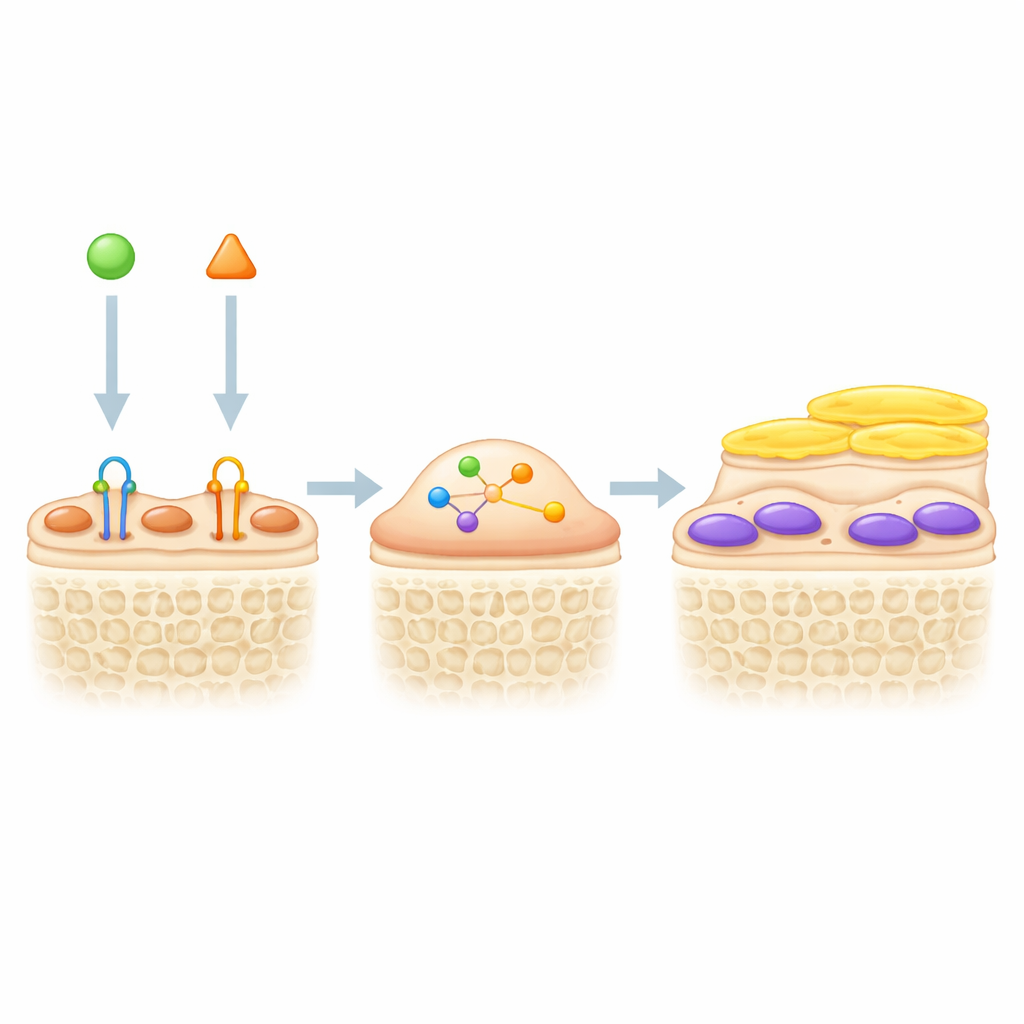
两把“杠杆”联合增强骨强度
鉴于硬化素阻断能唤醒衬里细胞而TGF-β则使其保持静默,作者们测试了同时阻断这两种信号能否促进骨形成。在带有遗传标记的小鼠中,阻断TGF-β的抗体增加了骨面上绿色活跃成骨细胞的厚度和数量,尤其是在与硬化素阻断联合使用时。在一种模拟不活动或航天失重导致骨丧失的后肢卸载模型中,单独使用硬化素阻断可增加骨量,但双重治疗效果更佳。接受两种抗体的小鼠相比只用其中一种的,具有更高的松质骨体积、更厚且更多的骨梁、更多的骨形成以及更少的骨吸收细胞。血液指标和组织染色提示,TGF-β抑制不仅有助于重新激活衬里细胞,还通过与硬化素阻断互补的机制减少骨吸收。
这对患者可能意味着什么
这项工作将特定信号通路TGF-β与骨细胞在休眠与建造之间的决策联系起来,并显示降低该信号可以放大针对硬化素这一强效现有抗骨质疏松药的益处。尽管这些实验证实于小鼠体内,且重要的安全性问题仍需评估——因为TGF-β在多个器官中发挥作用——该研究表明经过仔细调控的双重疗法可能既能唤醒沉睡的造骨细胞,又能抑制骨吸收。从长远看,这一策略或可转化为对抗骨质疏松及其他伴随过度骨丧失疾病的更稳健、持久的治疗方案。
引用: Choi, A., Lee, J.Y., Yoon, H. et al. Spatially resolved osteoblast-traced transcriptomics uncovers TGF-β as a combination target with sclerostin in osteoporosis. Bone Res 14, 37 (2026). https://doi.org/10.1038/s41413-026-00521-9
关键词: 骨质疏松, 成骨细胞, 骨重塑, TGF-β 信号, 硬化素抑制