Clear Sky Science · fr
Transcriptomique spatiale des ostéoblastes traqués révèle le TGF-β comme cible combinée avec la sclérostine dans l’ostéoporose
Pourquoi cette étude osseuse est importante
L’ostéoporose rend les os fragiles et facilement fracturables, en particulier chez les personnes âgées. De nombreux médicaments actuels ralentissent la résorption osseuse ou stimulent brièvement la formation osseuse, mais ils peuvent avoir des effets indésirables et leurs bénéfices peuvent s’estomper. Cette étude explore comment des cellules formatrices d’os silencieuses peuvent être réactivées, et propose une nouvelle stratégie de traitement combiné qui pourrait renforcer les os de façon plus puissante et durable.
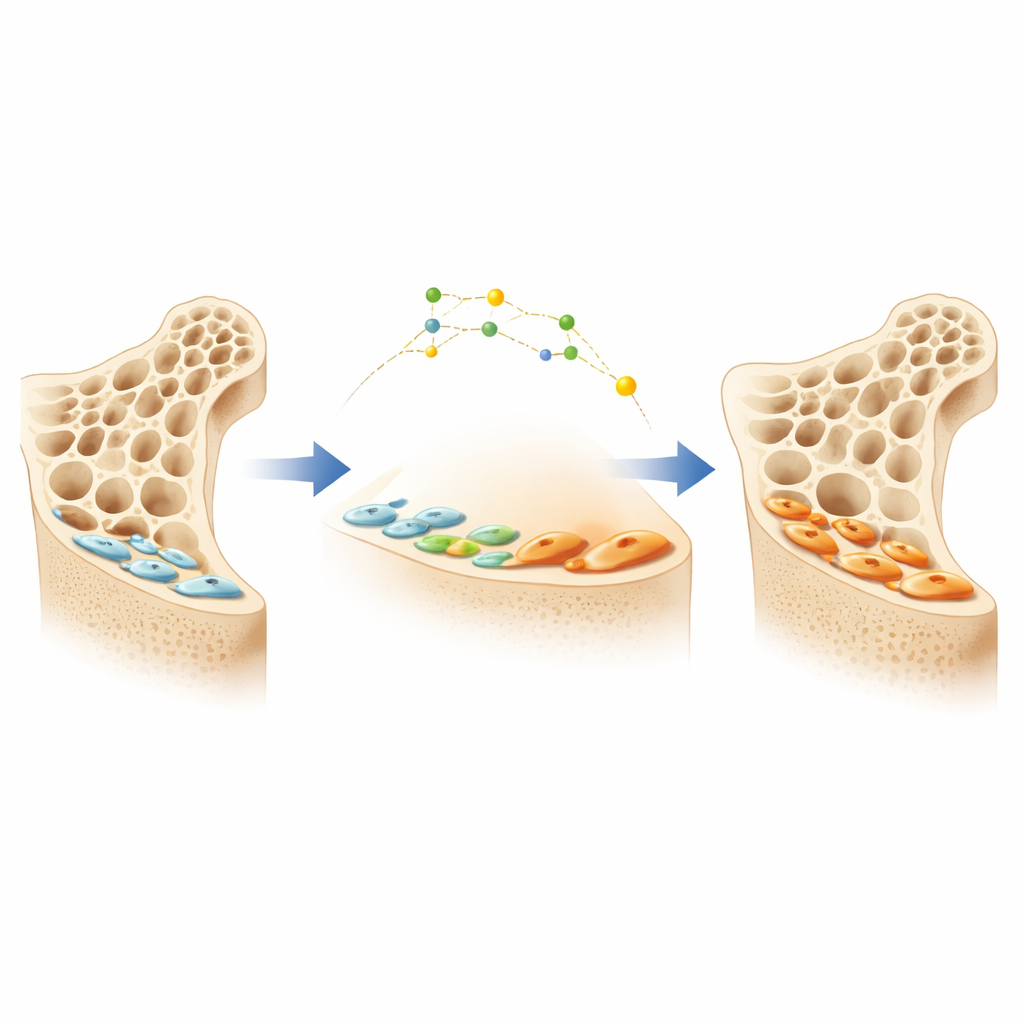
Des travailleurs silencieux à la surface de l’os
Les os sont constamment remodelés par deux types cellulaires principaux : les ostéoclastes, qui éliminent l’os ancien, et les ostéoblastes, qui déposent de l’os nouveau. Quand les ostéoblastes terminent une phase d’activité, beaucoup ne meurent pas ; ils s’aplatissent plutôt et deviennent de fines « cellules de revêtement osseux » qui reposent silencieusement à la surface de l’os. Ces cellules silencieuses constituent une grande réserve cachée de futurs constructeurs d’os. Un médicament plus récent contre l’ostéoporose, qui bloque une protéine appelée sclérostine, peut réveiller ces cellules de revêtement et les reconvertir en ostéoblastes actifs, entraînant des gains rapides de masse osseuse. Cependant, les mécanismes par lesquels les cellules de revêtement basculent entre états silencieux et actifs restent peu compris, ce qui complique la conception de thérapies plus intelligentes et plus durables.
Suivre les cellules osseuses in situ
Les chercheurs ont développé une approche qu’ils appellent « transcriptomique spatiale des ostéoblastes traqués » pour observer directement ces transitions à l’intérieur de l’os de souris. D’abord, ils ont utilisé un système de marquage génétique de sorte que les ostéoblastes matures et leurs descendants brillent en vert, permettant de suivre leur devenir lorsqu’ils deviennent des cellules de revêtement ou sont réactivés par des anticorps bloquant la sclérostine. Puis ils ont combiné cela avec une méthode d’échantillonnage au laser capable de découper délicatement de minuscules régions précisément choisies dans des coupes d’os tout en préservant l’ARN de chaque cellule. En séquençant l’ARN de ces régions, ils ont pu identifier quels gènes étaient activés ou réprimés dans les ostéoblastes actifs, les cellules de revêtement silencieuses et les cellules réactivées, tout en conservant la localisation de ces cellules à la surface osseuse.
Un frein majeur à la formation osseuse
En comparant les profils d’activité génique des ostéoblastes actifs, inactifs et réactivés, un système de signalisation s’est distingué comme un frein puissant : la voie contrôlée par le facteur de transformation bêta (TGF-β). Les cellules de revêtement silencieuses présentaient une activité TGF-β plus élevée, tandis que les ostéoblastes actifs — qu’ils soient naturellement actifs ou réactivés par le blocage de la sclérostine — affichaient des signaux TGF-β plus faibles. Le séquençage unicellulaire, qui analyse des milliers de cellules osseuses individuelles, a confirmé que les ostéoblastes les plus actifs présentaient systématiquement une signalisation TGF-β basse. Dans des organoïdes osseux en culture, l’ajout de TGF-β poussait les ostéoblastes à s’aplatir, à proliférer moins et à ressembler davantage à des cellules de revêtement. Ces résultats désignent le TGF-β comme un commutateur favorisant la quiescence et limitant l’activité de construction osseuse.
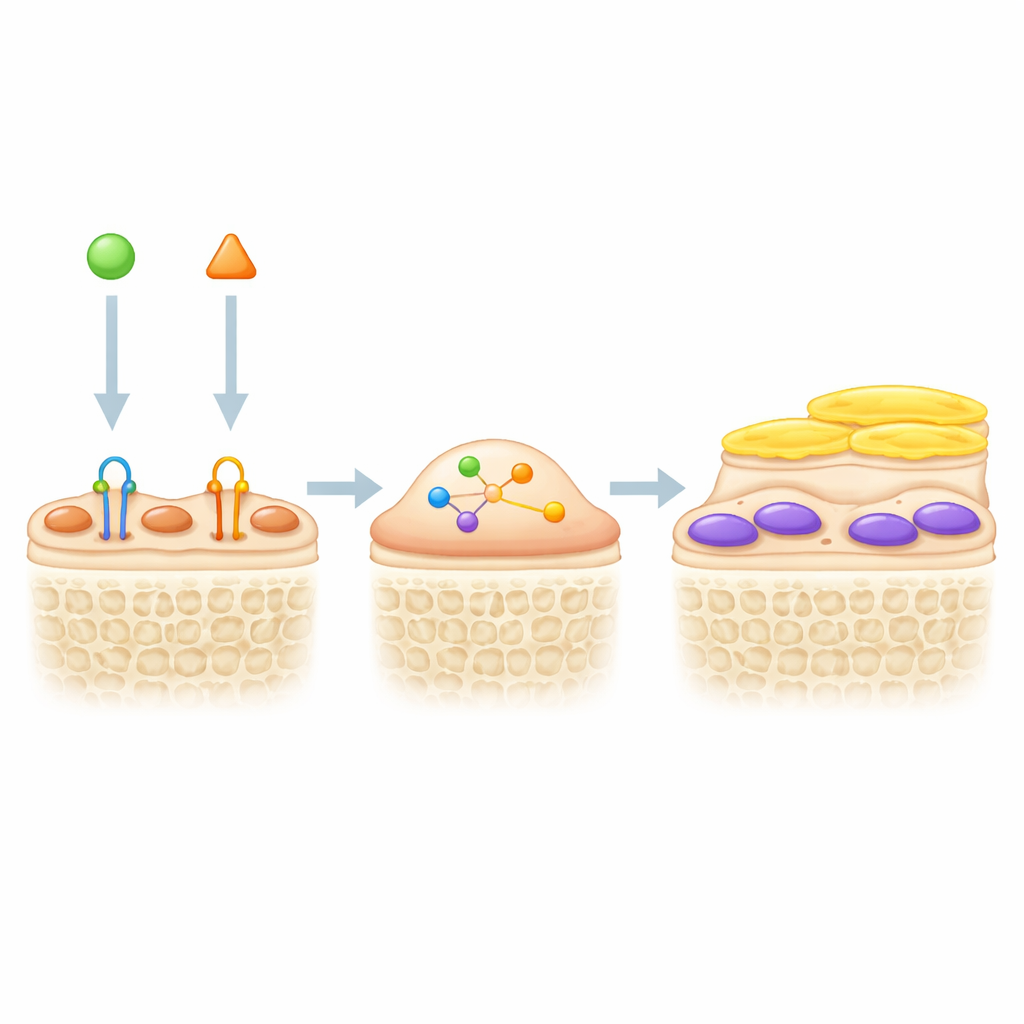
Combiner deux leviers pour des os plus solides
Comme le blocage de la sclérostine réveille les cellules de revêtement et que le TGF-β les maintient silencieuses, les auteurs ont testé si bloquer les deux signaux simultanément stimulerait la formation osseuse. Chez des souris marquées génétiquement, un anticorps bloquant le TGF-β a augmenté l’épaisseur et le nombre d’ostéoblastes verts actifs à la surface osseuse, en particulier en combinaison avec le traitement anti-sclérostine. Dans un modèle de décharge du membre postérieur, qui imite la perte osseuse due à l’inactivité ou au vol spatial, le blocage de la sclérostine seul augmentait la masse osseuse, mais le traitement dual était encore plus efficace. Les souris recevant les deux anticorps présentaient un volume osseux trabéculaire plus élevé, des travées osseuses plus épaisses et plus nombreuses, davantage de formation osseuse et moins de cellules résorbantes que les souris traitées par l’un ou l’autre médicament seul. Les marqueurs sanguins et les colorations tissulaires suggéraient que l’inhibition du TGF-β aidait non seulement à réactiver les cellules de revêtement mais réduisait aussi la résorption osseuse, par des mécanismes complémentaires au blocage de la sclérostine.
Ce que cela pourrait signifier pour les patients
Ce travail relie une voie de signalisation spécifique, le TGF-β, à la décision des cellules osseuses entre repos et construction, et montre que diminuer ce signal peut amplifier les bénéfices d’un médicament puissant existant contre l’ostéoporose ciblant la sclérostine. Bien que ces expériences aient été menées chez la souris et que des questions importantes de sécurité restent à résoudre — car le TGF-β intervient dans de nombreux organes — l’étude suggère que des thérapies duales finement ajustées pourraient à la fois réveiller les bâtisseurs d’os endormis et tempérer la dégradation osseuse. À long terme, cette stratégie pourrait se traduire par des traitements plus robustes et durables pour les personnes souffrant d’ostéoporose et d’autres pathologies caractérisées par une perte osseuse excessive.
Citation: Choi, A., Lee, J.Y., Yoon, H. et al. Spatially resolved osteoblast-traced transcriptomics uncovers TGF-β as a combination target with sclerostin in osteoporosis. Bone Res 14, 37 (2026). https://doi.org/10.1038/s41413-026-00521-9
Mots-clés: ostéoporose, ostéoblastes, remodelage osseux, signalisation TGF-bêta, inhibition de la sclérostine