Clear Sky Science · pl
Odmienna przestrzennie transkryptomika śledząca osteoblasty ujawnia TGF-β jako cel kombinacyjny ze sklerostyną w osteoporozie
Dlaczego to badanie kości ma znaczenie
Osteoporoza powoduje, że kości stają się kruche i łatwe do złamania, zwłaszcza u osób starszych. Wiele dostępnych leków albo spowalnia rozkład kości, albo krótkotrwale zwiększa ich odbudowę, ale mogą one wywoływać skutki uboczne, a ich korzyści mogą słabnąć z czasem. To badanie bada, jak uśpione komórki budujące kość można ponownie uaktywnić, i proponuje nową strategię leczenia kombinacyjnego, która mogłaby skuteczniej i trwalej wzmacniać struktury kostne.
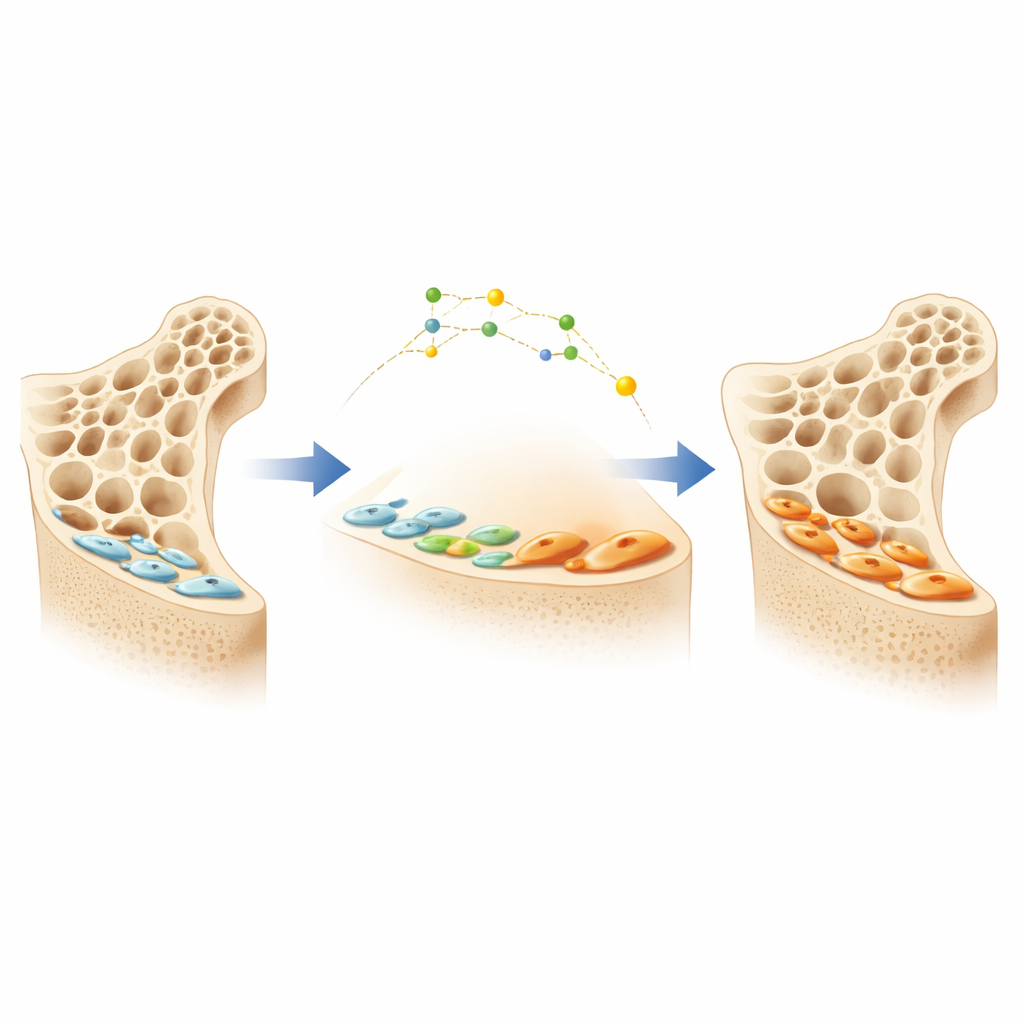
Uśpieni pracownicy na powierzchni kości
Kości są nieustannie przebudowywane przez dwa główne typy komórek: osteoklasty, które usuwają starą tkankę kostną, oraz osteoblasty, które odkładają nową kość. Gdy osteoblasty kończą okres zwiększonej aktywności, wiele z nich nie ginie; zamiast tego spłaszczają się i przekształcają w cienkie „komórki wyściełające” (lining cells), które siedzą spokojnie na powierzchni kości. Te uśpione komórki tworzą dużą ukrytą rezerwę potencjalnych budowniczych kości. Nowszy lek przeciw osteoporozie blokujący białko zwane sklerostyną potrafi obudzić te komórki wyściełające i przywrócić je do aktywnych osteoblastów, prowadząc do szybkiego przyrostu masy kostnej. Jednak mechanizmy przełączania się komórek wyściełających między stanami uśpienia a aktywności były dotąd niejasne, co utrudnia projektowanie bardziej inteligentnych i długotrwałych terapii.
Śledzenie komórek kostnych na miejscu
Naukowcy opracowali podejście, które nazwali „przestrzennie rozdzieloną transkryptomiką śledzącą osteoblasty”, aby obserwować te przemiany bezpośrednio w kościach myszy. Najpierw użyli systemu znakowania genetycznego, dzięki któremu dojrzałe osteoblasty i ich potomstwo świeciły na zielono, co pozwoliło zespołowi śledzić je podczas przechodzenia w komórki wyściełające lub ponownej aktywacji przez przeciwciała blokujące sklerostynę. Następnie połączyli to z metodą laserowego pobierania próbek, która umożliwia delikatne wycięcie maleńkich, precyzyjnie wybranych obszarów z preparatów kostnych, zachowując jednocześnie integralność RNA każdej komórki. Sekwencjonując RNA z tych regionów, mogli zobaczyć, które geny są włączone lub wyłączone w aktywnych osteoblastach, cichych komórkach wyściełających oraz ponownie uaktywnionych komórkach, przy jednoczesnym zachowaniu informacji o ich położeniu na powierzchni kości.
Kluczowy hamulec dla tworzenia kości
Porównując wzorce aktywności genów w osteoblastach aktywnych, nieaktywnych i ponownie aktywowanych, zespół wyróżnił jeden system sygnalizacyjny jako silny hamulec: szlak kontrolowany przez transformujący czynnik wzrostu beta (TGF-β). Ciche komórki wyściełające wykazywały silniejszą aktywność TGF-β, podczas gdy aktywne osteoblasty — zarówno naturalnie aktywne, jak i przywrócone do działania przez blokadę sklerostyny — miały słabsze sygnały TGF-β. Sekwencjonowanie pojedynczych komórek, analizujące tysiące pojedynczych komórek kostnych, potwierdziło, że najbardziej aktywne osteoblasty konsekwentnie wykazują niską aktywność TGF-β. W hodowanych w laboratorium organoidach kostnych dodanie TGF-β skłaniało osteoblasty do stawania się bardziej spłaszczonymi, mniej proliferującymi i podobnymi do komórek wyściełających. Wyniki te wskazują na TGF-β jako przełącznik sprzyjający uśpieniu i ograniczający aktywność budowania kości.
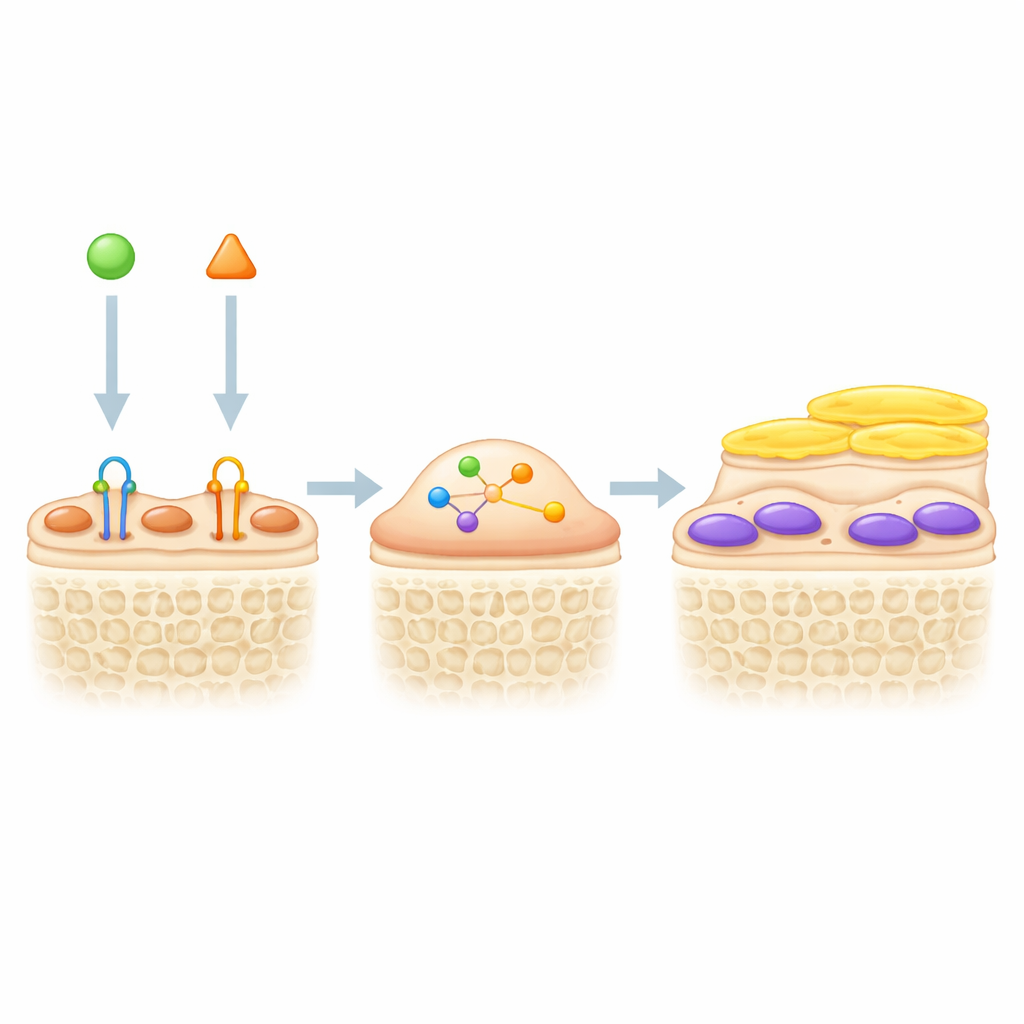
Połączenie dwóch dźwigni dla mocniejszych kości
Ponieważ blokada sklerostyny budzi komórki wyściełające, a TGF-β utrzymuje je w uśpieniu, autorzy sprawdzili, czy jednoczesne blokowanie obu sygnałów zwiększy tworzenie kości. U genetycznie znakowanych myszy przeciwciało blokujące TGF-β zwiększyło grubość i liczbę aktywnych zielonych osteoblastów na powierzchniach kości, szczególnie w połączeniu z leczeniem blokującym sklerostynę. W modelu odciążenia kończyny tylnej, który naśladuje utratę masy kostnej wynikającą z braku aktywności lub lotu kosmicznego, sama blokada sklerostyny zwiększała masę kostną, ale leczenie kombinowane dało jeszcze lepsze efekty. Myszy otrzymujące oba przeciwciała miały większą objętość kości beleczkowej, grubsze i liczniejsze beleczki kostne, więcej tworzenia kości i mniej komórek resorbujących kość niż myszy leczone którymkolwiek z leków osobno. Markery we krwi i barwienia tkanek sugerowały, że hamowanie TGF-β nie tylko pomaga w reaktywacji komórek wyściełających, lecz także zmniejsza resorpcję kości, działając mechanizmami uzupełniającymi blokadę sklerostyny.
Co to może znaczyć dla pacjentów
Praca ta łączy konkretny szlak sygnalizacyjny, TGF-β, z decyzją komórek kostnych między odpoczynkiem a odbudową i pokazuje, że osłabienie tego sygnału może wzmocnić korzyści potężnego, istniejącego leku przeciw osteoporozie celującego w sklerostynę. Choć eksperymenty przeprowadzono na myszach i wciąż pozostają ważne pytania dotyczące bezpieczeństwa — ponieważ TGF-β działa w wielu narządach — badanie sugeruje, że starannie dostrojone terapie podwójne mogłyby zarówno pobudzić śpiących budowniczych kości, jak i złagodzić rozkład kości. W dłuższej perspektywie strategia ta mogłaby przełożyć się na bardziej solidne i trwalsze leczenia dla osób żyjących z osteoporozą i innymi schorzeniami charakteryzującymi się nadmierną utratą kości.
Cytowanie: Choi, A., Lee, J.Y., Yoon, H. et al. Spatially resolved osteoblast-traced transcriptomics uncovers TGF-β as a combination target with sclerostin in osteoporosis. Bone Res 14, 37 (2026). https://doi.org/10.1038/s41413-026-00521-9
Słowa kluczowe: osteoporoza, osteoblasty, remodelowanie kości, szlak sygnalizacyjny TGF-beta, hamowanie sklerostyny