Clear Sky Science · pt
Transcriptômica espacialmente resolvida rastreada por osteoblastos revela TGF-β como alvo combinado com esclerostina na osteoporose
Por que este estudo ósseo é importante
A osteoporose torna os ossos frágeis e suscetíveis a fraturas, especialmente em adultos mais velhos. Muitos medicamentos atuais ou retardam a degradação óssea ou estimulam brevemente a formação óssea, mas podem causar efeitos colaterais e seus benefícios podem diminuir com o tempo. Este estudo investiga como células formadoras de osso quiescentes podem ser reativadas e sugere uma nova estratégia de tratamento combinado que pode ajudar a fortalecer os ossos de forma mais potente e duradoura.
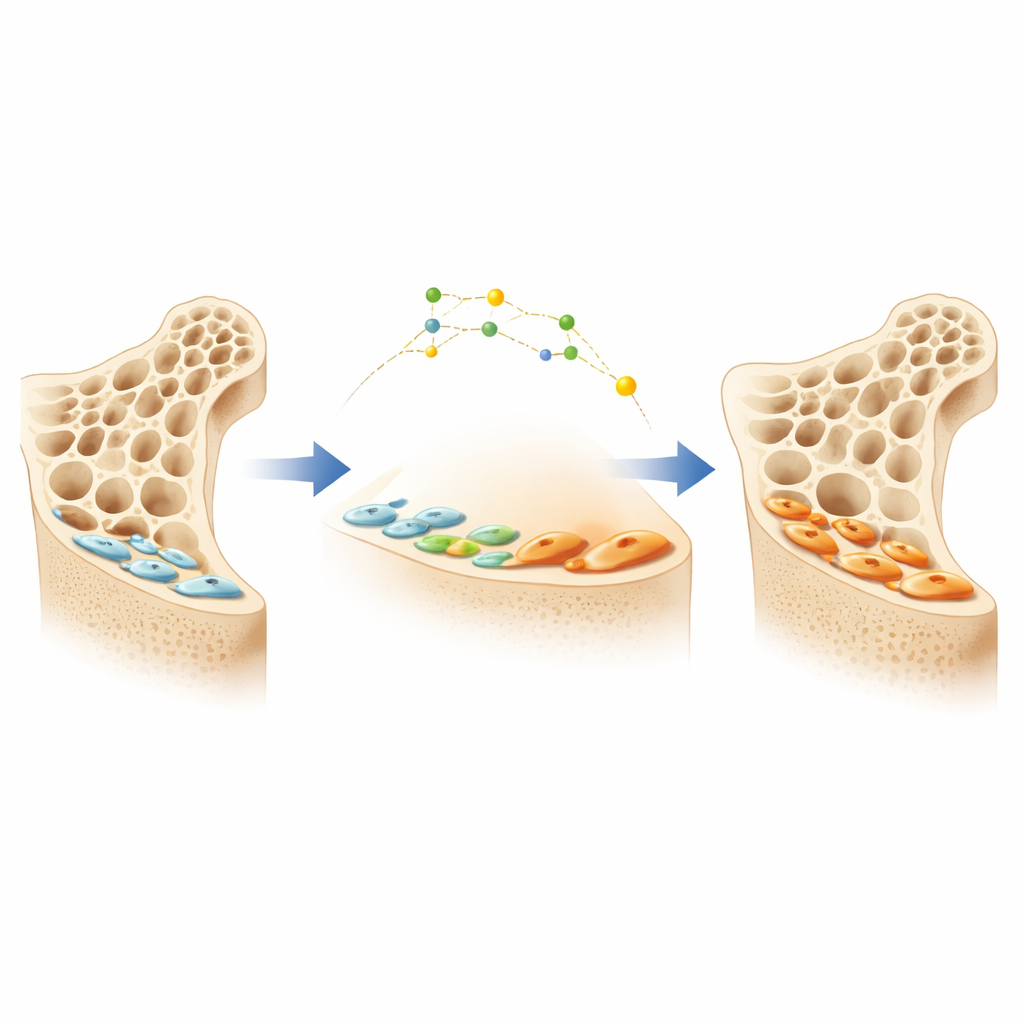
Trabalhadores silenciosos na superfície óssea
Os ossos são continuamente remodelados por dois tipos principais de células: osteoclastos, que removem o osso antigo, e osteoblastos, que depositam novo osso. Quando os osteoblastos terminam um período de atividade, muitos não morrem; em vez disso, achatam-se e se tornam finas “células de revestimento” que ficam silenciosas na superfície óssea. Essas células silenciosas formam uma grande reserva oculta de potenciais formadoras de osso. Um medicamento mais novo para osteoporose que bloqueia uma proteína chamada esclerostina pode despertar essas células de revestimento e reconvertê-las em osteoblastos ativos, levando a ganhos rápidos de massa óssea. No entanto, os detalhes de como as células de revestimento alternam entre estados quiescentes e ativos têm sido pouco claros, dificultando o desenho de terapias mais inteligentes e duradouras.
Rastreando células ósseas no local
Os pesquisadores desenvolveram uma abordagem que chamam de “transcriptômica espacialmente resolvida rastreada por osteoblastos” para observar essas transições diretamente dentro do osso de camundongos. Primeiro, usaram um sistema de marcação genética para que osteoblastos maduros e seus descendentes brilhassem em verde, permitindo à equipe acompanhá-los quando se tornavam células de revestimento ou eram reativados por anticorpos que bloqueiam a esclerostina. Em seguida, combinaram isso com um método de amostragem a laser capaz de recortar delicadamente regiões minúsculas e precisamente escolhidas de lâminas ósseas mantendo o RNA de cada célula intacto. Ao sequenciar o RNA dessas regiões, puderam ver quais genes estavam ligados ou desligados em osteoblastos ativos, células de revestimento quiescentes e células reativadas, preservando também a localização dessas células na superfície óssea.
Um freio chave na formação óssea
Ao comparar os padrões de atividade gênica de osteoblastos ativos, inativos e reativados, um sistema de sinalização destacou-se como um freio poderoso: a via controlada pelo fator de crescimento transformador beta (TGF-β). Células de revestimento quiescentes apresentaram atividade de TGF-β mais forte, enquanto osteoblastos ativos — sejam naturalmente ativos ou reativados pela bloqueio da esclerostina — mostraram sinais de TGF-β mais fracos. Sequenciamento de célula única, que analisa milhares de células ósseas individuais, confirmou que os osteoblastos mais ativos consistentemente exibiam baixa sinalização de TGF-β. Em organoides ósseos cultivados em laboratório, a adição de TGF-β levou os osteoblastos a tornarem-se mais finos, menos proliferativos e mais semelhantes a células de revestimento. Esses achados apontam para o TGF-β como um interruptor que promove a quiescência e restringe a atividade formadora de osso.
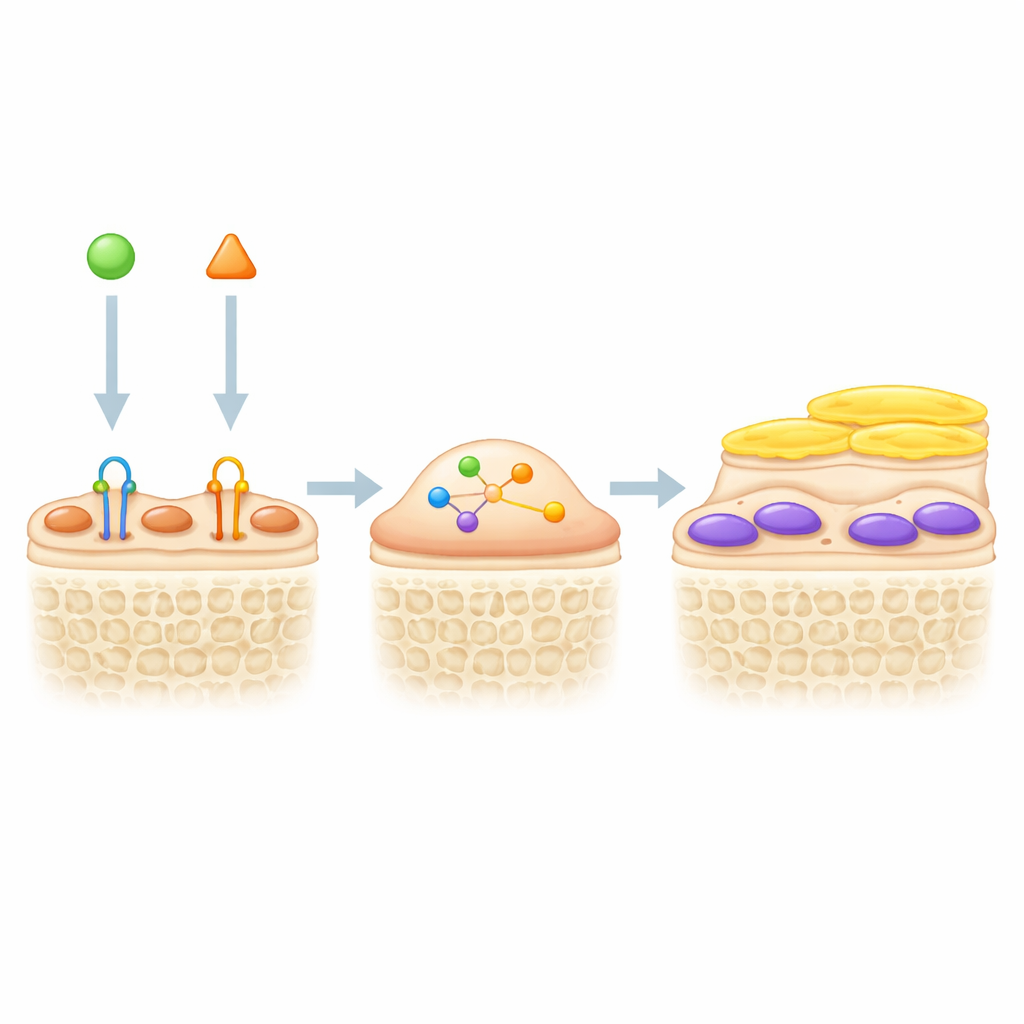
Combinando duas alavancas para ossos mais fortes
Como o bloqueio da esclerostina desperta células de revestimento e o TGF-β as mantém quiescentes, os autores testaram se bloquear ambos os sinais simultaneamente estimularia ainda mais a formação óssea. Em camundongos geneticamente marcados, um anticorpo bloqueador de TGF-β aumentou a espessura e o número de osteoblastos verdes ativos nas superfícies ósseas, especialmente quando combinado ao tratamento que bloqueia a esclerostina. Em um modelo de suspensão dos membros posteriores, que imita a perda óssea por inatividade ou voos espaciais, o bloqueio da esclerostina isoladamente aumentou a massa óssea, mas o tratamento duplo foi ainda mais eficaz. Camundongos que receberam ambos os anticorpos apresentaram maior volume ósseo trabecular, trabéculas mais espessas e mais numerosas, maior formação óssea e menos células reabsorvedoras de osso do que camundongos tratados com apenas um dos fármacos. Marcadores sanguíneos e colorações teciduais sugeriram que a inibição do TGF-β não apenas ajudou a reativar as células de revestimento, mas também reduziu a reabsorção óssea, agindo por mecanismos que complementam o bloqueio da esclerostina.
O que isso pode significar para pacientes
Este trabalho relaciona uma via de sinalização específica, o TGF-β, à decisão que as células ósseas tomam entre repouso e formação, e mostra que reduzir esse sinal pode amplificar os benefícios de um medicamento potente existente para osteoporose que tem a esclerostina como alvo. Embora esses experimentos tenham sido realizados em camundongos e questões importantes de segurança permaneçam — porque o TGF-β atua em muitos órgãos —, o estudo sugere que terapias duplas cuidadosamente ajustadas poderiam tanto estimular formadores de osso dormentes quanto atenuar a perda óssea. A longo prazo, essa estratégia pode se traduzir em tratamentos mais robustos e duradouros para pessoas com osteoporose e outras condições marcadas por perda óssea excessiva.
Citação: Choi, A., Lee, J.Y., Yoon, H. et al. Spatially resolved osteoblast-traced transcriptomics uncovers TGF-β as a combination target with sclerostin in osteoporosis. Bone Res 14, 37 (2026). https://doi.org/10.1038/s41413-026-00521-9
Palavras-chave: osteoporose, osteoblastos, remodelação óssea, sinalização TGF-beta, inibição da esclerostina