Clear Sky Science · nl
Ruimtelijk gereconstrueerde door osteoblasten gevolgde transcriptomica onthult TGF-β als combinatiedoelwit met sclerostine bij osteoporose
Waarom deze botstudie er toe doet
Osteoporose maakt botten broos en breekbaar, vooral bij ouderen. Veel huidige geneesmiddelen remmen ofwel de botafbraak of stimuleren tijdelijk de botaanmaak, maar ze kunnen bijwerkingen hebben en hun effecten kunnen afnemen. Deze studie onderzoekt hoe stille botvormende cellen weer geactiveerd kunnen worden en stelt een nieuwe combinatiebehandelingsstrategie voor die botten krachtiger en duurzamer zou kunnen versterken.
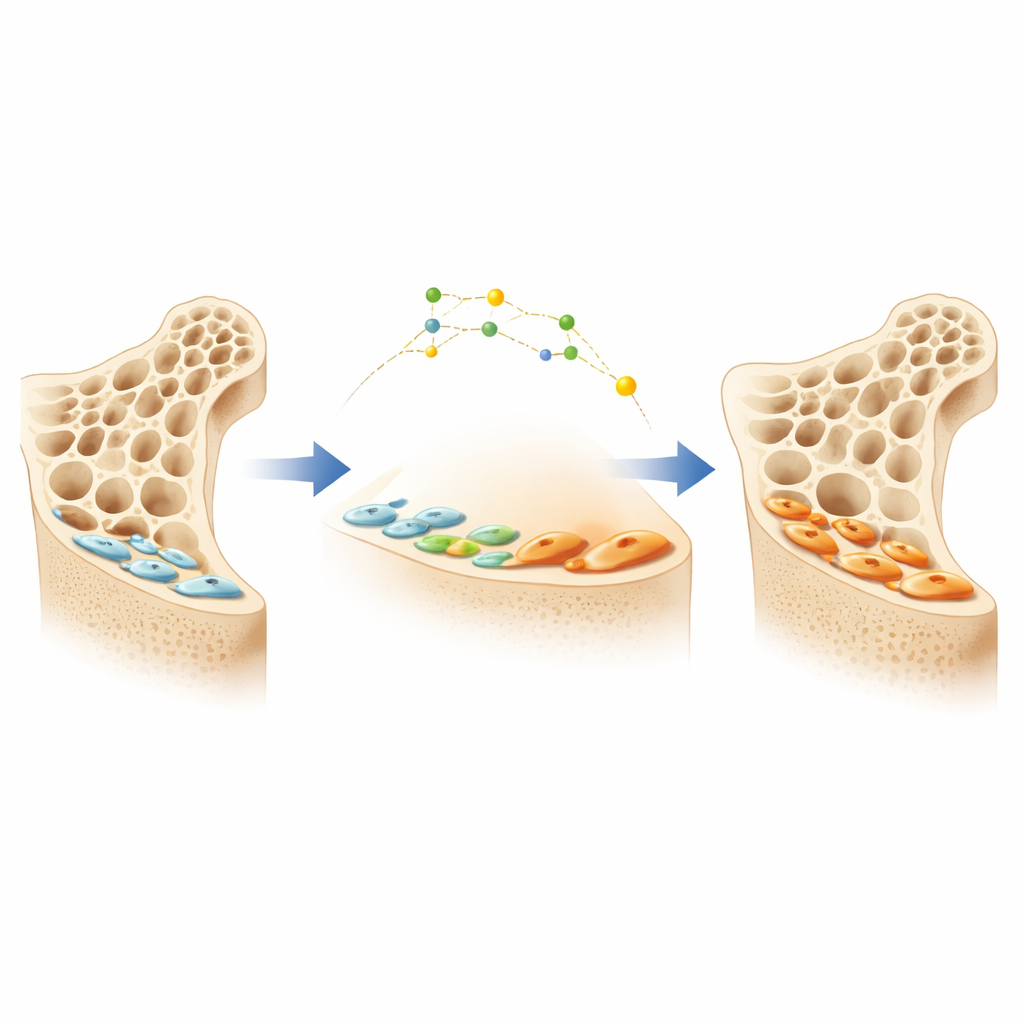
Zij die stilletjes op het botoppervlak werken
Botten worden voortdurend geremodelleerd door twee hoofdceltypen: osteoclasten, die oud bot verwijderen, en osteoblasten, die nieuw bot aanmaken. Wanneer osteoblasten een periode van activiteit beëindigen, sterven veel van hen niet; ze vlakken juist af en worden dunne “botbekledingscellen” die stil op het botoppervlak liggen. Deze stille cellen vormen een grote, verborgen reserve van potentiële botbouwers. Een relatief nieuw osteoporosemedicijn dat een eiwit genaamd sclerostine blokkeert, kan deze bekledingscellen wekken en weer omzetten in actieve osteoblasten, wat leidt tot snelle toename van botmassa. De precieze mechanismen waarmee bekledingscellen tussen rustige en actieve toestanden schakelen, waren echter onduidelijk, wat het lastig maakte om slimmere en duurzamere therapieën te ontwerpen.
Cellen in hun omgeving volgen
De onderzoekers ontwikkelden een aanpak die zij “ruimtelijk gereconstrueerde, door osteoblasten gevolgde transcriptomica” noemen om deze overgangen direct in muizenbot te observeren. Eerst gebruikten ze een genetisch labelingssysteem zodat rijpe osteoblasten en hun afstammelingen groen oplichten, waardoor het team ze kon volgen terwijl ze bekledingscellen werden of door sclerostine-blokkerende antilichamen werden geheractiveerd. Vervolgens combineerden ze dit met een lasergebaseerde bemonsteringsmethode die kleine, precies gekozen regio’s uit botdoorsneden kan uitsnijden terwijl het RNA van elke cel intact blijft. Door het RNA van deze regio’s te sequencen, konden ze zien welke genen aan- of uitgezet waren in actieve osteoblasten, stille bekledingscellen en herwaakte cellen, en dat alles terwijl de locatie van die cellen op het botoppervlak behouden bleef.
Een belangrijke rem op botvorming
Toen het team de genactiviteitsprofielen van actieve, inactieve en geheractiveerde osteoblasten vergeleek, stak één signaalweg met name bovenuit als krachtige rem: de route gecontroleerd door transforming growth factor beta (TGF-β). Stille bekledingscellen vertoonden sterkere TGF-β-activiteit, terwijl actieve osteoblasten—zowel natuurlijk actieve als door sclerostine-gewekte—zwakkere TGF-β-signalen lieten zien. Single-cell sequencing, dat duizenden individuele botcellen analyseert, bevestigde dat de meest actieve osteoblasten consequent lage TGF-β-signalisatie hadden. In in vitro gekweekte botorganoïden duwde toevoeging van TGF-β osteoblasten richting dunnere, minder proliferatieve en meer bekledingscelachtige toestanden. Deze bevindingen wijzen op TGF-β als een schakelaar die quiescentie bevordert en botbouwactiviteit onderdrukt.
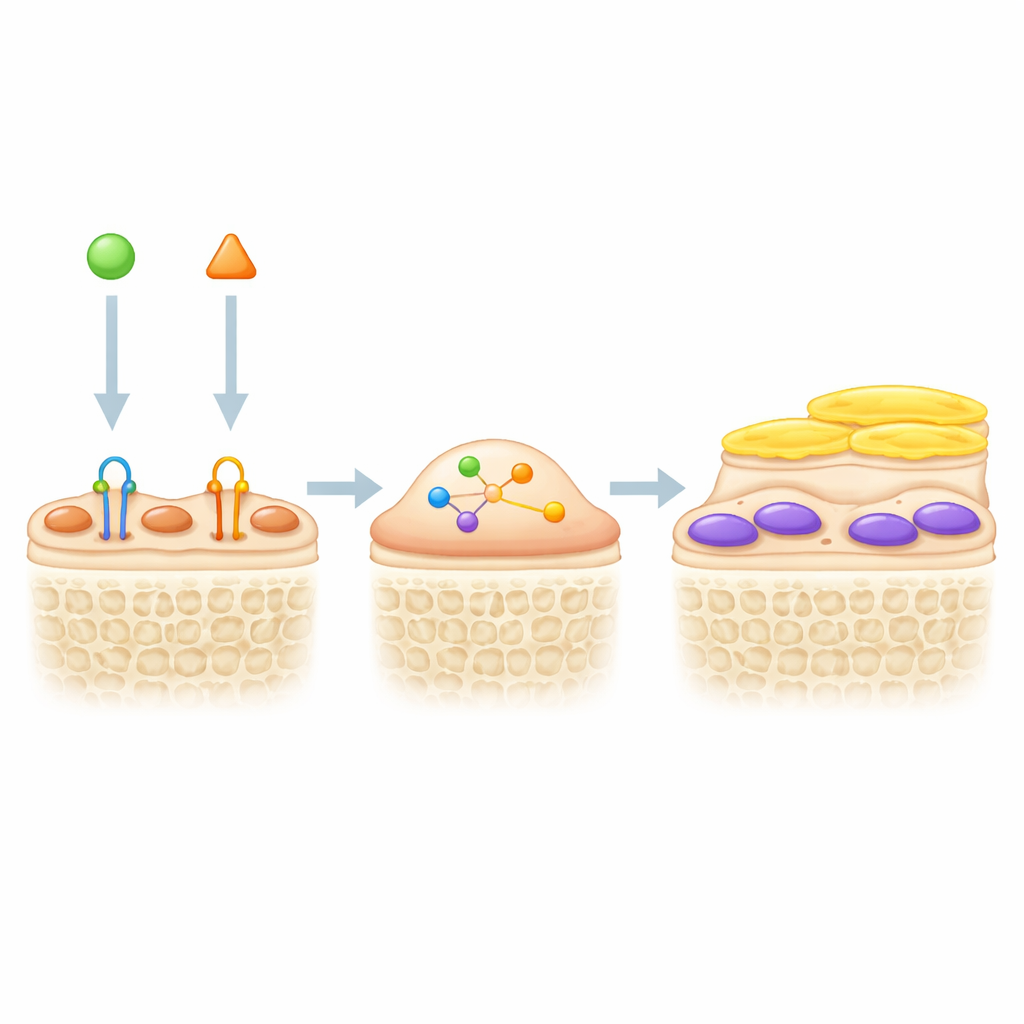
Twee hefbomen combineren voor sterkere botten
Aangezien sclerostine-blokkade bekledingscellen wekt en TGF-β ze juist stil houdt, testten de auteurs of gelijktijdige remming van beide signalen de botvorming zou versterken. In genetisch gelabelde muizen verhoogde een TGF-β-remmend antilichaam de dikte en het aantal actieve groene osteoblasten op botoppervlakken, vooral in combinatie met behandeling tegen sclerostine. In een model van achterste ledemaatontlading, dat botverlies door inactiviteit of ruimtevlucht nabootst, nam de botmassa toe bij sclerostine-blokkade alleen, maar de dubbele behandeling werkte nog beter. Muizen die beide antilichamen kregen, hadden een hogere trabeculaire botvolume, dikkere en talrijkere botstruts, meer botvorming en minder botresorberende cellen dan muizen die slechts één van de geneesmiddelen kregen. Bloedmarkers en weefselkleuring duidden erop dat TGF-β-remming niet alleen hielp bij het reactiveren van bekledingscellen maar ook de botresorptie verminderde, via mechanismen die sclerostine-blokkade aanvullen.
Wat dit voor patiënten kan betekenen
Dit werk koppelt een specifieke signaalweg, TGF-β, aan de beslissing die botcellen nemen tussen rust en opbouw, en toont aan dat het terugschakelen van dit signaal de voordelen van een krachtig bestaand osteoporosemiddel dat sclerostine target, kan versterken. Hoewel deze experimenten in muizen zijn uitgevoerd en belangrijke veiligheidsvragen blijven bestaan—omdat TGF-β in veel organen werkzaam is—suggereert de studie dat zorgvuldig afgestelde combinatietherapieën zowel slapende botbouwers kunnen activeren als botafbraak kunnen matigen. Op de lange termijn zou deze strategie kunnen leiden tot robuustere en duurzamere behandelingen voor mensen met osteoporose en andere aandoeningen die gepaard gaan met excessief botverlies.
Bronvermelding: Choi, A., Lee, J.Y., Yoon, H. et al. Spatially resolved osteoblast-traced transcriptomics uncovers TGF-β as a combination target with sclerostin in osteoporosis. Bone Res 14, 37 (2026). https://doi.org/10.1038/s41413-026-00521-9
Trefwoorden: osteoporose, osteoblasten, botremodellering, TGF-beta signalering, inhibitie van sclerostine