Clear Sky Science · sv
Rumsupplöst osteoblast-spårad transkriptomik avslöjar TGF-β som ett kombinationsmål med sklerostin vid osteoporos
Varför denna benskada-studie är viktig
Osteoporos gör benen lättare att bryta, särskilt hos äldre vuxna. Många nuvarande läkemedel bromsar antingen bennedbrytning eller ger en kortvarig ökning av benbildning, men de kan ha biverkningar och deras effekter kan avta. Denna studie utforskar hur tysta benbildande celler kan väckas till liv igen och föreslår en ny kombinationsbehandlingsstrategi som kan stärka benen mer kraftfullt och hållbart.
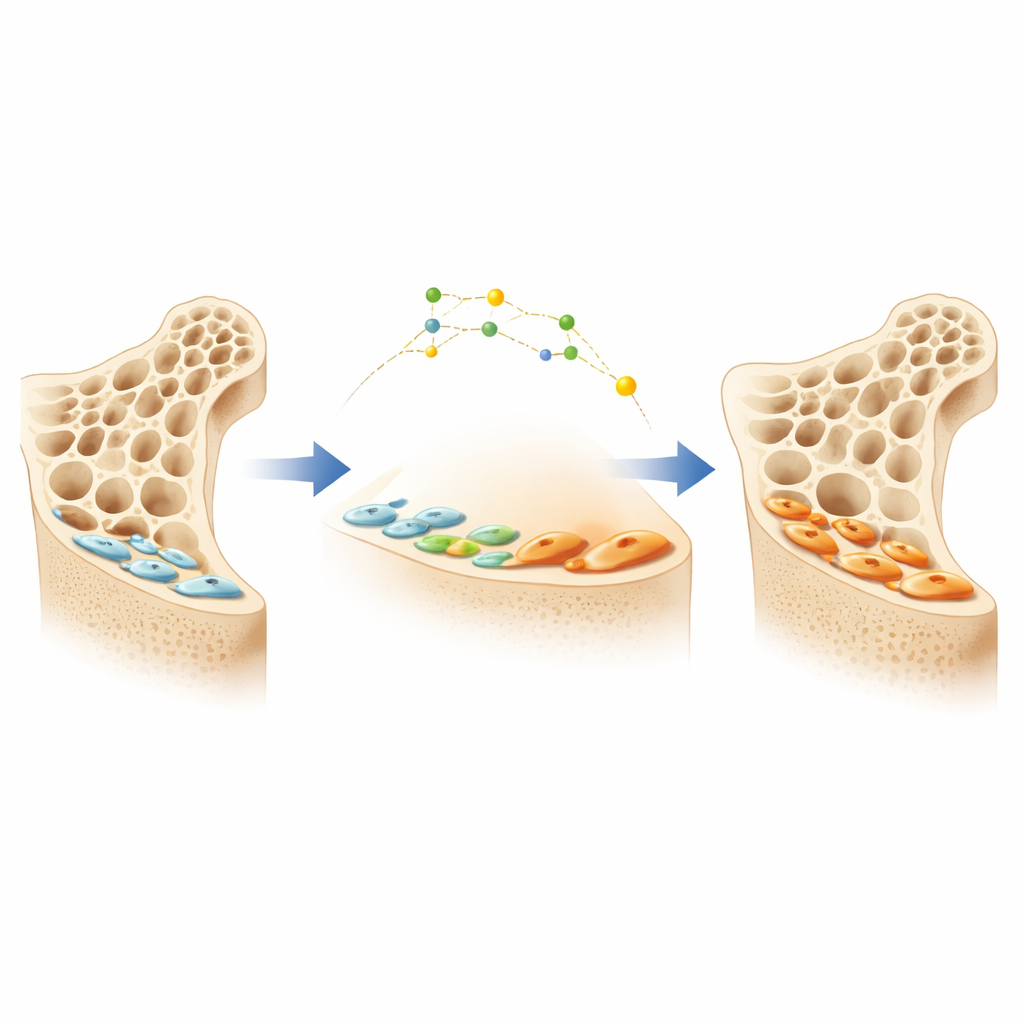
Tysta arbetare på benytan
Benen omformas ständigt av två huvudcelltyper: osteoklaster som tar bort gammalt ben och osteoblaster som bygger nytt ben. När osteoblasterna avslutar en arbetsperiod dör många inte; istället plattar de ut sig och blir tunna ”bone lining cells” som sitter tyst på benytan. Dessa tysta celler utgör ett stort dolt förråd av potentiella benbyggare. Ett nyare osteoporosläkemedel som blockerar ett protein kallat sklerostin kan väcka dessa lining cells och omvandla dem tillbaka till aktiva osteoblaster, vilket ger snabba ökningar i benmassa. Detaljerna kring hur lining cells växlar mellan tysta och aktiva tillstånd har dock varit oklara, vilket försvårar utformningen av smartare, mer långvariga terapier.
Spåra benceller på plats
Forskarna utvecklade en metod de kallar ”spatially resolved osteoblast-traced transcriptomics” för att direkt följa dessa övergångar inne i musben. Först använde de ett genetiskt märkningssystem så att mogna osteoblaster och deras härstamning lyste grönt, vilket gjorde det möjligt för teamet att följa dem när de blev lining cells eller återaktiverades av antikroppar som blockerar sklerostin. Sedan kombinerade de detta med en laserbaserad provtagningsmetod som försiktigt kan skära ut små, precist valda områden från bensnitt samtidigt som varje cells RNA bevaras intakt. Genom att sekvensera RNA från dessa regioner kunde de se vilka gener som var på- eller avstängda i aktiva osteoblaster, tysta lining cells och återväckta celler, samtidigt som de behöll information om var cellerna var lokaliserade på benytan.
En viktig broms på benbyggandet
När teamet jämförde genaktivitetsmönstren hos aktiva, inaktiva och återaktiverade osteoblaster framträdde ett signalsystem som en stark broms: vägen styrd av transforming growth factor beta (TGF-β). Tysta lining cells visade högre TGF-β-aktivitet, medan aktiva osteoblaster—oavsett om de var naturligt aktiva eller återuppväckta genom sklerostinblockad—visade svagare TGF-β-signaler. Enkelcellssekvensering, som analyserar tusentals individuella benceller, bekräftade att de mest aktiva osteoblasterna konsekvent hade låg TGF-β-signalering. I laboratorieodlade benorganoider drev tillförsel av TGF-β osteoblaster att bli tunnare, mindre proliferativa och mer lika lining cells. Dessa fynd pekar på TGF-β som en strömbrytare som främjar vilande tillstånd och begränsar benbyggande aktivitet.
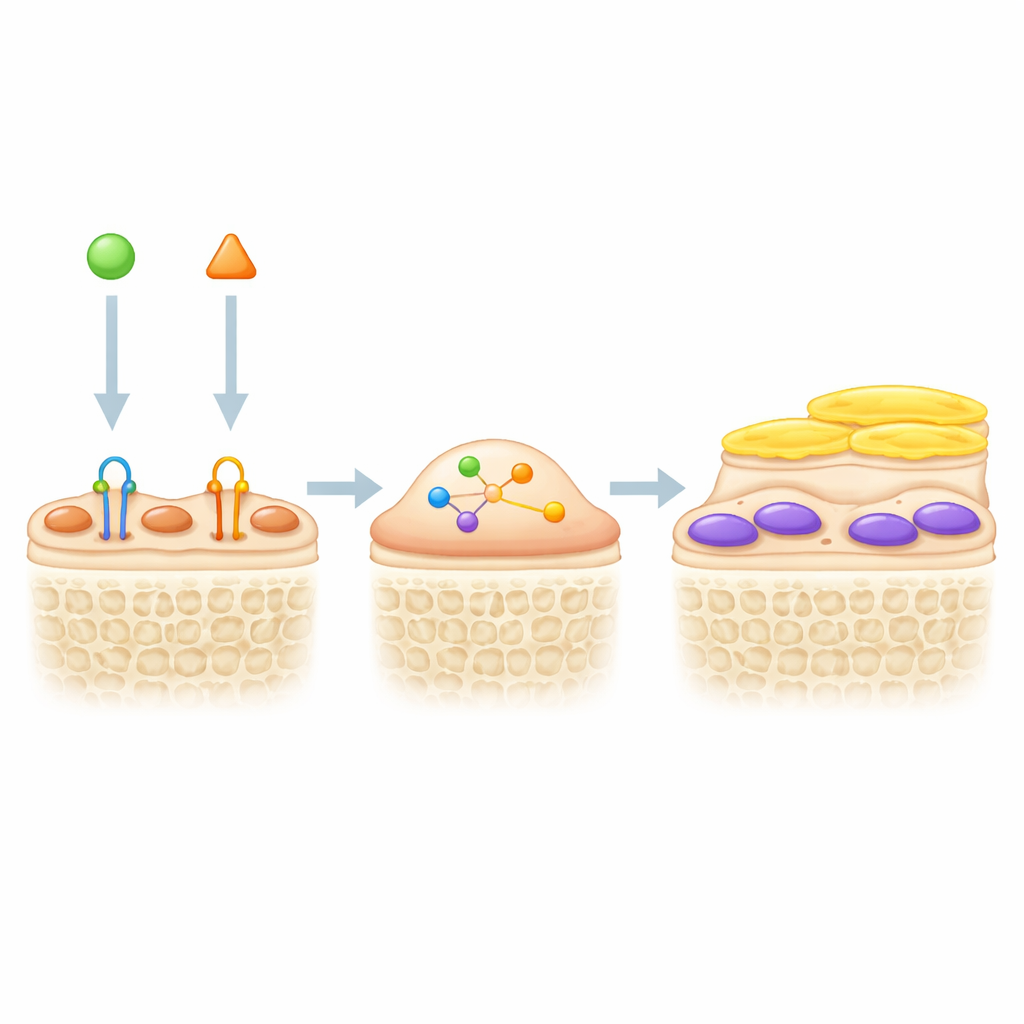
Kombinera två spakar för starkare ben
Eftersom sklerostinblockad väcker lining cells och TGF-β håller dem tysta, testade författarna om blockering av båda signalerna tillsammans skulle öka benbildningen. I genetiskt märkta möss ökade en TGF-β-blockerande antikropp tjockleken och antalet aktiva gröna osteoblaster på benytor, särskilt i kombination med behandling som blockerar sklerostin. I en modell med avlastning av bakben, som efterliknar benförlust vid inaktivitet eller rymdfärder, ökade sklerostinblockad ensam benmassan, men dubbelbehandlingen gav ännu bättre resultat. Möss som fick båda antikropparna hade högre trabekulär benvolym, tjockare och fler benbalkar, mer benbildning och färre benresorberande celler än möss som fick något av läkemedlen ensam. Blodmarkörer och vävnadsfärgningar antydde att TGF-β-hämning inte bara hjälpte till att återaktivera lining cells utan också minskade bennedbrytning, genom mekanismer som kompletterar sklerostinblockad.
Vad detta kan betyda för patienter
Detta arbete kopplar en specifik signalväg, TGF-β, till beslutet som benceller fattar mellan vila och uppbyggnad, och visar att nedreglering av denna signal kan förstärka fördelarna av ett kraftfullt befintligt osteoporosl läkemedel som riktar sig mot sklerostin. Medan dessa experiment utfördes i möss och viktiga säkerhetsfrågor kvarstår—eftersom TGF-β verkar i många organ—tyder studien på att noggrant avvägda dubbla terapier både kan väcka sovande benbyggare och dämpa bennedbrytning. På sikt skulle denna strategi kunna omsättas i robustare, mer hållbara behandlingar för personer med osteoporos och andra tillstånd som kännetecknas av överdriven benförlust.
Citering: Choi, A., Lee, J.Y., Yoon, H. et al. Spatially resolved osteoblast-traced transcriptomics uncovers TGF-β as a combination target with sclerostin in osteoporosis. Bone Res 14, 37 (2026). https://doi.org/10.1038/s41413-026-00521-9
Nyckelord: osteoporos, osteoblaster, bennedbrytning och -omsättning, TGF-beta-signalering, hämning av sklerostin