Clear Sky Science · ru
Пространственно разрешённая остеобластовая трассированная транскриптомика выявляет TGF-β как комбинируемую мишень с склеростином при остеопорозе
Почему это исследование костей важно
Остеопороз делает кости хрупкими и склонными к переломам, особенно у пожилых людей. Многие существующие препараты либо замедляют разрушение кости, либо кратковременно повышают образование кости, но они могут иметь побочные эффекты, а их эффект со временем ослабевает. В этом исследовании изучают, как «спящие» клетки, формирующие кость, могут быть вновь активированы, и предлагают новую стратегию комбинированного лечения, которая может более сильно и долговременно укреплять кости.
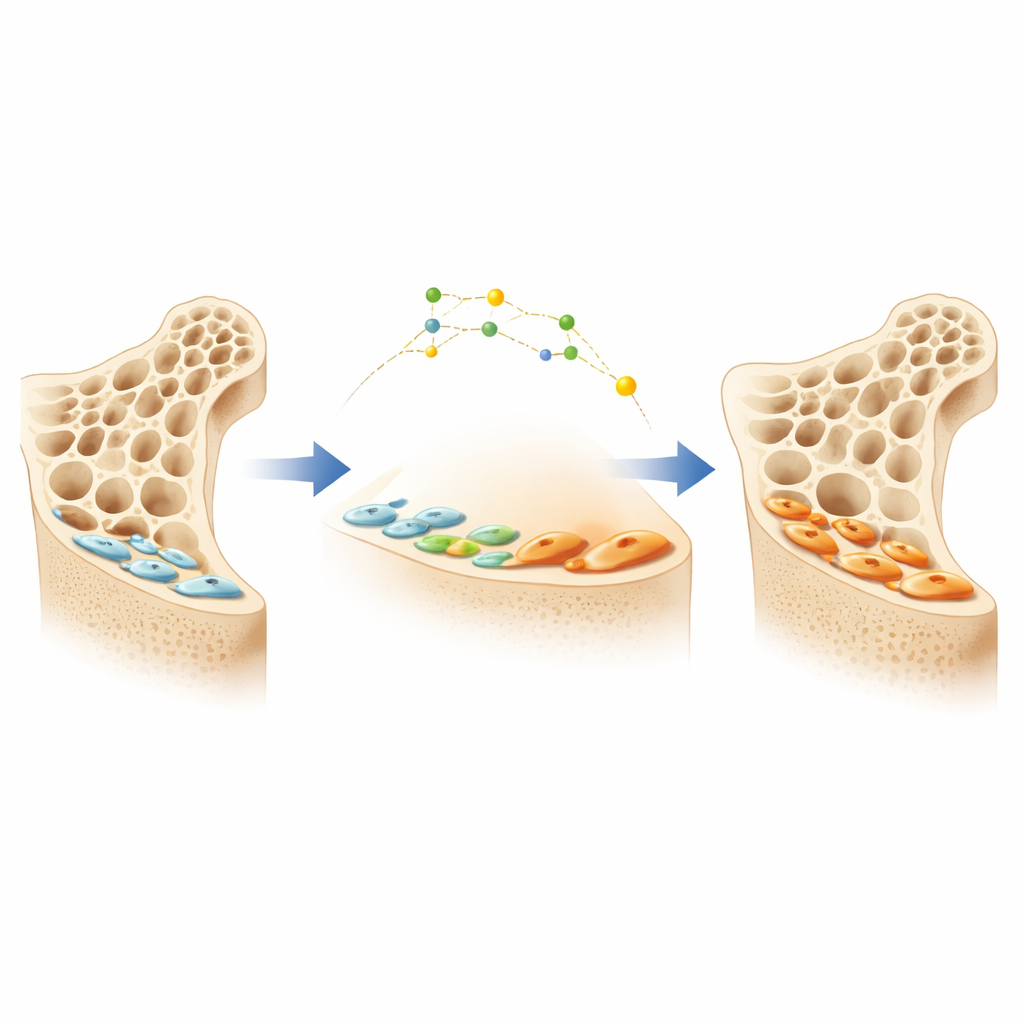
Тихие рабочие на поверхности кости
Кости постоянно ремоделируются двумя основными типами клеток: остеокластами, которые удаляют старую кость, и остеобластами, которые формируют новую кость. Когда остеобласты завершают фазу активности, многие из них не умирают; вместо этого они уплощаются и превращаются в тонкие «покровные клетки», располагающиеся тихо на поверхности кости. Эти молчаливые клетки представляют собой большой скрытый резерв потенциальных строителей кости. Новый препарат от остеопороза, блокирующий белок под названием склеростин, может разбудить эти покровные клетки и вернуть их в активные остеобласты, что приводит к быстрому увеличению массы кости. Однако детали того, как покровные клетки переключаются между тихим и активным состояниями, оставались неясными, что затрудняло разработку более изощрённых и долговечных терапий.
Отслеживание костных клеток на месте
Исследователи разработали подход, который они называют «пространственно разрешённой остеобластовой трассированной транскриптомикой», чтобы наблюдать эти переходы непосредственно внутри кости мыши. Сначала они использовали генетическую систему маркировки, чтобы зрелые остеобласты и их потомки светились зелёным, что позволяло команде прослеживать их превращение в покровные клетки или их реактивацию анти-телами, блокирующими склеростин. Затем это сочетали с лазерным методом выборки, который аккуратно вырезает крошечные, точно выбранные участки из срезов кости, сохраняя при этом РНК каждой клетки нетронутой. Секвенируя РНК из этих областей, они могли увидеть, какие гены включены или выключены в активных остеобластах, тихих покровных клетках и вновь пробуждённых клетках, при этом сохраняя информацию о том, где именно эти клетки находились на поверхности кости.
Ключевой тормоз образования кости
Сравнивая паттерны активности генов в активных, неактивных и реактивированных остеобластах, исследователи выявили одну сигнальную систему как мощный тормоз: путь, контролируемый трансформирующим фактором роста бета (TGF-β). В тихих покровных клетках активность TGF-β была сильнее, тогда как в активных остеобластах — как естественно активных, так и вновь пробуждённых после блокирования склеростина — сигналы TGF-β были слабее. Секвенирование отдельных клеток, анализирующее тысячи отдельных клеток кости, подтвердило, что наиболее активные остеобласты последовательно характеризуются низкой сигнализацией TGF-β. В лабораторных органоидах кости добавление TGF-β приводило к тому, что остеобласты становились более плоскими, меньше пролиферировали и приобретали черты покровных клеток. Эти данные указывают на TGF-β как на переключатель, который способствует покою и сдерживает костеобразующую активность.
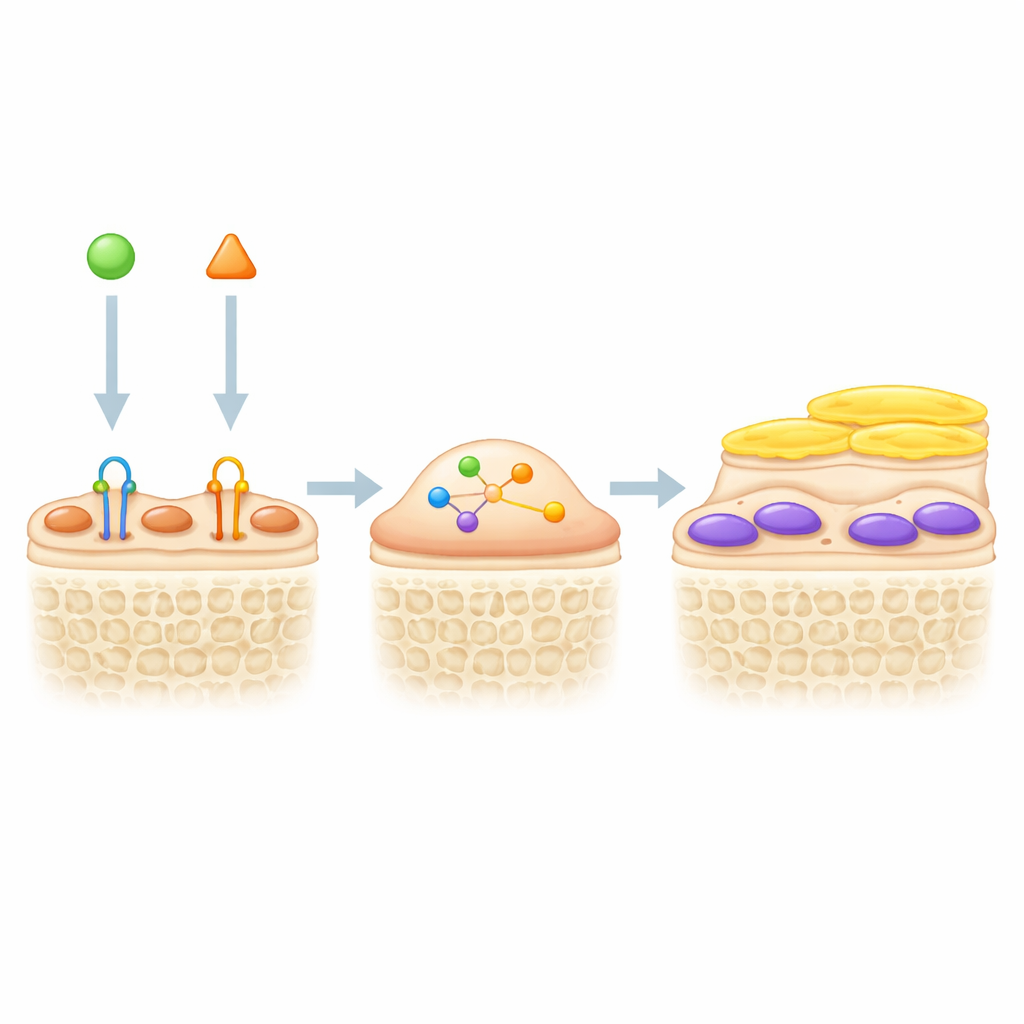
Комбинация двух рычагов для более крепких костей
Поскольку блокада склеростина пробуждает покровные клетки, а TGF-β удерживает их в покое, авторы проверили, усилит ли одновременная блокада обоих сигналов образование кости. У генетически меченых мышей антитело, блокирующее TGF-β, увеличивало толщину и число активных зелёных остеобластов на поверхностях кости, особенно в сочетании с лечением, блокирующим склеростин. В модели разгрузки задних конечностей, имитирующей потерю кости при неактивности или космическом полёте, одна лишь блокада склеростина увеличивала массу кости, но комбинированная терапия дала ещё лучший эффект. У мышей, получавших оба антитела, был выше трабекулярный объём кости, толще и более многочисленны костные тяги, увеличено образование кости и снижено число костеразрушающих клеток по сравнению с животными, получавшими только один препарат. Маркеры в крови и окраска тканей показали, что ингибиция TGF-β не только помогала реактивировать покровные клетки, но и уменьшала резорбцию кости, действуя через механизмы, дополняющие блокаду склеростина.
Что это может значить для пациентов
Эта работа связывает конкретный сигнальный путь, TGF-β, с решением, которое принимают костные клетки между отдыхом и строительством, и показывает, что ослабление этого сигнала может усилить преимущества мощного существующего препарата от остеопороза, нацеленного на склеростин. Несмотря на то, что эксперименты проводилиcь на мышах и остаются важные вопросы безопасности — поскольку TGF-β действует во многих органах — исследование предполагает, что тщательно настроенные двойные терапии могут одновременно разбудить «спящих» строителей кости и уменьшить её разрушение. В долгосрочной перспективе такая стратегия может превратиться в более надёжные и долговечные лечения для людей с остеопорозом и другими состояниями, сопровождающимися избыточной потерей кости.
Цитирование: Choi, A., Lee, J.Y., Yoon, H. et al. Spatially resolved osteoblast-traced transcriptomics uncovers TGF-β as a combination target with sclerostin in osteoporosis. Bone Res 14, 37 (2026). https://doi.org/10.1038/s41413-026-00521-9
Ключевые слова: остеопороз, остеобласты, ремоделирование кости, сигнальный путь TGF-бета, ингибиция склеростина