Clear Sky Science · he
טרנסקריפטומיקה ממוקמת שעוקבת אחר אוסטאובלאסטים חושפת את TGF-β כמטרה משולבת עם סקלרוסטין באוסטאופורוזיס
מדוע מחקר העצם הזה חשוב
אוסטאופורוזיס גורם לעצמות להיחלש ולהיות קלות לשבירה, במיוחד במבוגרים. תרופות רבות כיום או מאטות את פירוק העצם או מגרות זמנית את בניית העצם, אך הן עלולות לגרום תופעות לוואי והתועלת שלהן עלולה לדעוך. מחקר זה בוחן כיצד ניתן להפעיל מחדש תאים שקטים שמייצרים עצם, ומציע אסטרטגיית טיפול משולבת חדשה שעשויה לחזק עצמות בעוצמה ומשך זמן גדולים יותר.
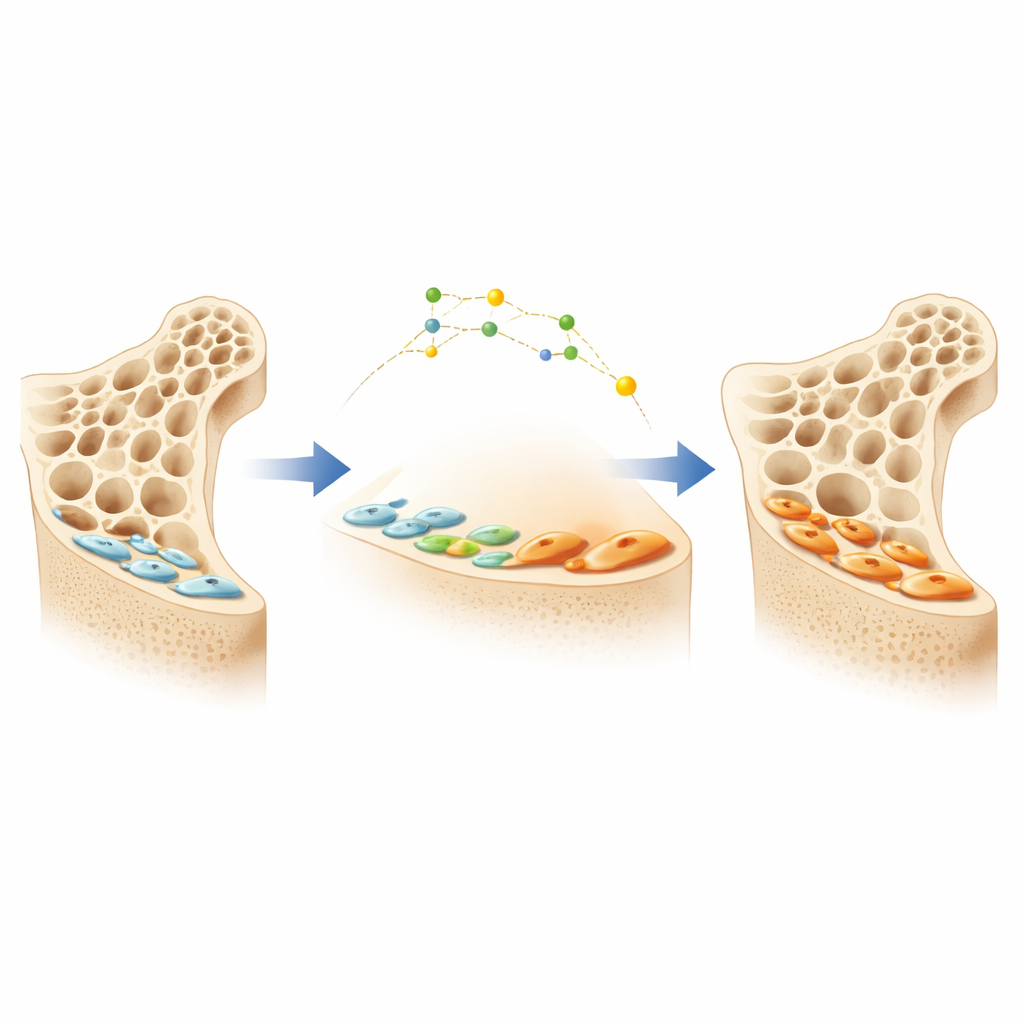
עובדים שקטים על פני העצם
העצמות עוברים חידוש מתמיד על ידי שני סוגי תאים עיקריים: אוסטיאוקלסטים, שמסירים עצם ישן, ואוסטאובלאסטים, שמבנים עצם חדש. כאשר האוסטאובלאסטים מסיימים פרץ פעילות, רבים לא מתים; במקום זאת הם משטחים והופכים לתאי "ריפוד" דקים שיושבים בשקט על פני העצם. התאים השקטים האלה יוצרים מאגר חבוי גדול של בוני עצם פוטנציאליים. תרופה חדשה לאוסטאופורוזיס החוסמת חלבון בשם סקלרוסטין יכולה להעיר את תאי הריפוד האלה ולהחזירם לאוסטאובלאסטים פעילים, מה שמוביל לגידול מהיר במסת העצם. עם זאת, הפרטים של כיצד תאי הריפוד עוברים בין מצבי שקט לפעילות היו בלתי ברורים, וזה מקשה על עיצוב טיפולים חכמים ובעלי השפעה ארוכת טווח.
מעקב אחר תאי עצם במקומם
החוקרים פיתחו גישה שהם מכנים "טרנסקריפטומיקה ממוקמת שעוקבת אחר אוסטאובלאסטים" כדי לצפות במעברים הללו ישירות בתוך עצם של עכבר. תחילה השתמשו במערכת תיוג גנטית כך שאוסטאובלאסטים בוגרים וצאצאיהם זהרו בירוק, מה שאפשר לצוות לעקוב אחריהם כשהפכו לתאי ריפוד או כשהופעלו מחדש על ידי נוגדנים החוסמי סקלרוסטין. לאחר מכן שילבו זאת עם שיטת דגימה מבוססת לייזר שיכולה לחתוך בעדינות אזורים זעירים ונבחרים בדיוק מפרוסות עצם תוך שמירה על ה-RNA של כל תא. על ידי ריצוף RNA מאזורים אלו הם יכלו לראות אילו גנים נדלקים או כובים באוסטאובלאסטים פעילים, בתאי ריפוד שקטים ובתאים שהוחזרו לפעילות, וכל זאת תוך שמירה על מיקום התאים על פני העצם.
בלם מרכזי על בניית העצם
כאשר הקבוצה השוותה דפוסי פעילות גנטית של אוסטאובלאסטים פעילים, לא פעילים ומופעלים מחדש, מערכת איתות אחת בלטה כבלם רב עוצמה: הנתיב הנשלט על ידי גורם הצמיחה המטרנספורמינג בטא (TGF-β). בתאי הריפוד השקטים נצפתה פעילות TGF-β חזקה יותר, בעוד באוסטאובלאסטים פעילים—בין אם באופן טבעי או שהופעלו מחדש על ידי חסימת סקלרוסטין—נראו איתותי TGF-β מוחלשים. ריצוף תא יחיד, האנליזה של אלפי תאי עצם בודדים, אישר שהאוסטאובלאסטים הפעילים ביותר באופן עקבי הציגו איתות TGF-β נמוך. באורגנואידים של עצם שגודלו במעבדה, הוספת TGF-β דחפה אוסטאובלאסטים להפוך לדקים יותר, פחות מתחלקים ויותר בדומה לתאי ריפוד. ממצאים אלה מצביעים על TGF-β כמפסל שמקדם שקט ומגביל את פעילות בניית העצם.
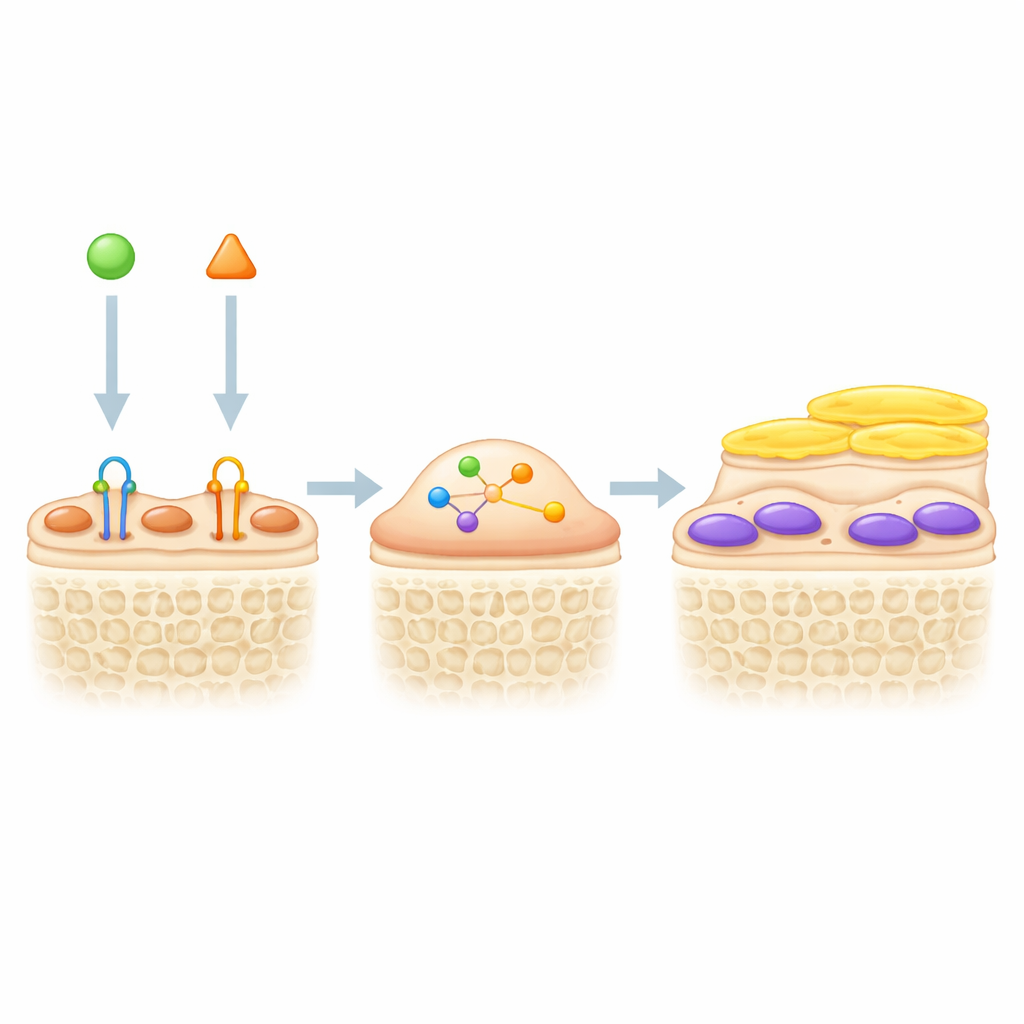
שילוב שתי מניפות לעצמות חזקות יותר
מכיוון שחסימת סקלרוסטין מעירה תאי ריפוד ו-TGF-β משמר אותם בשקט, המחברים בדקו האם חסימת שני האותות יחד תחזק את בניית העצם. בעכברים מתויגים גנטית, נוגדן החוסם TGF-β הגדיל את עובי ומספר האוסטאובלאסטים הירוקים הפעילים על פני העצם, במיוחד בשילוב עם טיפול החוסם סקלרוסטין. במודל של הורדת עומס על הגפה האחורית, המדמה איבוד עצם בשל חוסר פעילות או טיסת חלל, חסימת סקלרוסטין לבדה הגדילה את מסת העצם, אך הטיפול הכפול השיג תוצאה טובה עוד יותר. עכברים שקיבלו את שני הנוגדנים הראו נפח עצם טרבקולרי גבוה יותר, קורות עצם עבות ומרובות יותר, יותר בניית עצם ופחות תאים מפרקים לעומת עכברים שקיבלו כל תרופה בנפרד. סימני דם וצביעה רקמתית הציעו שחסימת TGF-β לא רק סייעה להחזיר תאי ריפוד לפעילות אלא גם הפחיתה את פירוק העצם, ופעלה דרך מנגנונים שמשלימים את חסימת הסקלרוסטין.
מה זה עשוי להכיל למטופלים
עבודה זו מקשרת נתיב איתות ספציפי, TGF-β, להחלטה של תאי עצם בין מנוחה לבניה, ומדגימה שהנמכת אות זה יכולה להגביר את היתרונות של תרופה עוצמתית קיימת לאוסטאופורוזיס המכוונת לסקלרוסטין. בעוד שהניסויים הללו בוצעו בעכברים ונשארות שאלות בטיחות חשובות—כי TGF-β פועל באיברים רבים—המחקר מציע שטיפולים משולבים ומותאמים בקפידה עשויים גם לעורר בוני עצם ישנים וגם לרכך את פירוק העצם. בטווח הארוך, אסטרטגיה זו עשויה להתרגם לטיפולים עמידים וחזקים יותר עבור אנשים החיים עם אוסטאופורוזיס ומצבים אחרים המתאפיינים באובדן עצם מופרז.
ציטוט: Choi, A., Lee, J.Y., Yoon, H. et al. Spatially resolved osteoblast-traced transcriptomics uncovers TGF-β as a combination target with sclerostin in osteoporosis. Bone Res 14, 37 (2026). https://doi.org/10.1038/s41413-026-00521-9
מילות מפתח: אוסטאופורוזיס, אוסטאובלאסטים, חידוש עצם, אותות TGF-β, עיכוב סקלרוסטין