Clear Sky Science · de
Räumlich aufgelöste, osteoblast-verfolgte Transkriptomik enthüllt TGF-β als Kombinationsziel mit Sklerostin bei Osteoporose
Warum diese Knochenstudie wichtig ist
Osteoporose macht Knochen brüchig und leicht verletzbar, besonders bei älteren Menschen. Viele der derzeitigen Medikamente verlangsamen entweder den Knochenabbau oder steigern die Knochenbildung nur kurzzeitig, können Nebenwirkungen haben und zeigen mit der Zeit nachlassende Effekte. Diese Studie untersucht, wie ruhende knochenbildende Zellen wieder aktiviert werden können, und schlägt eine neue Kombinationsbehandlungsstrategie vor, die Knochen nachhaltiger und wirkungsvoller stärken könnte.
Stille Arbeiter an der Knochenoberfläche
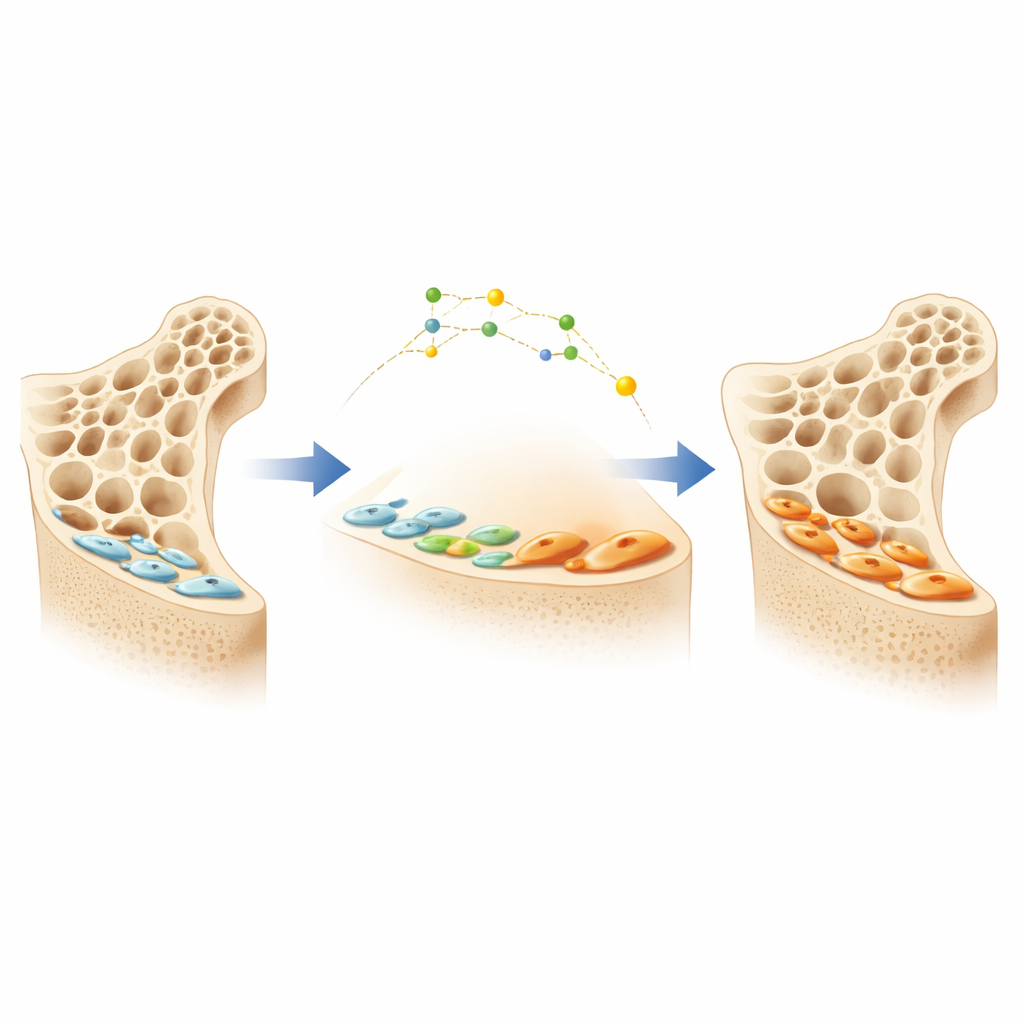
Knochen werden ständig von zwei Hauptzelltypen umgebaut: Osteoklasten, die alten Knochen entfernen, und Osteoblasten, die neuen Knochen aufbauen. Wenn Osteoblasten eine Arbeitsschub beenden, sterben viele nicht; stattdessen flachen sie ab und werden zu dünnen „Knochenoberflächenzellen“ (lining cells), die ruhig auf der Knochenoberfläche sitzen. Diese stillen Zellen bilden ein großes verborgenes Reservoir potenzieller Knochenbildner. Ein neueres Osteoporosemedikament, das ein Protein namens Sklerostin blockiert, kann diese Lining-Zellen wecken und sie wieder zu aktiven Osteoblasten machen, was zu schnellen Zuwächsen an Knochenmasse führt. Die genauen Mechanismen, wie Lining-Zellen zwischen Ruhe- und Aktivzustand wechseln, waren jedoch bislang unklar, was die Entwicklung intelligenterer, langlebigerer Therapien erschwert.
Knochenzellen an ihrem Ort verfolgen
Die Forscher entwickelten einen Ansatz, den sie „räumlich aufgelöste, osteoblast-verfolgte Transkriptomik“ nennen, um diese Übergänge direkt im Maus-Knochen zu beobachten. Zunächst nutzten sie ein genetisches Markierungssystem, sodass reife Osteoblasten und ihre Nachfahren grün leuchteten und das Team ihnen folgen konnte, wenn sie zu Lining-Zellen wurden oder durch sklerostinblockierende Antikörper reaktiviert wurden. Dann kombinierten sie dies mit einer laserbasierten Probennahme, die winzige, präzise ausgewählte Regionen aus Knochenschnitten schonend ausschneiden kann, während die RNA jeder Zelle intakt bleibt. Durch das Sequenzieren der RNA aus diesen Regionen konnten sie sehen, welche Gene in aktiven Osteoblasten, ruhenden Lining-Zellen und reaktivierten Zellen ein- oder ausgeschaltet waren, und das alles bei Erhalt der genauen Lage dieser Zellen auf der Knochenoberfläche.
Eine wichtige Bremse für die Knochenbildung
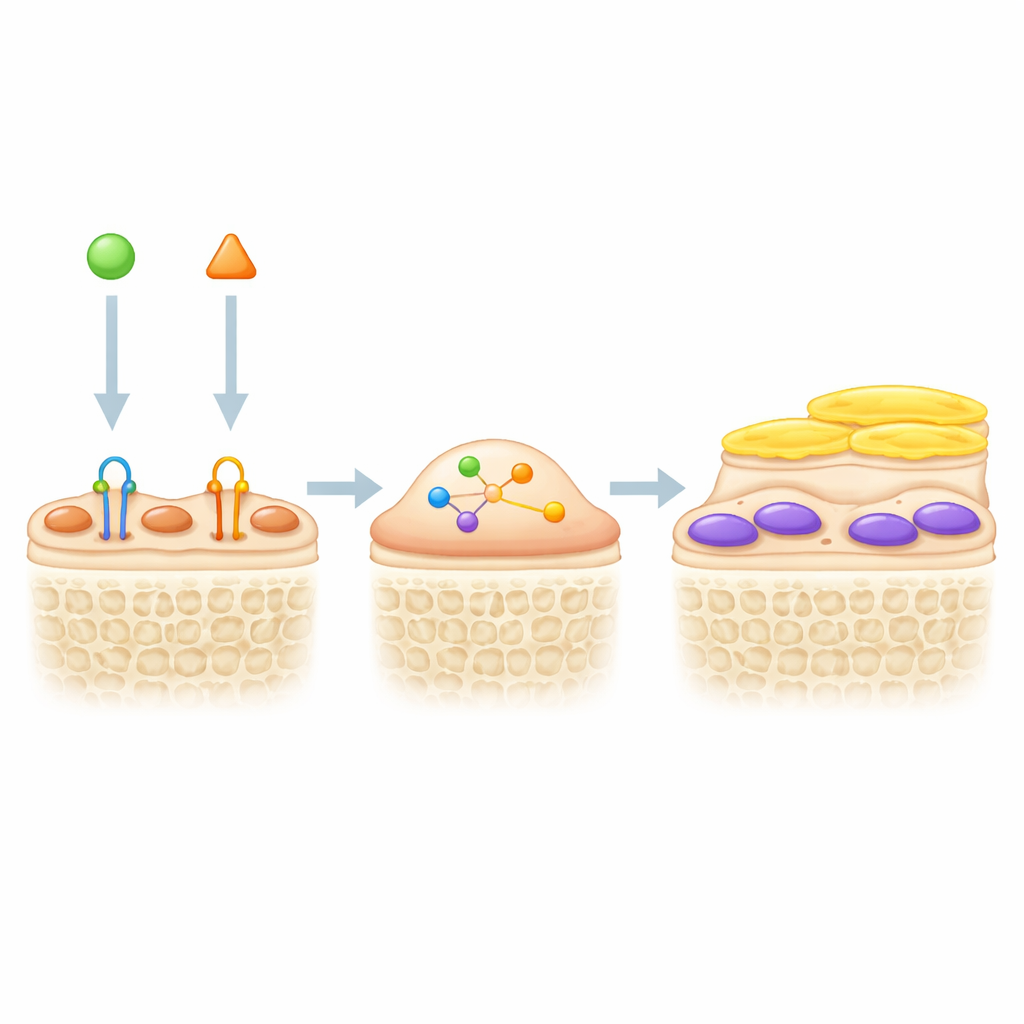
Als das Team die Genaktivitätsmuster aktiver, inaktiver und reaktivierter Osteoblasten verglich, hob sich ein Signalsystem als starke Bremse hervor: der Signalweg, der durch das Transforming Growth Factor Beta (TGF-β) gesteuert wird. Ruhende Lining-Zellen zeigten stärkere TGF-β-Aktivität, während aktive Osteoblasten — ob natürlicherweise aktiv oder durch Sklerostin-Blockade reaktiviert — schwächere TGF-β-Signale aufwiesen. Einzelzell-Sequenzierungen, die Tausende einzelner Knochenzellen analysieren, bestätigten, dass die aktivsten Osteoblasten durchgängig niedrige TGF-β-Signalisierung hatten. In im Labor gezüchteten Knochenorganoiden bewirkte die Zugabe von TGF-β, dass Osteoblasten dünner, weniger proliferativ und mehr Lining-Zellen-ähnlich wurden. Diese Ergebnisse deuten darauf hin, dass TGF-β als Schalter wirkt, der Ruhe fördert und die knochenbildende Aktivität hemmt.
Zwei Hebel kombinieren für stärkere Knochen
Da Sklerostin-Blockade Lining-Zellen weckt und TGF-β sie ruhig hält, testeten die Autoren, ob das gleichzeitige Blockieren beider Signale die Knochenbildung verstärkt. In genetisch markierten Mäusen erhöhte ein TGF-β-blockierender Antikörper die Dicke und Zahl aktiver grüner Osteoblasten auf Knochenoberflächen, besonders in Kombination mit einer Sklerostin-blockierenden Behandlung. In einem Modell der Hintergliedmaßen-Entlastung, das Knochenverlust durch Inaktivität oder Raumfahrt nachahmt, steigerte allein die Sklerostin-Blockade die Knochenmasse, doch die Doppelbehandlung schnitt noch besser ab. Mäuse, die beide Antikörper erhielten, wiesen ein höheres trabekuläres Knochenvolumen, dickere und zahlreichere Knochenbälkchen, mehr Knochenbildung und weniger knochenabbauende Zellen auf als Mäuse, die nur eines der Medikamente bekamen. Blutmarker und Gewebefärbungen deuteten darauf hin, dass die TGF-β-Inhibition nicht nur half, Lining-Zellen zu reaktivieren, sondern auch den Knochenabbau reduzierte — durch Mechanismen, die die Sklerostin-Blockade ergänzen.
Was das für Patientinnen und Patienten bedeuten könnte
Diese Arbeit verknüpft einen spezifischen Signalweg, TGF-β, mit der Entscheidung von Knochenzellen zwischen Ruhen und Bauen und zeigt, dass das Absenken dieses Signals die Vorteile eines wirksamen bestehenden Osteoporosemittels, das auf Sklerostin abzielt, verstärken kann. Obwohl diese Experimente an Mäusen durchgeführt wurden und wichtige Sicherheitsfragen offenbleiben — da TGF-β in vielen Organen wirkt — legt die Studie nahe, dass sorgfältig abgestimmte Doppeltherapien sowohl schlafende Knochenbildner reaktivieren als auch den Knochenabbau dämpfen könnten. Langfristig könnte diese Strategie in robustere, dauerhaftere Behandlungen für Menschen mit Osteoporose und anderen Erkrankungen mit übermäßigem Knochenverlust übersetzt werden.
Zitation: Choi, A., Lee, J.Y., Yoon, H. et al. Spatially resolved osteoblast-traced transcriptomics uncovers TGF-β as a combination target with sclerostin in osteoporosis. Bone Res 14, 37 (2026). https://doi.org/10.1038/s41413-026-00521-9
Schlüsselwörter: Osteoporose, Osteoblasten, Knochenumbau, TGF-beta-Signalisierung, Sklerostin-Inhibition