Clear Sky Science · it
Trascrittomica spazialmente risolta tracciata negli osteoblasti rivela il TGF-β come bersaglio combinato con la sclerostina nell’osteoporosi
Perché questo studio sulle ossa è importante
L’osteoporosi rende le ossa fragili e facilmente soggette a fratture, soprattutto nelle persone anziane. Molti farmaci attuali rallentano la perdita ossea o stimolano temporaneamente la formazione di nuovo osso, ma possono avere effetti collaterali e i loro benefici possono diminuire nel tempo. Questo studio esplora come le cellule formatrici d’osso silenti possano essere riattivate e propone una nuova strategia terapeutica combinata che potrebbe rafforzare le ossa in modo più potente e duraturo.
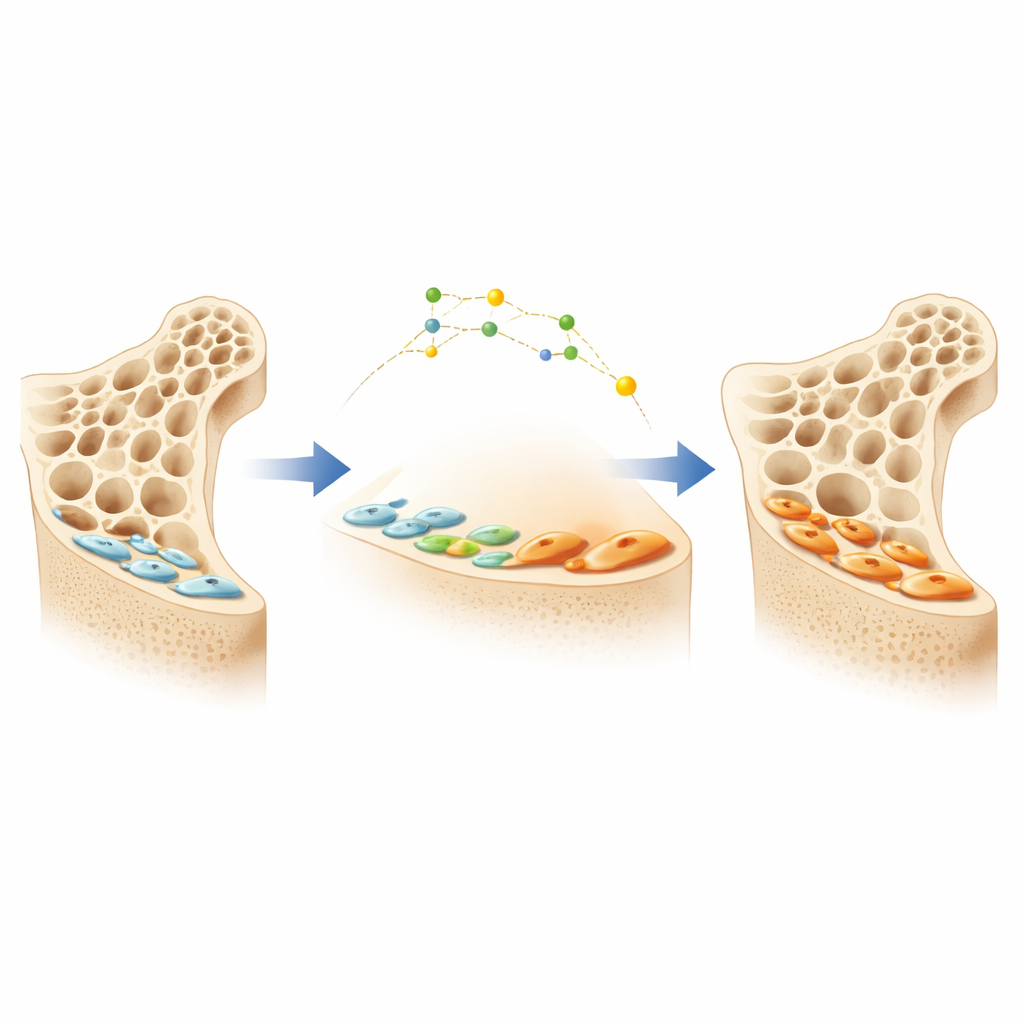
Operatori silenziosi sulla superficie ossea
Le ossa sono continuamente rimodellate da due tipi cellulari principali: gli osteoclasti, che rimuovono l’osso vecchio, e gli osteoblasti, che depongono nuovo osso. Quando gli osteoblasti terminano un periodo di intensa attività, molti non muoiono; invece si appiattiscono e diventano sottili “cellule di rivestimento” dell’osso che rimangono silenti sulla superficie. Queste cellule silenti costituiscono una grande riserva nascosta di potenziali costruttori ossei. Un farmaco più recente per l’osteoporosi che blocca una proteina chiamata sclerostina può risvegliare queste cellule di rivestimento e trasformarle nuovamente in osteoblasti attivi, portando a rapidi aumenti della massa ossea. Tuttavia, i meccanismi con cui le cellule di rivestimento passano dallo stato silente a quello attivo non erano chiari, ostacolando la progettazione di terapie più intelligenti e durature.
Tracciare le cellule ossee nel loro luogo
I ricercatori hanno messo a punto un approccio che chiamano “trascrittomica spazialmente risolta tracciata negli osteoblasti” per osservare direttamente queste transizioni all’interno dell’osso del topo. Prima hanno utilizzato un sistema di marcatura genetica in modo che gli osteoblasti maturi e i loro discendenti brillassero di verde, consentendo al gruppo di seguirli mentre diventavano cellule di rivestimento o venivano riattivati da anticorpi che bloccano la sclerostina. Hanno poi combinato questo con un metodo di campionamento basato su laser in grado di asportare delicatamente minuscole regioni scelte con precisione da sezioni ossee, mantenendo intatto l’RNA di ogni cellula. Sequenziando l’RNA di queste regioni, hanno potuto vedere quali geni erano attivi o spenti negli osteoblasti attivi, nelle cellule di rivestimento silenti e nelle cellule riattivate, preservando al contempo la posizione di queste cellule sulla superficie ossea.
Un freno chiave alla formazione ossea
Confrontando i profili di espressione genica degli osteoblasti attivi, inattivi e riattivati, un sistema di segnalazione è emerso come un potente freno: la via controllata dal fattore di crescita trasformante beta (TGF-β). Le cellule di rivestimento silenti mostravano una maggiore attività del TGF-β, mentre gli osteoblasti attivi—sia naturalmente attivi sia riattivati dal blocco della sclerostina—mostravano segnali di TGF-β più deboli. Il sequenziamento a singola cellula, che analizza migliaia di singole cellule ossee, ha confermato che gli osteoblasti più attivi presentano costantemente una segnalazione del TGF-β bassa. In organoidi ossei coltivati in laboratorio, l’aggiunta di TGF-β spingeva gli osteoblasti a diventare più sottili, meno proliferativi e più simili alle cellule di rivestimento. Questi risultati indicano il TGF-β come un interruttore che promuove la quiescenza e limita l’attività formatrice di osso.
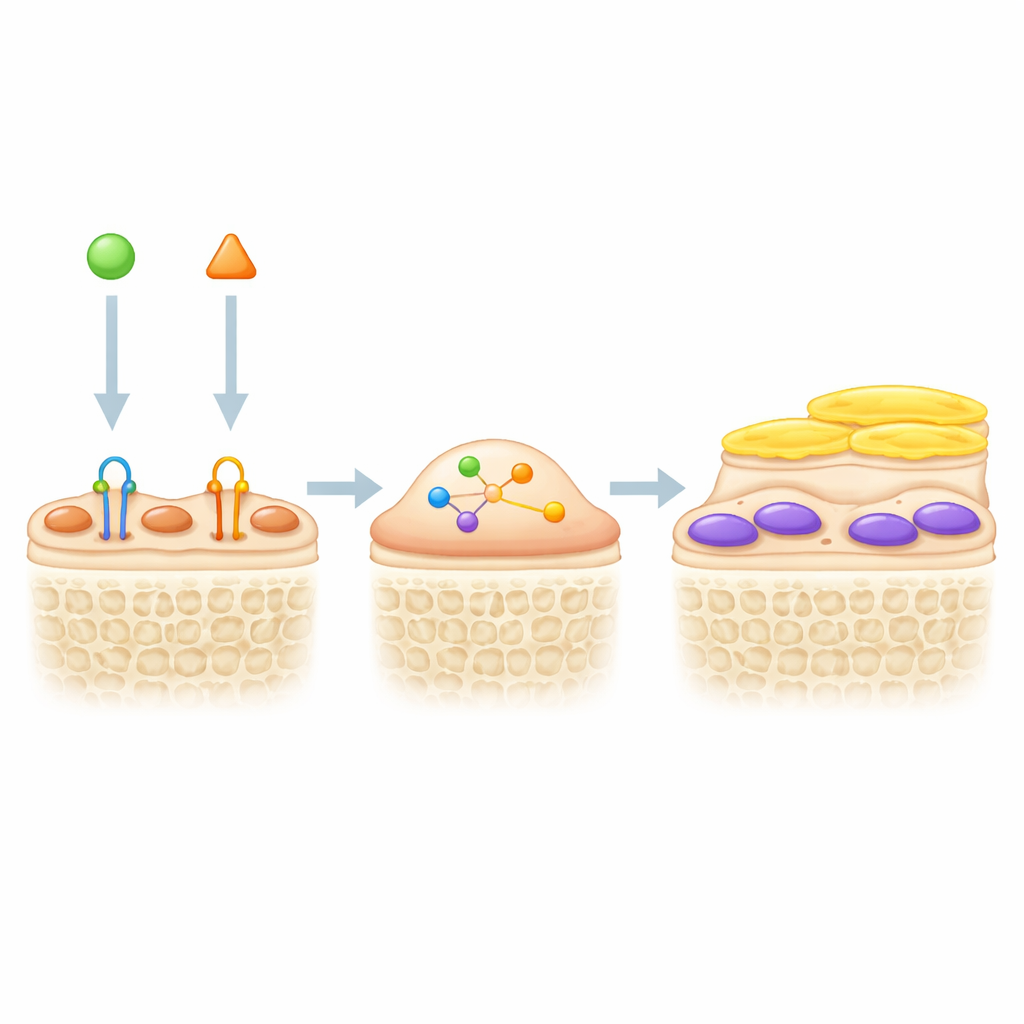
Combinare due leve per ossa più robuste
Poiché il blocco della sclerostina risveglia le cellule di rivestimento e il TGF-β le mantiene silenti, gli autori hanno testato se bloccare entrambi i segnali insieme avrebbe potenziato la formazione ossea. In topi geneticamente marcati, un anticorpo bloccante il TGF-β aumentava lo spessore e il numero di osteoblasti verdi attivi sulle superfici ossee, specialmente se combinato con il trattamento anti-sclerostina. In un modello di scarico dell’arto posteriore, che imita la perdita ossea dovuta all’inattività o ai voli spaziali, il blocco della sclerostina da solo aumentava la massa ossea, ma il trattamento doppio dava risultati ancora migliori. I topi trattati con entrambi gli anticorpi mostravano un maggiore volume osseo trabecolare, travi ossee più spesse e numerose, più formazione di osso e meno cellule che riassorbono l’osso rispetto ai topi che ricevevano uno solo dei farmaci. I marker ematici e le colorazioni tissutali suggerivano che l’inibizione del TGF-β non solo aiutava a riattivare le cellule di rivestimento, ma riduceva anche il riassorbimento osseo, agendo tramite meccanismi che si complementano al blocco della sclerostina.
Cosa potrebbe significare per i pazienti
Questo lavoro collega una via di segnalazione specifica, il TGF-β, alla decisione che le cellule ossee prendono tra riposo e attività costruttrice, e mostra che abbassare questo segnale può amplificare i benefici di un potente farmaco esistente per l’osteoporosi che prende di mira la sclerostina. Sebbene questi esperimenti siano stati condotti nei topi e rimangano importanti questioni di sicurezza—dato che il TGF-β agisce in molti organi—lo studio suggerisce che terapie duali opportunamente calibrate potrebbero sia risvegliare i costruttori ossei dormienti sia temperare il riassorbimento. A lungo termine, questa strategia potrebbe tradursi in trattamenti più robusti e duraturi per le persone con osteoporosi e altre condizioni caratterizzate da eccessiva perdita ossea.
Citazione: Choi, A., Lee, J.Y., Yoon, H. et al. Spatially resolved osteoblast-traced transcriptomics uncovers TGF-β as a combination target with sclerostin in osteoporosis. Bone Res 14, 37 (2026). https://doi.org/10.1038/s41413-026-00521-9
Parole chiave: osteoporosi, osteoblasti, rimodellamento osseo, segnalazione TGF-beta, inibizione della sclerostina